

El Átomo
Presentation
•
Chemistry
•
11th Grade
•
Hard
Joseph Anderson
FREE Resource
29 Slides • 17 Questions
1
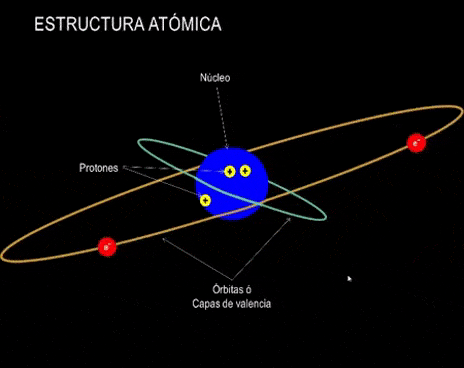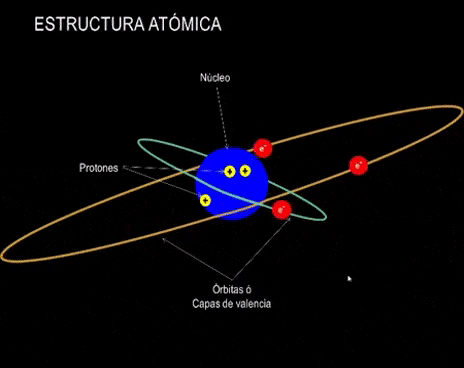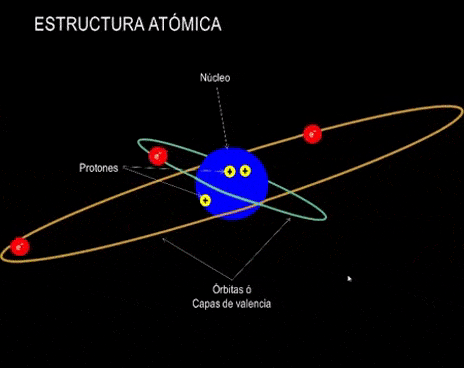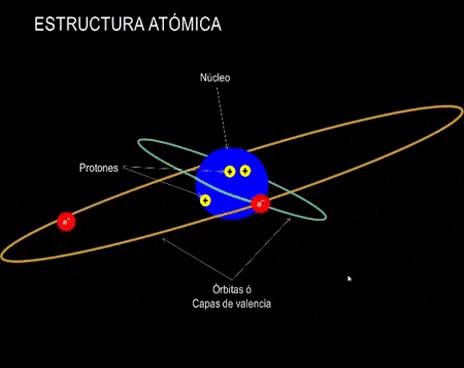
El átomo y su estructura

2
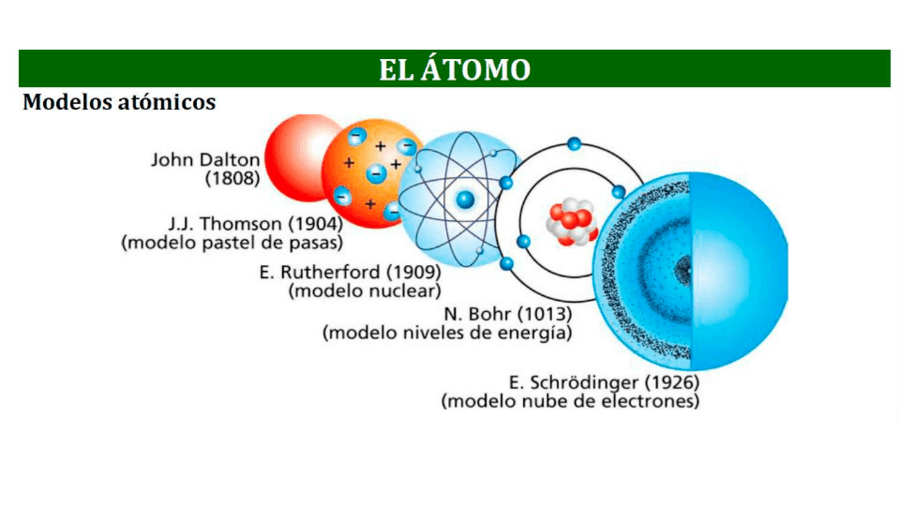
3

4

5
6

7

8
9
10
Multiple Choice
6. Si nos indican el siguiente elemento, 3889Sr podemos decir que está constituido por:
A) 89 protones, 89 electrones y 38 neutrones.
B) 38 protones, 38 electrones y 89 neutrones.
C) 51 protones, 51 electrones y 38 neutrones.
D) 38 protones, 38 electrones y 51 neutrones.
11
Multiple Choice
7. Indicar cuál es la composición del átomo 512B
A) 5 protones, 5 electrones y 12 neutrones.
B) 12 protones, 5 electrones y 5 neutrones.
C) 7 protones, 7 electrones y 5 neutrones.
D) 5 protones, 5 electrones y 7 neutrones
12

13
Multiple Choice
3. Indicar cuál de las siguientes afirmaciones es INCORRECTA:
A.
El número másico es el número de protones y neutrones que tiene un átomo en su núcleo.
B.
El número másico coincide siempre con el peso atómico del elemento de que se trate.
C.
En cualquier ion monoatómico positivo el número de protones es siempre mayor que el número de electrones.
D.
El número másico de un átomo es siempre igual o mayor que su número atómico.
14
Multiple Choice
4. El número atómico es:
A) El número de nucleones que tenga.
B) El número de protones que hay en el núcleo atómico, y que siempre coincide con el número de electrones de la corteza.
C) El número de electrones que hay en la corteza atómica.
D) El número de protones que hay en el núcleo atómico.
15

16

17

18
Multiple Choice
Los átomos que ganan electrones cuando establecen un enlace químico para completar la regla del octeto tienen una carga.
A) Positiva
B) Negativa
C) Isoelectrónica
D) Neutra
19

20

21

22

23

24
Multiple Choice
2. Dos átomos con el mismo número de protones y diferente número de neutrones reciben el nombre de:
A) Isotópicos
B) Isóbaros
C) Isostéricos
D) Isótopos
25
Multiple Choice
110. El carbono 12C6 y 14C6 son isotopos que presentan una variación en el número de:
A) Electrones
B) Protones
C) Neutrones
D) Orbitales
26
Multiple Choice
5. Si comparamos los valores del número atómico y del número másico de un determinado átomo, podremos observar que:
A) Siempre son diferentes.
B) El número másico es siempre mayor que el número atómico.
C) El número másico es siempre igual o mayor que el número atómico.
D) El número atómico es siempre mayor o igual que el número másico.
27

28

29

30

31

32

33
34
Multiple Choice
10. Un ion es una especie química que ha ganado o perdido electrones y por lo tanto tiene carga. La configuración electrónica para un átomo neutro "P" con Z = 19 es 1s2 2s2 2p6 3s2 3p6 4s1. De acuerdo con esto, la configuración electrónica más probable para el ion P2+ es:
A) 1s2 2s2 2p6 3s2 3p6 4s2
B) 1s2 2s2 2p6 3s2 3p6
C) 1s2 2s2 2p6 3s2 3p5
D) 1s2 2s2 2p6 3s2 3p6 4s2 3d1
35

36

37
Multiple Choice

9. El siguiente esquema representa parte de la información que contiene la tabla periódica.
Si se tiene en cuenta que los elementos que quedan ubicados en un mismo grupo presentan propiedades químicas semejantes, es válido afirmar que forman parte de un grupo los siguientes elementos
A) B, C y N
B) N, S y Br
C) Be, Mg y Ca
D) Li, Na y Be
38
Cuestionario
39
Multiple Choice

11. De acuerdo con la información de la tabla, es válido afirmar que los números de masa de X y Y son respectivamente:
A) 13 y 12
B) 11 y 6
C) 22 y 12
D) 23 y 14
40
Multiple Choice

12. El elemento X presenta en su último nivel de energía la configuración electrónica [Ne]3s2 3p5. Es probable que este elemento forme un compuesto iónico con un elemento cuya configuración electrónica en su último nivel de energía sea:
A. [Ne] 3s2
B. [Ne] 3s2 3p2
C. [Ne] 3s2 3p3
D. [Ne] 3s2 3p4
41
Multiple Choice

13. De acuerdo con la información presentada en la tabla es válido afirmar que:
A) X y Y son átomos de un mismo elemento con diferente carga
B) Z es el catión del elemento Y
C) X y Z son átomos de un mismo elemento diferente de Y
D) X y Y tienen la misma masa atómica
42
Multiple Choice

14. La mayor masa atómica corresponde a:
A) X = 19
B) Z y Y = 40
C) X y Y = 38
D) Z = 40
43
Multiple Choice

15. Son isótopos (átomos de un mismo elemento con diferente masa atómica):
A) Y y Z
B) Z y X
C) X y Y
D) Solo Y
44

45
Multiple Choice

El número másico de un átomo se presenta como A = Z + N; donde Z corresponde al número atómico o número de protones, que en un átomo neutro equivale también al número de electrones y N representa el número de neutrones. La siguiente tabla muestra algunas características de tres elementos
16. Es correcto afirmar que los números atómicos (X, X+1, X+2) para cada elemento son respectivamente:
A) 9; 10 y 11
B) 17; 18 y 19
C) 29; 30 y 31
D) 53; 54 y 55
46
Multiple Choice

17. El número de protones, neutrones y electrones respectivamente del elemento G es:
A) 10; 10; 10
B) 11; 10; 11
C) 12; 12; 12
D) 11; 12; 10
El átomo y su estructura

Show answer
Auto Play
Slide 1 / 46
SLIDE
Similar Resources on Wayground

44 questions
Introducción al estudio de Química
Presentation
•
12th Grade

41 questions
Алфавит наутявиковского языка
Presentation
•
KG

41 questions
Circles
Presentation
•
11th Grade

42 questions
Regents Review June 11
Presentation
•
11th - 12th Grade

39 questions
Quadratic Post Test Review
Presentation
•
11th Grade

40 questions
Functions - Linear
Presentation
•
11th Grade

42 questions
MATEMATICAS ICFES REFUERZO
Presentation
•
11th Grade

39 questions
Le Chatelier's Principle
Presentation
•
10th Grade
Popular Resources on Wayground

20 questions
"What is the question asking??" Grades 3-5
Quiz
•
1st - 5th Grade

20 questions
“What is the question asking??” Grades 6-8
Quiz
•
6th - 8th Grade

10 questions
Fire Safety Quiz
Quiz
•
12th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

34 questions
STAAR Review 6th - 8th grade Reading Part 1
Quiz
•
6th - 8th Grade

20 questions
“What is the question asking??” English I-II
Quiz
•
9th - 12th Grade

20 questions
Main Idea and Details
Quiz
•
5th Grade

47 questions
8th Grade Reading STAAR Ultimate Review!
Quiz
•
8th Grade