

Diagramas de fases
Presentation
•
Chemistry
•
University
•
Hard
Norberto Arango
Used 17+ times
FREE Resource
6 Slides • 2 Questions
1
Diagramas de fases
Se denomina diagrama de fase a la representación de las fronteras entre diferentes estados de la materia, en función de ciertas variables. Por ejemplo, el diagrama de fase del agua muestra las fronteras de transición entre los estados sólido (hielo), líquido (agua líquida) y gaseoso (vapor de agua), en función de la temperatura y la presión.

2
Multiple Choice
La temperatura crítica es
La máxima temperatura que puede soportar un gas
Temperatura por encima de la cual no es posible condensar un gas aplicándole presión
Temperatura mínima a la que se puede evaporar un líquido
La máxima temperatura que puede alcanzar un líquido
3
Multiple Choice
La Presión Crítica es
La mínima presión que se debe aplicar para llevar a cabo la condensación de un gas a la temperatura crítica
La máxima Presión que puede alcanzar un gas
La mínima presión posible
La máxima presión que puede soportar un líquido
4
5
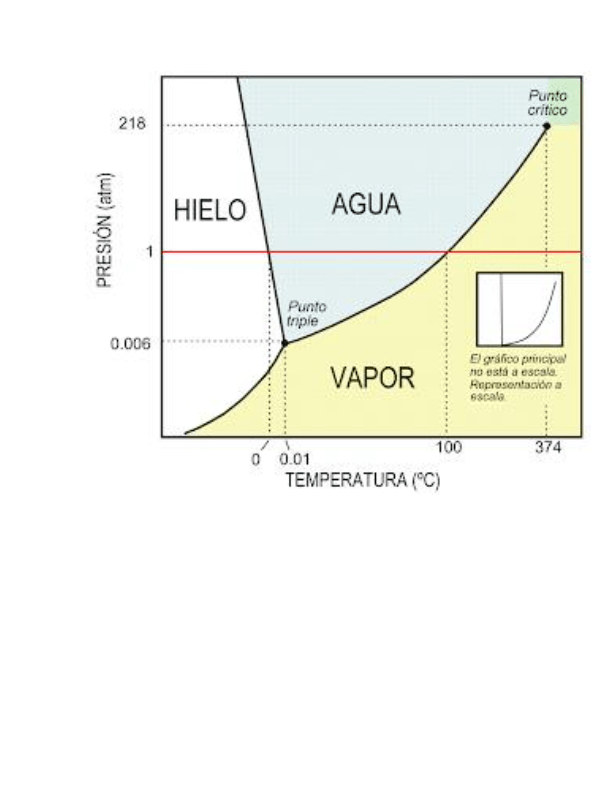
Las lineas que separan dos regiones son curvas de equilibrio entre dos fases
La línea entre el punto triple y el punto crítico representa el equilibrio entre las fases líquida y gaseosa y termina allí en el punto crítico
Cualquier punto sobre ésta línea describe un conjunto de condiciones temperatura y presión bajo las cuales el líquido y el vapor pueden existir en equilibrio.
La curva A-O representa el equilibrio entre la fase sólida y el vapor.
La O-B es la correspondiente al punto de fusión y representa las condiciones de equilibrio solido - líquido.
6
La intersección de las tres curvas en el punto O se denomina punto triple, donde coexisten las tres fases en equilibrio
El punto triple se presenta a una temperatura y presión que dependen de la naturaleza de las sustancias. Para el agua ocurre a 0,01 °C y a una presión de 4,58 mmHg
Cada una de las tres regiones del diagrama corresponde a un sistema monofásico, es decir, para cualquier valor de presión y temperatura que caiga dentro de la región, la sustancia está en la fase allí especificada
7
En la Tierra a nivel del mar estamos habituados a ver que el agua se congela a 0ºC y que se evapora a 100ºC. Esto se puede apreciar en la línea roja de la gráfica, que indica la presión de una atmósfera.
Sin embargo, si la presión se reduce lo suficiente, se podría observar como el hielo pasa a estado gaseoso directamente. O incluso encontrar un punto en el que se puede conseguir cualquiera de los tres estados con una pequeña variación de los parámetros (punto triple). Este punto presenta un gran interés para la calibración de termómetros de precisión.
.
8
Por otra parte, si aumentamos la temperatura y la presión se puede ver que la curva que separa las fases vapor-líquido se detiene en un punto llamado punto crítico. Más allá de este punto, la materia se presenta como un fluido supercrítico que tiene al mismo tiempo propiedades de un líquido y de un gas. Modificando la presión y temperatura en valores alrededor del punto crítico se producen reacciones que pueden tener interés industrial, como por ejemplo las utilizadas para obtener café descafeinado
Diagramas de fases
Se denomina diagrama de fase a la representación de las fronteras entre diferentes estados de la materia, en función de ciertas variables. Por ejemplo, el diagrama de fase del agua muestra las fronteras de transición entre los estados sólido (hielo), líquido (agua líquida) y gaseoso (vapor de agua), en función de la temperatura y la presión.

Show answer
Auto Play
Slide 1 / 8
SLIDE
Similar Resources on Wayground

4 questions
1ra lección
Presentation
•
University

4 questions
Materia y masa
Presentation
•
University

5 questions
Funciones químicas inorgánicas I
Presentation
•
University

5 questions
INGENIERÍA BIOQUÍMICA
Presentation
•
University

8 questions
Historia del peru
Presentation
•
University

8 questions
Naturaleza y origen de la justicia en La república de Platón
Presentation
•
KG

5 questions
SESION 3
Presentation
•
University

8 questions
Marie Curie II
Presentation
•
6th - 9th Grade
Popular Resources on Wayground

16 questions
Grade 3 Simulation Assessment 2
Quiz
•
3rd Grade

19 questions
HCS Grade 5 Simulation Assessment_1 2526sy
Quiz
•
5th Grade

10 questions
Cinco de Mayo Trivia Questions
Interactive video
•
3rd - 5th Grade

17 questions
HCS Grade 4 Simulation Assessment_2 2526sy
Quiz
•
4th Grade

24 questions
HCS Grade 5 Simulation Assessment_2 2526sy
Quiz
•
5th Grade

13 questions
Cinco de mayo
Interactive video
•
6th - 8th Grade

20 questions
Math Review
Quiz
•
3rd Grade

30 questions
GVMS House Trivia 2026
Quiz
•
6th - 8th Grade
Discover more resources for Chemistry

55 questions
Post Malone Addtion (Tres)
Quiz
•
12th Grade - University

20 questions
Disney Trivia
Quiz
•
University

50 questions
AP Biology Exam Review 2017
Quiz
•
11th Grade - University

24 questions
5th Grade Math EOG Review
Quiz
•
KG - University

12 questions
Star Wars Trivia - Easy
Quiz
•
KG - University

215 questions
8th Physical Science GA Milestones Review
Quiz
•
KG - University

40 questions
Famous Logos
Quiz
•
7th Grade - University

14 questions
(5-3) 710 Mean, Median, Mode & Range Quick Check
Quiz
•
6th Grade - University