

Ioonide teke
Presentation
•
Chemistry
•
8th Grade
•
Practice Problem
•
Medium
Merle Kairit
Used 23+ times
FREE Resource
14 Slides • 22 Questions
1
Ioonide teke
Keemia 8.klass
2
Tuletame meelde!
Üksikaatomitel on kõrge energia, seega on nad ebapüsivas olekus
Püsivas olekus on aatomid, mille väliskihil on tavaliselt 8 elektroni - seda nimetatakse ELEKTRONOKTETIKS
Aatom tervikuna oli NEUTRAALNE aineosake
Metalliaatomitel on väliskihil VÄHE elektrone, seega on neile iseloomulik elektronide LOOVUTAMINE
Mittemetalliaatomitel on väliskihil PALJU elektrone, seega on neile iseloomulik elektronide LIITMINE
3
Multiple Choice
Üksikaatomite energia on
kõrge
madal
energia puudub
4
Multiple Choice
Aatom on püsivas olekus, kui tema väliskihil on
2 elektroni
4 elektroni
6 elektroni
8 elektroni
5
Multiple Choice
Kui aatomil on väliskihil 8 elektroni, siis on tal
elektronoktett
elektronkvintett
elektronkvartett
6
Multiple Choice
Metalliaatomitel on väliskihil
palju elektrone
vähe elektrone
7
Multiple Choice
Metalliaatomitele on iseloomulik elektronide
liitmine
loovutamine
8
Multiple Choice
Mittemetalliaatomitel on väliskihil
vähe elektrone
palju elektrone
9
Multiple Choice
Mittemetalliaatomitele on iseloomulik elektronide
liitmine
loovutamine
10
Ioonide teke
Aatom on tervikuna neutraalne
Aatomid on võimelised väliskihile elektrone juurde võtma ehk liitma või ära andma ehk loovutama
Elektrone liidavad mittemetallid ja loovutavad metallid
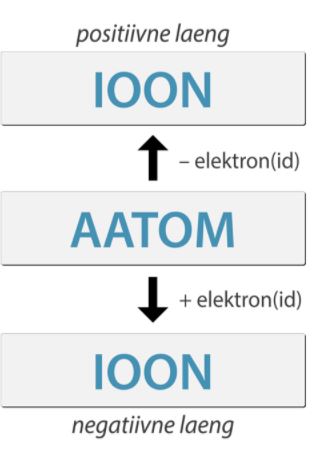
Aatomit, mis on elektrone juurde võtnud või ära andnud, nimetatakse IOONIKS
Ioon on laenguga aatom
11

12

13
Naatriumiooni teke
Naatriumi aatomi elektronskeem Na: +11/2)8)1)
Na aatomi väliskihil on 1 elektron, mille ta loovutab mingile teisele aatomile Na - 1e- --> Na+
Tekib naatriumioon, millel on positiivne laeng
Iooni elektronskeem Na+: 11/2)8)
Positiivne ioon ehk katioon
14

15
Kloriidiooni teke
Kloori aatomi elektronskeem
Cl: +17/2)8)7)
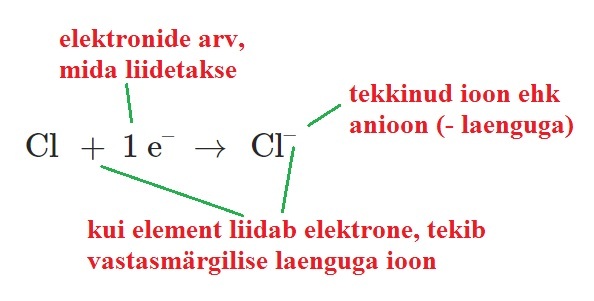
Cl aatomi väliskihil on 7 elektroni, kuhu ta võtab juurde 1 elektroni
Cl + 1e- --> Cl-
Tekib kloriidioon, millel on negatiivne laeng
Iooni elektronskeem Cl-: 17/2)8)8)
Negatiivne ioon ehk anioon

16
17
Ioonide teke
Kui metallil on väliskihil 2 elektroni, siis loovutab ta mõlemad ja saab laenguks 2+, näiteks Mg: +12/2)8)2) = > Mg - 2e- --> Mg2+
Kui mittemetallil on väliskihil 6 elektroni, siis on elektronoktetist puudu veel 2 elektroni ja ta võtab need juurde ning saab negatiivse laengu (2-), näiteks S: +16/2)8)6) => S + 2e- --> S2-
Kokkuvõtteks: kui aatom loovutab elektrone, on iooni laeng positiivne; kui aatom liidab elektrone, on iooni laeng negatiivne!
18
Multiple Choice
Laenguga aatom on
ioon
neoon
müoom
joon
19
Multiple Choice
Kui aatom loovutab elektrone, siis tekkinud iooni laeng on
positiivne
negatiivne
neutraalne
20
Multiple Choice
Kui aatom liidab elektrone, siis tekkinud iooni laeng on
positiivne
negatiivne
neutraalne
21
Multiple Choice
Positiivse laenguga iooni nimetatakse
aniooniks
katiooniks
maniooniks
minioniks :)
22
Multiple Choice
Negatiivse laenguga iooni nimetatakse
aniooniks
katiooniks
maniooniks
minioniks :)
23
Multiple Choice
Kas alumiiniumi aatom liidab või loovutab väliskihi elektrone?
Al: +13/2)8)3)
Liidab
Loovutab
24
Multiple Choice
Millise laenguga ioon saab tekkida alumiiniumi aatomist?
Al: +13/2)8)3)
3+
3-
5+
5-
25
Multiple Choice
Kas lämmastiku aatom liidab või loovutab väliskihi elektrone?
N: +7/2)5)
Liidab
Loovutab
26
Multiple Choice
Mitu elektroni lämmastiku aatom saab väliskihile juurde võtta?
N: +7/2)5)
2 elektroni
3 elektroni
4 elektroni
5 elektroni
27
Multiple Choice
Millise laenguga ioon saab lämmastiku aatomist tekkida?
N: +7/2)5)
3+
3-
5+
5-
28
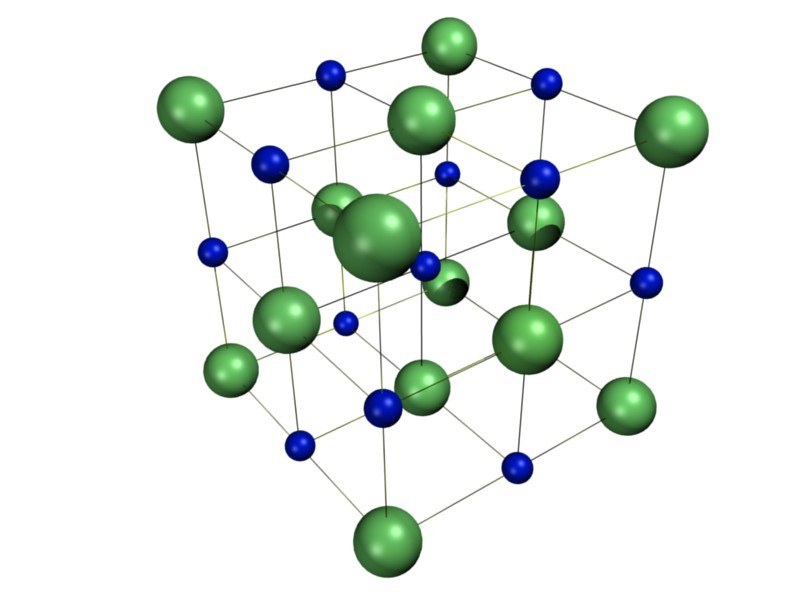
Iooniline side
Iooniline side on vastasmärgiliste ioonide tõmbumine
Iooniline side tekib elektronide üleminekul aktiivselt metallilt aktiivsele mittemetallile
Ioonilise sidemega ained EI MOODUSTA molekule, vaid kristalle
Iooniline side esineb metalli ja mittemetalli aatomite vahel
29

30

31
Multiple Choice
Märgi ioonilise sidemega aine.
CaO
Br2
N2O
32
Multiple Choice
Märgi ioonilise sidemega aine.
H2S
BaCl2
HCl
33
Multiple Choice
Millise valemiga aine tekib, kui on järgmised ioonid: Na+ ja S2-?
NaS
Na2S
NaS2
34
Multiple Choice
Millise valemiga aine tekib, kui on järgmised ioonid: Mg2+ ja O2-?
MgO
Mg2O
MgO2
35
Multiple Choice
Millise valemiga aine tekib, kui on järgmised ioonid: Al3+ ja O2-?
AlO
Al3O2
Al2O3
36
Tänan tähelepanu eest!
Olid väga tubli! :)
Ioonide teke
Keemia 8.klass

Show answer
Auto Play
Slide 1 / 36
SLIDE
Similar Resources on Wayground

11 questions
Vesinik
Presentation
•
9th - 12th Grade

9 questions
Elektronski omotač
Presentation
•
KG

30 questions
Aatomi ehituse seosed perioodilisussüsteemiga
Presentation
•
8th Grade

26 questions
Zgradba atoma
Presentation
•
8th Grade

15 questions
Ioonid
Presentation
•
7th Grade

34 questions
Keemia ajalugu
Presentation
•
9th - 12th Grade
Popular Resources on Wayground

15 questions
Grade 3 Simulation Assessment 1
Quiz
•
3rd Grade

22 questions
HCS Grade 4 Simulation Assessment_1 2526sy
Quiz
•
4th Grade

16 questions
Grade 3 Simulation Assessment 2
Quiz
•
3rd Grade

19 questions
HCS Grade 5 Simulation Assessment_1 2526sy
Quiz
•
5th Grade

17 questions
HCS Grade 4 Simulation Assessment_2 2526sy
Quiz
•
4th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

24 questions
HCS Grade 5 Simulation Assessment_2 2526sy
Quiz
•
5th Grade

20 questions
Math Review
Quiz
•
3rd Grade
Discover more resources for Chemistry

10 questions
Exploring Properties and Models of Acids and Bases
Interactive video
•
6th - 10th Grade

10 questions
Identifying Types of Chemical Reactions
Interactive video
•
6th - 10th Grade

20 questions
Counting Atoms Practice
Quiz
•
8th Grade

20 questions
States of Matter
Quiz
•
8th Grade

41 questions
Atomic Structure and Periodic Table Unit Review
Quiz
•
8th Grade

20 questions
Chemical Reactions
Quiz
•
8th Grade

10 questions
Exploring Stoichiometry Concepts
Interactive video
•
6th - 10th Grade

10 questions
Exploring Solutions and Their Properties
Interactive video
•
6th - 10th Grade