

Remedial Termokimia
Presentation
•
Chemistry
•
11th Grade
•
Medium
Rara Aprilia
Used 12+ times
FREE Resource
39 Slides • 17 Questions
1
Indikator
Memahami pengertian termokimia
Memahami pengertian sistem
Menjelaskan pembagian sistem
Memahami hukum kekekalan energi
Menjelaskan energi dalam suatu materi
Memahami reaksi endoterm dan eksoterm
2
Sistem dan Lingkungan
Sistem adalah bagian dari alam semesta yang menjadi pusat perhatian kita.
Lingkungan adalah bagian dari alam semesta yang membatasi sistem.
Pada gambar tersebut:
Sistem: air yang dipanaskan
Lingkungan: segala sesuatu yang ada di luar sistem

3

Apakah sama antara kalor dan suhu?
Some text here about the topic of discussion.
4

5
TERMOKIMIA
Termo = Thermo
"berhubungan dengan panas"
Bagian dari ilmu kimia yang mempelajari tentang.....
"Perubahan Energi yang menyertai Reaksi Kimia dalam suatu Sistem"
6
Untuk apa kita mempelajari termokimia?
Dengan memahami termokimia, kita dapat:
memilih suatu bahan yang dapat digunakan sebagai sumber energi dengan nilai ekonomis yang tinggi
Menghitung dengan tepat jumlah bahan bakar yang diperlukan untuk suatu kebutuhan

7
memilih reaksi zat-zat untuk tujuan tertentu, misalnya untuk mengompres panas tubuh penderita demam tinggi dimanfaatkan reaksi zat yang berlangsung endotermis
dan kegunaan lainnya

8
MOTIVASI
9

10

Pembagian Sistem
11
1. Hukum Pertama Termokimia
12
Multiple Choice

gambar tersebut merupakan contoh sistem terisolasi karena . . . .
tidak terjadi pertukaran energi
tidak terjadi pertukaran materi
tidak terjadi pertukaran materi dan energi
terjadi pertukaran energi dan materi
13
Multiple Select
Tina mereaksikan larutan HCl dengan larutan NaHCO3 ke dalam beker glas. Agar mendapatkan campuran larutan yang sempurna, Tina mengaduknya dengan batang pengaduk. Berdasarkan deskripsi tersebut yang merupakan sistem adalah ...
larutan HCl
larutan NaHCO3
beker gelas
batang pengaduk
s
14

15
Multiple Choice
Jika reaksi antara logam Barium dengan Asam Klorida encer di campurkan ke
d alam tabung reaksi yang tersumbat dengan rapat, gas Hidrogen di dalam sistem tidak dapat meninggalkan sistem. Akan tetapi perambatan kalor meninggalkan sistem tetap terjadi melalui dinding pada tabung reaksi. Maka percobaan ini termasuk ke dalam…
Sistem Terbuka
Sistem tertutup
Sistem terisolasi
Perubahan energi dalam
16
Open Ended
Jika sepotong logan Barium (Ba) direaksikan dengna asam klorida (HCl) encer pada suatu sistem terbuka dengan reaksi Ba (s) + 2HCl(aq) → BaCl2(aq) + H2
pada reaksi tersebut sistem melepas kalor sebesar 150 kJ dan menghasilkan gas yang akan menyebabkan terjadinya perubahan volume. sistem juga melakukan kerja sebesar 45 kJ. Perubahan energi dalam pada proses tersebut adalah ... kJ (fotokan hasil perhitungannya)
17


18
Multiple Choice
Perubahan energi dalam yang terjadi pada suatu sistem yang menyerap 20 kJ dan menerima usaha sebesar 110 kJ adalah....
90 kj
100 kj
110 kj
120 kj
130 kj
19

20

21

22

23

Contoh Reaksi Eksoterm
*pembakaran
*karat
*kondensasi
*kristalisasi
Some text here about the topic of discussion.
24
Contoh Endoterm
*fotosintesis
*mencair
*pelarutan urea
Some text here about the topic of discussion
25
Sesungguhnya energi kalor pada proses kimia hanya berpindah dari satu bagian ke bagian lain dari alam semesta.

26
Multiple Choice
Jika satu sendok serbuk seng dimasukkan ke dalam gelas kimia yang berisi larutan HCl, ternyata terbentuk gelembung gas dan dasar tabung terasa panas. Reaksi ini dapat digolongkan :
Eksoterm, energi berpindah dari sistem ke lingkungan
Eksoterm, energi berpindah dari lingkungan ke sistem
Endoterm, energi berpindah dari sistem ke lingkungan
Endoterm, energi berpindah dari lingkungan ke sistem
Endoterm, energi tidak berpindah
27
Open Ended
Energi panas atau kalor mengalir dari suhu ..... ke ......
28
Open Ended
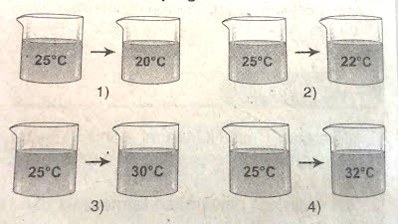
Terjadinya reaksi endoterm ditunjakkan pada gambar nomor…
29
Multiple Choice

Perhatikan gambar berikut ini !
Reaksi tersebut termasuk ke dalam reaksi ....
eksoterm, karena H pereaksi < H hasil reaksi, ΔH = -
endoterm, karena H pereaksi < H hasil reaksi, ΔH = +
eksoterm, karena H pereaksi > H hasil reaksi, ΔH = +
endoterm, karena H pereaksi > H hasil reaksi, ΔH = -
endoterm, karena H pereaksi = H hasil reaksi, ΔH = +
30
Multiple Choice
Perhatikan data berikut :
Reaksi I : C3H8 + 5 O2 ⟶ 3 CO2 + 4 H2O ΔH = – P kJ
Reaksi II : NH4Cl + NaOH ⟶ NH3 + NaCL ΔH = + Q kJ
Pernyataan yang benar dari data tersebut adalah ....
Reaksi I sistem melepas kalor , reaksi eksoterm
Reaksi II sistem menyerap kalor, reaksi eksoterm
Reaksi II lingkungan menyerap kalor, reaksi eksoterm
Reaksi I lingkungan menyerap kalor, reaksi endoterm
Reaksi II lingkungan menyerap kalor, reaksi endoterm
31

32

33

34

35

36

37
Multiple Choice
Persamaan termokimia yang benar untuk pembentukan 1 mol H2O dari unsur – unsur nya adalah . . .
2H2 + O2 → 2H2O
H2 + 2O2 → H2O
2H2O → 2H2 + O2
½ H2 + O2 → H2O
H2 + ½ O2 → H2O
38
Multiple Choice
Pernyataan di bawah ini benar tentang reaksi endoterm, kecuali....
Menyerap kalor
∆H bernilai negatif
entalpi bernilai positif
entalpi produk > entalpi pereaksi
39
Multiple Choice
1. Persamaan termokimia yang benar untuk pembentukan 1 mol H2O dari unsur – unsur nya adalah . . .
2H2 + O2 → 2H2O
H2 + 2O2 → H2O
2H2O → 2H2 + O2
½ H2 + O2 → H2O
H2 + ½ O2 → H2O
40

41

42

43

44

45

46

47

48

49

50

51

52

53
Multiple Choice

-40 kJ
-140 kJ
+40 kJ
+140 kJ
54
Multiple Choice
Tentukan ΔH reaksi berikut.
CH4(g) + 2O2(g) ----> CO2(g) + 2H2O(l)
Jika diketahui
Δ𝐻𝑓0 CH4 (g) = -75kJ/mol
Δ𝐻𝑓0 H2O (l) = -285kJ/mol
+898 kJ/mol
+233 kJ/mol
-233 kJ/mol
-898 kJ/mol
55
Multiple Choice

Jika energi ikatan rata- rata dari ;
– 510 kkal
– 72,8 kkal
– 12 kkal
+ 12 kkal
+ 510 kkal
56
Multiple Choice
Perhatikan persamaan reaksi termokimia di bawah ini:
1. ½ N2 (g) + ½ O2 (g) → NO (g) ΔH = +kJ/mol
2. NO2 (g) → ½ N2 (g) + O2 (g) ΔH = −kJ/mol
3. CO2 (g) → C (s) + O2 (g) ΔH = +kJ/mol
4. C2H5OH + 3O2 → 2CO2 + 3H2O ΔH = −kJ/mol
5. Na (s) + ½ Cl2 (g) → NaCl ΔH = −kJ/mol
Persamaan reaksi yang merupakan ΔHfo, ΔHdo, dan ΔHco berturut-turut adalah ….
(3), (4), dan (5)
(2), (4), dan (5)
(1), (3), dan (5)
(1), (2), dan (4)
(1), (2), dan (3)
Indikator
Memahami pengertian termokimia
Memahami pengertian sistem
Menjelaskan pembagian sistem
Memahami hukum kekekalan energi
Menjelaskan energi dalam suatu materi
Memahami reaksi endoterm dan eksoterm
Show answer
Auto Play
Slide 1 / 56
SLIDE
Similar Resources on Wayground

57 questions
Module 6: Lesson 3: Names & Formula for Ionic Compounds (pg 180)
Presentation
•
10th Grade

47 questions
AP physics review
Presentation
•
10th - 12th Grade

47 questions
Rasamala VC Desember 2021
Presentation
•
12th Grade

45 questions
Termodinamika (2)
Presentation
•
11th Grade

51 questions
10.1 ANCAMAN ALAM SEKITAR
Presentation
•
11th Grade

47 questions
Preicfes 2024
Presentation
•
11th Grade

53 questions
Add Maths Marathon!
Presentation
•
12th Grade

49 questions
ÇOCUKTA DAVRANIŞ YÖNETİMİ
Presentation
•
12th Grade
Popular Resources on Wayground

20 questions
Math Review
Quiz
•
3rd Grade

15 questions
Fast food
Quiz
•
7th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

19 questions
Classifying Quadrilaterals
Quiz
•
3rd Grade

20 questions
Figurative Language Review
Quiz
•
6th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

10 questions
Identify Fractions, Mixed Numbers & Improper Fractions
Quiz
•
3rd - 4th Grade