

QT1S06 Historia del átomo
Presentation
•
Chemistry
•
9th Grade
•
Medium
Arturo Rodríguez
Used 5+ times
FREE Resource
0 Slides • 91 Questions
1
Multiple Choice
2
Multiple Choice

Según Dalton ¿Qué caracteriza al átomo?
Es indestructible
Es divisible
Es idéntico a otro átomo
Es esférico, macizo, indivisible e indestructible
3
Multiple Choice
Partícula subatómica con carga positiva.
esfera
electrón
neutrón
protón
4
Multiple Choice
¿Quiénes fueron los precursores de la Teoría Atomista?
Aristóteles y Demócrito
Leucipo y Thomson
Leucipo y Demócrito
Aurelio y Aristóteles
5
Multiple Choice

Observa la imagen y selecciona a cual tipo de modelo atómico corresponde
Dalton
Leucipo y Demócrito
Rutherford
Bohr
6
Multiple Select
El número atómico me indica:
la cantidad de neutrones
7
Multiple Choice
¿Quién propuso el término átomo?
John Dalton
J.J. Thomson
Ernest Rutherford
Demócrito
8
Multiple Choice
197 y un número atomico de 79
Tiene 79 electrones y 110 neutrones
Tiene 79 electrones y 118 neutrones
9
Multiple Select
Leucipo sostenia que si dividimos la materia en partes cada vez mas pequeñas acabariamos encontrando una...
porcion que se seguiria dividiendo
porción que no se podría seguir dividiendo.
ninguna de las anteriores
10
Multiple Choice
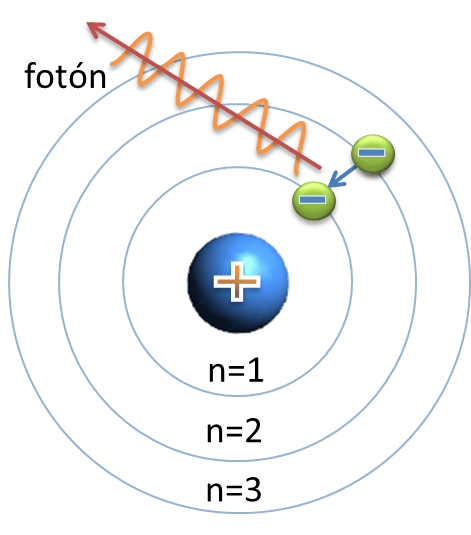
Thomson
Bohr
Rutherford
11
Multiple Choice

¿Quién descubrió el núcleo del átomo?
Niels Bohr
Ernest Rutherford
J.J. Thomson
Louis de Broglie
12
Multiple Choice

¿Por qué el átomo es eléctricamente neutro?
Porque los protones y neutrones se encuentran separados
Porque el número de protones es igual al de neutrones
Porque tiene igual cantidad de protones que de electrones
Porque los electrones son la carga representativa del átomo
13
Multiple Choice

Científico que experimentó con los rayos catódicos
Jhon Dalton
J.J. Thomson
Niels Bohr
Ernest Rutherford
14
Multiple Choice
¿Qué son los niveles de energía en el modelo Bohr?
Lugar donde están los protones
Distintas orbitas donde se mueven los electrones
Zona donde se mueven los electrones
Zona más densa del atomo
15
Multiple Choice

El experimento de los rayos catódicos fue crucial para descubrir una partícula subatómica que tiene una carga eléctrica :
Positiva
negativa
neutra
inversa
16
Multiple Choice
¿Quién hizo el experimento de la placa de oro?
Dalton
Thompson
Rutherford
Bohr
17
Multiple Choice

EL siguiente modelo fue propuesto por..... y se le llamó:.......
Bohr/ sistema planetario
Thomson / budín de pasas
Dalton/ esfera rígida
18
Multiple Choice
La configuración electrónica me indica cómo están organizados los electrones alrededor del núcleo.
Las configuraciones electrónicas que corresponde a los elementos Na de numero atómico 11 y Cl de numero atómico 17 son respectivamente
1s2 2s2 2p6 3s1 y 1s2 2s2 2p6 3s2 3p5
1s2 2s2 2p6 3s1 y 1s2 2s2 2p6
1s2 2s2 2p6 3s2 y 1s2 2s2 2p6 3s2 3p5
1s2 2s2 2p6 y 1s2 2s2 2p5
19
Multiple Choice

La imagen representa el modelo atómico de
Sommerfeld
Dalton
Bohr
Thomson
20
Multiple Choice
A partir de la distribución electrónica, sería correcto afirmar que el elemento con numero atómico 6
esta en el período 3 y el grupo III A
se ubica en el sector s, con un periodo de 3 y un grupo de IIIA
se ubica en un periodo 3 y un grupo IIIB, siendo un elemento de transición
es un no metal, es del grupo IVA y en el período 2
21
Multiple Choice
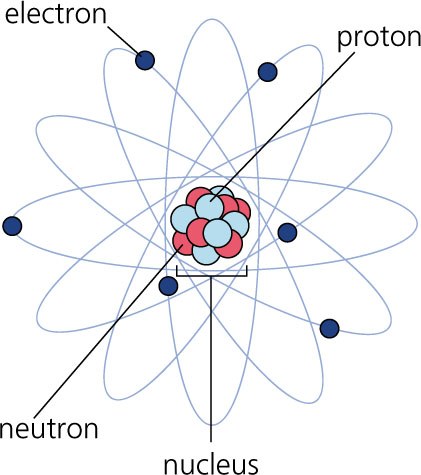
¿Qué carga tiene el electrón?
22
Multiple Choice

Con base en la imagen se puede ubicar al elemento en
El grupo III y el período 8
El grupo 18 y el período 2
El grupo VIIIA y en el período 3
El grupo 8B y período 4
23
Multiple Choice

Uno de los postulados de Dalton dice que:
Los átomos de un mismo elemento son iguales pero cambian al combinarse con otros átomos.
Los átomos de un mismo elemento son iguales entre sí, tienen el mismo peso e iguales propiedades.
Los átomos de los elementos solo se combinan con átomos iguales.
Los átomos pueden dividirse según la reacción química que se produzca.
24
Multiple Choice
Hojalata es la lámina delgada de acero con revestimiento de estaño.
La distribución electrónica del estaño es
1S2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p2;
el grupo y el período en el que se encuentra en la tabla periódica son
grupo VA, período 4
grupo IVA, período 5
grupo IIA, período 5
grupo VA, período 2
25
Multiple Choice
¿Qué partícula fundamental del átomo tiene menor masa?
Neutrón
Protón
Electrón
26
Multiple Choice
La configuración electrónica de un elemento es 1s2 2s2 2p6 3s2 3p5.
Con esta única información se puede determinar
I. el grupo al que pertenece el elemento en la tabla periódica
II. el número atómico del elemento
III. el período al que pertenece el elemento en la tabla periódica.
sólo I
sólo I y II
tanto I, II y III
solo II y III
27
Multiple Choice
Plantea que los electrones se mueven a travez de órbitas...
Dalton
Borh
Rutherford
Thompson
28
Multiple Choice

En la estructura del H2SO4.
El estado de oxidación o valencia del azufre es
+6
-2
+1
-6
29
Multiple Choice
30
Multiple Choice

En la estructura de Lewis del HClO4
el hidrógeno gana 1 electrón
el cloro pierde 7 electrones
el oxigeno tiene valencia +2
el cloro tiene valencia -7
31
Multiple Select
¿Cuáles son las partículas que se encuentran ubicadas en el núcleo?
Electrones
Neutrones
Protones
32
Multiple Choice

Según la imagen los números de oxidación o valencia del carbono y el oxigeno son respectivamente
-2 y +5
+1 y +5
+6 y -2
+4 y -2
33
Multiple Choice
¿Quién descubrió el neutrón?
Thompson
Goldstein
Dalton
Chadwick
34
Multiple Choice

Considere la estructura de Lewis donde E es un elemento desconocido (ver imagen)
¿Cuál elemento de la lista se identifica con E?
O
S
Br
Xe
35
Multiple Choice

¿Por qué el átomo es eléctricamente neutro?
Porque los protones y neutrones se encuentran separados
Porque el número de protones (positivo) es igual al de neutrones
Porque tiene igual cantidad de protones que de electrones
Porque los electrones son la carga representativa del átomo
36
Reorder
Ordena los modelos atómicos según fueron diseñados (del antiguo al moderno)
37
Multiple Choice

Thomson
Bohr
Rutherford
38
Multiple Select

Observa la imagen e identifica a que modelo atómico corresponde.
Modelo de Rutherford
Modelo de Dalton
Modelo de Bohr
Modelo de Thomson
39
Multiple Choice

En el modelo atómico de Thomson aparece el concepto de:
Rayo gamma
Orbital energético
Electrón
Número cuántico
40
Multiple Choice

¿Quién descubrió el núcleo del átomo?
Niels Bohr
Ernest Rutherford
J.J. Thomson
Louis de Broglie
41
Multiple Choice

El esquema representa el modelo atómico de:
Bohr
Sommerfeld
Atomismo
Thomson
42
Multiple Choice
Selecciona el modelo atómico de Dalton
43
Multiple Choice
Una de estas afirmaciones es correcta:
Las cargas positivas repelen a las negativas
Cargas desiguales se repelen, cargas iguales se atraen
Cargas desiguales se atraen, cargas iguales se repelen
Los electrones se mueven de la carga positiva a la carga negativa
44
Multiple Choice

Científico que experimentó con los rayos catódicos
JJ Thomson
Ernest Rutherford
Niels Boh
Jhon Dalton
45
Multiple Select
Selecciona la respuesta que no sea correcta.
El elemento Cl tiene valores de 17 y 35 de Z y A respectivamente, con ello podemos concluir que:
El cloro tiene 52 de numero atómico
El cloro tiene 17 protones
El cloro tiene 17 electrones
El cloro tiene 18 neutrones
46
Multiple Choice

Científico que experimentó con los rayos catódicos
Jhon Dalton
J.J. Thomson
Niels Bohr
Ernest Rutherford
47
Multiple Choice

¿Qué partículas encontramos dentro del núcleo de cualquier átomo?
Protones y electrones
Neutrones y electrones
Protones y neutrones
Protones, neutrones y electrones
48
Multiple Choice
¿Cuál de las siguientes proposiciones no es un postulado de la teoría atómica de Dalton?
La materia está formada por átomos.
Los átomos de un elemento son idénticos entre sí.
Los átomos están formados por partículas subatómicas.
Los átomos de un elemento no pueden transformarse en otros.
49
Multiple Choice
Afirmaba que un átomo solo sería igual a otro si pertenecía al mismo elemento
Leucipo
Dalton
Demócrito
Thonson
50
Multiple Choice

¿Qué se muestra en la imagen?
Una célula
Un órgano
Una molécula
51
Multiple Choice
En uno de estos experimentos, utilizaron partículas alfas para hacerlas incidir en una lámina de oro delgada y así poderla atravesar. Este experimento comprobó la teoría de :
Rutherford
Dalton
Thomson
Bhor
52
Multiple Choice
Osciloscopio
Atomizador de aceite, fuente de luz, microscopio
53
Multiple Choice
¿A qué teoría pertenece el siguiente postulado?"Un electrón solo emite o absorbe energía cuando se mueve de una órbita permitida a otra"
Dalton
Bohr
Rutherford
Thomson
54
Multiple Choice
Decía: "Los electrones se distribuyen en orbitales que son regiones donde existe la mayor probabilidad de encontrar a un electrón".
Rutherford
Bohr
De Broglie
E. Schrodinger
55
Multiple Select
Selecciona todas las respuestas que sean correctas sobre la estructura del átomo
El núcleo atómico es una estructura de gran tamaño
Los electrones giran alrededor del núcleo
Los átomos tiene cargas positivas dentro del núcleo
Los átomos son partículas sólidas
56
Multiple Choice
Se encuentra alrededor del núcleo y esta constituido por orbitas.
Nube electrónica
Núcleo atómico
Partículas subatómicas
57
Multiple Select

El Número Atómico (Z) me indica:
Los Neutrones y Protones
Los Protones
Los Protones y Los Electrones
Los Electrones
58
Multiple Choice
El átomo presenta las siguientes partículas sub-atómicas :
Electrón. neutrón y metaloide
Electrón, neutrón y protón
Protón, uranio y electrón
neutrón, protón y metal.
59
Multiple Choice
Radiactividad es sinónimo de:
Desintegración
Agregación
Fusión
Especiación
60
Multiple Choice
Los protones y neutrones se ubican dentro del átomo en :
la nube electrónica
la tabla periódica
los elementos químicos
el núcleo
61
Multiple Choice
Propuso que los electrones giran alrededor del núcleo en unos niveles bien definidos.
Rutherford
Bohr
Dalton
Demócrito
62
Multiple Choice
El electrón se encuentra en el átomo en la siguiente ubicación :
En el núcleo
En el protón
En el neutrón
En los orbitales
63
Multiple Choice
¿Cuál es el modelo atómico que propone Ernest Rutherford?
64
Multiple Choice
¿Por qué los átomos son diferentes?
Presentan diferentes cantidades de electrones y protones
Presentan diferentes cantidades de electrones y neutrones
Presentan diferentes cantidades de neutrones y electrones
Presentan diferentes cantidades de electrones, protones y neutrones
65
Multiple Choice

Los electrones hacen parte de la particulas subatomicas del atomo, esta se encuentra:
En el núcleo del átomo
En el núcleo y en las orbitas
En las orbitas
Quarks
66
Multiple Choice
Son los subniveles que encontramos dentro de los niveles de energía
s, p, d, f
s, p
s, p, f ,d
p, s, d, f
67
Multiple Choice
Se extiende alrededor del núcleo y está constituida por orbitales o reempes.
Nube electrónica
Núcleo atómico
Partículas subatómicas
68
Multiple Choice

Un orbital atómico es:
una región donde puedo encontrar un protón en movimiento
un espacio donde se encuentran los neutrones
la región donde existe la posibilidad de encontrar un electrón en movimiento.
69
Multiple Choice

El filósofo griego que sostenía que la materia estaba constituida por 4 elementos (tierra, aire, fuego y agua).
70
Multiple Choice
¿Cuál de las siguientes imágenes representa el movimiento de los electrones en el orbital s?
71
Multiple Choice
Iones son átomos que tienen la características de perder o ganar :
Protones
Electrones
Neutrones
Masa Atómica
72
Multiple Choice
¿Cuál de las siguientes imágenes representa el movimiento de los electrones en el orbital p?
73
Multiple Choice
Un átomo tiene Z=9 y 10 neutrones. ¿Cuál es su número másico (A)?
9
10
19
1
74
Multiple Choice
El núcleo de un átomo contiene:
p+ y n°
solo n°
e- y p+
Solo p+
75
Multiple Choice
EL núcleo de un átomo contiene:
p+ y n°
solo n°
e- y p+
Solo p+
76
Multiple Choice

¿Qué carga tiene el electrón?
77
Multiple Choice

Científico que experimentó con los rayos catódicos
Jhon Dalton
J.J. Thomson
Niels Bohr
Ernest Rutherford
78
Multiple Choice

Esta imagen representa el modelo atómico de:
Sommerfeld
Bohr
Heisenberg
Thomson
79
Multiple Choice
El elemento Carbono tiene el numero atómico seis y por tanto tiene en su estructura atómica:
80
Multiple Select
El modelo llamado pudín o panqué con pasas lo propúso
Leucipo
Demócrito
Dalton
Thomson
81
Multiple Choice
¿Qué partícula subatómica tiene una carga negativa (-)?
Protón
Electrón
Neutrón
82
Multiple Choice
Es la partícula más pequeña de la materia que puede existir como
compuesto.
Un elemento
Una molécula
Una sustancia
83
Multiple Choice
¿Qué son los niveles de energía en el modelo Bohr?
Lugar donde están los protones
Distintas orbitas donde se mueven los electrones
Zona donde se mueven los electrones
Zona más densa del atomo
84
Multiple Choice
Se define como la partícula más pequeña que puede existir de una sustancia simple o elemento químico.
Una molécula
Un átomo
Un cuerpo
85
Multiple Choice
Decía: "Los electrones se distribuyen en orbitales que son regiones donde existe la mayor probabilidad de encontrar a un electrón".
Rutherford
Bohr
De Broglie
Schrodinger
86
Multiple Choice
Hay protones con carga negativa
Verdadero
Falso
87
Multiple Choice
¿Quién ocupó por primera vez el nombre átomo?
Demócrito
Thompson
Dalton
Bohr
88
Multiple Choice
Hay electrones con carga negativa
Verdadero
Falso
89
Multiple Choice
La materia está compuesta por partículas muy pequeñas a las que llamamos
átomos.
moléculas
partículas
90
Multiple Choice
El Principio de Incertidumbre fue propuesto por .... y decía:.....
De Broglie / El electrón se halla en un nivel externo
Bohr/ solo hay emisión y absorción de energía cuando el electrón cambia de orbita
Heisenberg/ Es imposible conocer simultáneamente la posición y la velocidad de un electrón
91
Multiple Choice
El modelo actual del átomo habla de ......... que es una región donde existe ................... de encontrar a un electrón
Órbitas / la certeza
Orbital / la máxima probabilidad
2 números cuánticos/ la certeza
3 números cuánticos/ la menor probabilidad
Show answer
Auto Play
Slide 1 / 91
MULTIPLE CHOICE
Similar Resources on Wayground

80 questions
Geometry Saturday Review
Presentation
•
9th Grade

81 questions
Alg A: Capstone 2, Part 1 Review
Presentation
•
8th - 10th Grade

85 questions
UD 3
Presentation
•
7th Grade

80 questions
Argumentative Writing Outline
Presentation
•
10th Grade

92 questions
Math EOG Review
Presentation
•
8th Grade

87 questions
Ligação covalente -hidrocarbonetos
Presentation
•
10th Grade

86 questions
מקבילית - תכונות - שיעור 2
Presentation
•
9th Grade

89 questions
SAVVAS K Objects Experience 1
Presentation
•
KG
Popular Resources on Wayground

20 questions
"What is the question asking??" Grades 3-5
Quiz
•
1st - 5th Grade

20 questions
“What is the question asking??” Grades 6-8
Quiz
•
6th - 8th Grade

10 questions
Fire Safety Quiz
Quiz
•
12th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

34 questions
STAAR Review 6th - 8th grade Reading Part 1
Quiz
•
6th - 8th Grade

20 questions
“What is the question asking??” English I-II
Quiz
•
9th - 12th Grade

20 questions
Main Idea and Details
Quiz
•
5th Grade

47 questions
8th Grade Reading STAAR Ultimate Review!
Quiz
•
8th Grade