

07x01 Acidi e basi secondo Arrhenius
Presentation
•
Chemistry
•
9th - 12th Grade
•
Hard
Pietro Blu Giandonato
FREE Resource
10 Slides • 18 Questions
1

Acidi e basi secondo Arrhenius
Lezione creata dal prof P. B. Giandonato @profgiando
Immagini credits Zanichelli ed.
2
3
Acidi e basi secondo Arrhenius
In base alla teoria di Arrhenius acido è una sostanza che in acqua libera ioni H+ e base una sostanza che in acqua libera ioni OH-
Per esempio, la dissoluzione dell'acido cloridrico in acqua può essere rappresentata dalla seguente equazione:
Analogamente, la dissoluzione in acqua dell'idrossido di potassio (base) può essere rappresentata dalla seguente equazione:


4
Acidi e basi secondo Arrhenius
Versiamo in un becher una quantità di soluzione di acido HCl, e aggiungiamo alcune gocce di indicatore universale.
II colore rosso segnala che la soluzione è acida, cioè che contiene ioni H+

In un secondo becher versiamo una soluzione di una base, KOH, e aggiungiamo l'indicatore universale. II colore blu indica che la soluzione è basica, cioè che contiene un certo numero di ioni ossidrile OH-

5
Reazione di neutralizzazione
Mescolando una soluzione acida e una basica, provoca una reazione di neutralizzazione, le due sostanze perdono le loro caratteristiche.

Scrivendo al posto delle formule delle sostanze le formule degli ioni presenti in soluzione, la reazione può essere rappresentata da un'equazione in forma ionica:

6
Reazione di neutralizzazione
Eliminando gli ioni che rimangono inalterati (chiamati anche ioni spettatori) la reazione può essere rappresentata da un'equazione in forma ionica semplificata:


Mescolando una soluzione basica e una acida, il colore del sistema diviene verde: è avvenuta una trasformazione chimica, la soluzione non è più né acida né basica e diciamo che è neutra.
7
Reazione di neutralizzazione
In acqua, la reazione di neutralizzazione avviene tra lo ione H+ dell'acido e lo ione OH- della base: questi ioni si combinano e si annullano reciprocamente formando molecole di H2O.

In generale, i prodotti della reazione di neutralizzazione tra un acido e una base in soluzione acquosa sono sempre due: l'acqua e un sale, diverso a seconda dell'acido e della base che hanno reagito.

8
Dropdown
9
Multiple Choice
Quali tra le seguenti sostanze è un acido?
HCl
KOH
H2O
H2
10
Multiple Choice
Quali tra le seguenti sostanze è una base?
HCl
KOH
H2O
H2
11
Multiple Choice
Le sostanze acide in soluzione acquosa liberano:
H+
OH-
H2O
H2
12
Multiple Choice
Le sostanze basiche in soluzione acquosa liberano:
H+
OH-
H2O
H2
13
Multiple Select
Quando sostanze basiche e acide in soluzione acquosa si combinano formano:
H+
OH-
H2O
Sale
14
Dropdown
15
Multiple Choice
Per neutralizzare una soluzione acida, bisogna aggiungere una soluzione
16
Multiple Choice
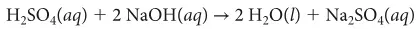
In questa reazione di neutralizzazione qual è il sale?
H2SO4
NaOH
Na2SO4
H2O
17
Multiple Choice
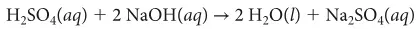
In questa reazione di neutralizzazione qual è l'acido?
H2SO4
NaOH
Na2SO4
H2O
18
Multiple Choice
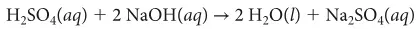
In questa reazione di neutralizzazione qual è la base?
H2SO4
NaOH
Na2SO4
H2O
19
Titolazione acido-base
Le reazioni di neutralizzazione possono essere usate per determinare la quantità di acido o di base presente in una data soluzione.
Per determinare la concentrazione di una soluzione acquosa di acido solforico (H2SO4) si può usare una soluzione basica di idrossido di sodio (NaOH) di cui è nota la concentrazione (soluzione titolante).
In un becher con la soluzione acida si aggiunge un indicatore acido-base. Goccia a goccia si aggiunge una soluzione basica a concentrazione nota finché si avrà il cambio di colore della soluzione, chiamato viraggio dell'indicatore.

20
Titolazione acido-base
Il cambiamento indica che tutto l'acido è stato neutralizzato: tutti gli ioni H+ hanno reagito con altrettanti ioni OH- formando molecole di acqua. In base al volume di soluzione basica si può determinare la concentrazione della soluzione acida.
L'insieme delle procedure sperimentali e dei calcoli per determinare la concentrazione di una soluzione acida (oppure di una soluzione basica) prende il nome di titolazione acido-base.

21
Proticità di un acido
Nella reazione di neutralizzazione tra idrossido di sodio e acido solforico occorrono due moli di NaOH per neutralizzare una mole di H2SO4:

Questo perché ogni molecola di H2SO4 libera due ioni H+ che possono neutralizzare i due ioni OH- di due molecole di NaOH.
L'acido solforico viene chiamato acido biprotico perché libera due protoni H+. Gli acidi che liberano un protone sono chiamati monoprotici, mentre quelli in grado di liberare più protoni sono poliprotici.
22
Multiple Choice
L'acido solforico HCl è un acido
monoprotico
biprotico
poliprotico
megaprotico
23
Multiple Choice
L'acido fosforico H3PO4 è un acido
monoprotico
biprotico
poliprotico
megaprotico
24
Multiple Choice
L'acido fosforico H2SO4 è un acido
monoprotico
biprotico
poliprotico
megaprotico
25
Multiple Choice
L'acido solforico H2S è un acido
monoprotico
biprotico
poliprotico
megaprotico
26
Multiple Choice
L'acido cloridrico HClO3 è un acido
monoprotico
biprotico
poliprotico
megaprotico
27
Multiple Choice
L'acido borico H3BO3 è un acido
monoprotico
biprotico
poliprotico
megaprotico
28
Multiple Choice
L'acido acetico CH3COOH è un acido
monoprotico
biprotico
poliprotico
megaprotico

Acidi e basi secondo Arrhenius
Lezione creata dal prof P. B. Giandonato @profgiando
Immagini credits Zanichelli ed.
Show answer
Auto Play
Slide 1 / 28
SLIDE
Similar Resources on Wayground

19 questions
Entropia
Presentation
•
9th - 12th Grade

20 questions
PESO E MASSA
Presentation
•
9th - 12th Grade

20 questions
05x01 L'economia globale - Parte 1
Presentation
•
9th - 12th Grade

20 questions
La cellula vegetale e la cellula animale
Presentation
•
9th - 12th Grade

19 questions
Prodotto audiovisivo
Presentation
•
9th - 12th Grade

19 questions
La preistoria
Presentation
•
9th - 12th Grade

25 questions
Classificazione di una Rete
Presentation
•
9th - 12th Grade

20 questions
La cellula vegetale e la cellula animale
Presentation
•
10th - 12th Grade
Popular Resources on Wayground

15 questions
Grade 3 Simulation Assessment 1
Quiz
•
3rd Grade

22 questions
HCS Grade 4 Simulation Assessment_1 2526sy
Quiz
•
4th Grade

16 questions
Grade 3 Simulation Assessment 2
Quiz
•
3rd Grade

19 questions
HCS Grade 5 Simulation Assessment_1 2526sy
Quiz
•
5th Grade

17 questions
HCS Grade 4 Simulation Assessment_2 2526sy
Quiz
•
4th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

24 questions
HCS Grade 5 Simulation Assessment_2 2526sy
Quiz
•
5th Grade

20 questions
Math Review
Quiz
•
3rd Grade
Discover more resources for Chemistry

22 questions
Solubility Curve Practice
Quiz
•
10th Grade

10 questions
Exploring Properties and Models of Acids and Bases
Interactive video
•
6th - 10th Grade

19 questions
Review Set 3 - Moles & Chemical Formulas
Presentation
•
10th Grade

20 questions
Types of Chemical Reactions
Quiz
•
9th - 12th Grade

20 questions
Stoichiometry Practice
Quiz
•
10th Grade

10 questions
Identifying Types of Chemical Reactions
Interactive video
•
6th - 10th Grade

20 questions
Redox Reactions
Quiz
•
10th - 12th Grade

20 questions
pH and pOH Calculations
Quiz
•
10th - 11th Grade