

ATIVIDADE DE REVISÃO PARA A PROVA BIMESTRAL
Presentation
•
Chemistry
•
2nd Grade
•
Practice Problem
•
Hard
Fatima Jacqueline Da Silva Barboza Dos Santos
Used 25+ times
FREE Resource
1 Slide • 14 Questions
1
ATIVIDADE DE REVISÃO PARA A PROVA BIMESTRAL
QUÍMICA 2ª EM
PROFESSORA: FATIMA JACQUELINE
HABILIDADES:
(EM13CNT107) Realizar previsões qualitativas e quantitativas sobre o funcionamento de geradores, motores elétricos e seus componentes, bobinas, transformadores, pilhas, baterias e dispositivos eletrônicos, com base na análise dos processos de transformação e condução de energia envolvidos – com ou sem o uso de dispositivos e aplicativos digitais –, para propor ações que visem à sustentabilidade.
(EM13CNT308) Investigar e analisar o funcionamento de equipamentos elétricos e/ou eletrônicos e sistemas de automação para compreender as tecnologias contemporâneas e avaliar seus impactos sociais, culturais e ambientais.
OBJETIVOS: Analisar e realizar previsões qualitativas e quantitativas sobre o funcionamento de pilhas e baterias
2
Multiple Choice

Para determinar a reação global de uma pilha, é necessário saber quais são as semirreações envolvidas no processo.
Aplicando seus conhecimentos sobre os dispositivos, assinale a alternativa que apresenta todas as informações corretas:
A) Ânodo (polo negativo):
Fe→Fe2++2e−Fe→Fe2++2e−
B) Ânodo (polo positivo):
Fe→Fe2++2e−Fe→Fe2++2e−
C) Cátodo C) (polo positivo):
Fe2+→Fe+2e−Fe2+→Fe+2e−
D) Cátodo (polo negativo):
Fe→Fe2++2e−Fe→Fe2++2e−
E) Ânodo (polo negativo):
Fe2+→Fe+2e−Fe2+→Fe+2e−
3
Multiple Select
Muitas vezes, usamos os termos "pilhas" e "baterias" como sinônimos, mas há diferenças entre os dois dispositivos.
Analise as afirmações a seguir e assinale às alternativas relacionadas apenas às pilhas.
São dispositivos eletroquímicos simples, compostos por uma única célula eletroquímica. Elas geralmente não são recarregáveis e são usadas até a energia armazenada se esgotar.
Muitas delas são recarregáveis, como as de íons de lítio, usadas em dispositivos eletrônicos modernos, ou as de chumbo-ácido, empregadas em automóveis.
Geralmente têm menor capacidade de energia e são usadas em dispositivos de baixa potência, como controles remotos, lanternas e brinquedos.
São usadas principalmente em dispositivos portáteis e de baixo consumo energético.
Têm maior capacidade de energia e são usadas em dispositivos que requerem maiores potência e durabilidade, como laptops, smartphones, veículos elétricos e ferramentas elétricas.
4
Multiple Choice

(Espcex (Aman) 2012) Abaixo são fornecidos os resultados das reações entre metais e sais. De acordo com as reações ao lado equacionadas, a ordem decrescente de reatividade dos metais envolvidos em questão é:
Al, Fe e Ag.
Ag, Fe e Al.
Fe, Al e Ag.
Ag, Al e Fe.
Al, Ag e Fe.
5
Fill in the Blanks
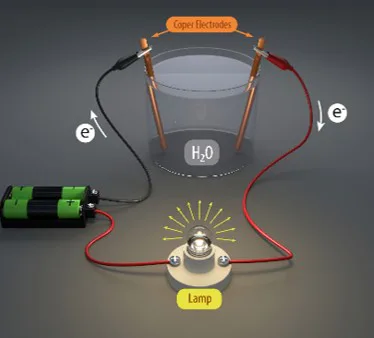
Type answer...
6
Multiple Choice
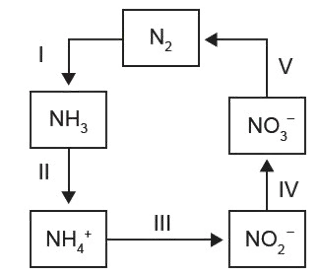
ENEM (2014) A aplicação excessiva de fertilizantes nitrogenados na agricultura pode acarretar alterações no solo e na água pelo acúmulo de compostos nitrogenados, principalmente na forma mais oxidada, favorecendo a proliferação de algas e plantas aquáticas e alterando o ciclo do nitrogênio, representado no esquema. A espécie nitrogenada mais oxidada tem sua quantidade controlada por ação de microrganismos que promovem a reação de redução dessa espécie, em um processo denominado desnitrificação. O processo citado está representado na etapa:
I
II
III
IV
V
7
Multiple Choice
(Ueg 2017) O escurecimento de talheres de prata pode ocorrer devido à presença de derivados de enxofre encontrados nos alimentos. A equação química de oxidação e redução que representa esse processo está descrita a seguir:
SULFETO DE HIDROGÊNIO
OXIGÊNIO GASOSO
SULFETO DE PRATA
PRATA METÁLICA
ÁGUA
8
Multiple Choice
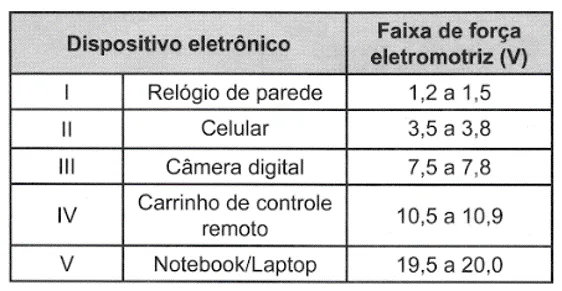
(ENEM 2021) O quadro lista alguns dispositivos eletrônicos que estão presentes no dia a dia, bem como a faixa de força eletromotriz necessária ao seu funcionamento. Considere que uma bateria é construída pela associação em série de três pilhas de lítio-iodo, nas condições-padrão, conforme as semiequações de redução apresentadas.
Essa bateria é adequada para o funcionamento de qual dispositivo eletrônico?
I2 + 2 e- → 2 I- Eº = + 0,54 V
Li+ + e- → Li Eº = - 3,05 V
I
II
III
IV
V
9
Multiple Choice
(Famerp 2024) O arranjo experimental mostrado na imagem ao lado representa uma célula eletroquímica (pilha) usada na obtenção do potencial-padrão de redução (E°) de semirreações, adotando-se E° = 0 V para o eletrodo de hidrogênio. Atribui-se E° positivo para o metal que reduz, diante do H e E° negativos para o metal ou a espécie que oxida.
A substituição do cobre por outro metal (metal M) no arranjo experimental gera um potencial de 0,44 V, e o fluxo de elétrons inverte-se de M para o eletrodo de hidrogênio.
De acordo com as informações, uma pilha formada pelo metal M e pelo metal cobre produz um potencial de:
0,10 V, na qual M é o cátodo.
0,78 V, em que o cobre é o cátodo
0,10 V, em que o cobre é o ânodo
0,10 V, na qual M é o ânodo
0,78 V, na qual M é o cátodo.
10
Fill in the Blanks
Type answer...
11
Multiple Choice
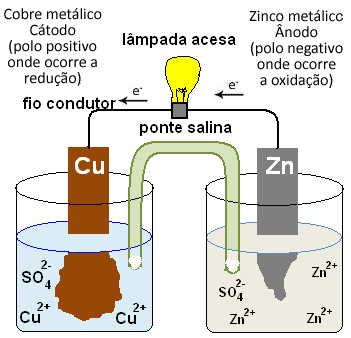
(UniMontes – 2017) A célula de Daniel consiste de eletrodos de zinco e cobre imersos em soluções de cloreto de zinco e cloreto de cobre II, respectivamente, como mostrado na figura abaixo.
É CORRETO afirmar que a ponte salina:
permite a migração dos íons da solução de zinco para a solução
de cobre.
impede a migração dos íons Cl–
para o eletrodo de Zn e para o
eletrodo de Cu.
é necessária quando os dois
eletrodos compartilham um
eletrólito comum.
é essencial para evitar que ambas
as soluções percam sua
neutralidade elétrica.
12
Multiple Choice

(ENEM – 2016) Utensílios de uso cotidiano e ferramentas que contêm ferro em sua liga metálica tendem a sofrer processo corrosivo e enferrujar. A corrosão é um processo eletroquímico e, no caso do ferro, ocorre a precipitação do óxido de ferro (III) hidratado, substância marrom pouco solúvel, conhecida como ferrugem. Esse processo corrosivo é, de maneira geral, representado pela equação química:
4 Fe(s) + 3 O2(g) + 2 H2O(l) → 2 Fe2O3 · H2O(s)
Uma forma de impedir o processo corrosivo nesses utensílios é:
renovar sua superfície, polindo-a semanalmente.
evitar o contato de utensílio com calor, isolando-o termicamente
impermeabilizar a superfície, isolando-a de seu contato com o ar úmido.
esterilizar frequentemente os utensílios, impedindo a proliferação de bactérias.
guardar os utensílios em embalagens, isolando-os do contato com outros objetos.
13
Multiple Choice
(UFU, 2009) A eletrólise é um processo que separa, na cela eletrolítica, os elementos químicos de uma substância, através do uso da eletricidade. Esse processo é um fenômeno físico-químico de reação de oxirredução não espontânea. Uma importante aplicação industrial da eletrólise é a obtenção de sódio metálico, com eletrodos inertes, a partir de cloreto de sódio fundido.
A respeito desse processo industrial, é correto afirmar que, além da obtenção do sódio metálico, também se observa a formação:
de hidróxido de sódio fundido, basificando o meio, e de moléculas de gás cloro e de gás hidrogênio, respectivamente, no ânodo e no cátodo da cela eletrolítica.
tanto de moléculas de gás cloro como de gás hidrogênio, respectivamente, no ânodo e no cátodo da cela eletrolítica.
de moléculas de gás cloro no ânodo da cela eletrolítica.
de moléculas de gás hidrogênio no cátodo da cela eletrolítica
14
Multiple Choice
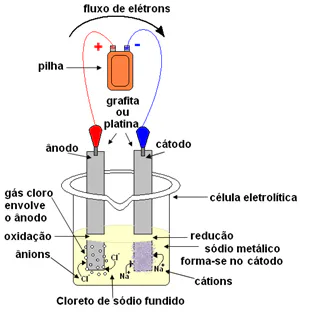
(Enem, 2017) A eletrólise é um processo não espontâneo de grande importância para a indústria química. Uma de suas aplicações é a obtenção do gás cloro e do hidróxido de sódio, a partir de uma solução aquosa de cloreto de sódio. Nesse procedimento, utiliza-se uma célula eletroquímica, como ilustrado: No processo eletrolítico ilustrado, o produto secundário obtido é o:
vapor de água.
oxigênio molecular
hipoclorito de sódio.
hidrogênio molecular.
cloreto de hidrogênio.
15
Fill in the Blanks
Type answer...
ATIVIDADE DE REVISÃO PARA A PROVA BIMESTRAL
QUÍMICA 2ª EM
PROFESSORA: FATIMA JACQUELINE
HABILIDADES:
(EM13CNT107) Realizar previsões qualitativas e quantitativas sobre o funcionamento de geradores, motores elétricos e seus componentes, bobinas, transformadores, pilhas, baterias e dispositivos eletrônicos, com base na análise dos processos de transformação e condução de energia envolvidos – com ou sem o uso de dispositivos e aplicativos digitais –, para propor ações que visem à sustentabilidade.
(EM13CNT308) Investigar e analisar o funcionamento de equipamentos elétricos e/ou eletrônicos e sistemas de automação para compreender as tecnologias contemporâneas e avaliar seus impactos sociais, culturais e ambientais.
OBJETIVOS: Analisar e realizar previsões qualitativas e quantitativas sobre o funcionamento de pilhas e baterias
Show answer
Auto Play
Slide 1 / 15
SLIDE
Similar Resources on Wayground

12 questions
El trabajo
Presentation
•
2nd Grade

14 questions
Probabilidade 2 ano
Presentation
•
2nd Grade

13 questions
Konfigurasi elektron
Presentation
•
2nd Grade

10 questions
TIEMPO Matemáticas
Presentation
•
1st Grade

11 questions
ecuaciones de primer grado
Presentation
•
2nd Grade

10 questions
Manejo de Sustancias Quimicas
Presentation
•
KG

10 questions
ADDITION OF RUPEES AND PAISE (MONEY)
Presentation
•
2nd - 3rd Grade

9 questions
Marie Curie I
Presentation
•
6th Grade
Popular Resources on Wayground

25 questions
The Ultimate College Knowledge Quiz
Quiz
•
8th Grade

20 questions
Math Review
Quiz
•
3rd Grade

15 questions
Fast food
Quiz
•
7th Grade

20 questions
Math Review
Quiz
•
6th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

19 questions
Classifying Quadrilaterals
Quiz
•
3rd Grade

20 questions
Figurative Language Review
Quiz
•
6th Grade
Discover more resources for Chemistry

30 questions
Multiplication Facts 1-12
Quiz
•
2nd - 5th Grade

20 questions
Cartoon Characters!
Quiz
•
KG - 5th Grade

12 questions
Summer Trivia
Quiz
•
1st - 5th Grade

17 questions
Natural Resources
Presentation
•
2nd Grade

39 questions
Arrays and Repeated Addition
Quiz
•
2nd Grade

10 questions
Memorial Day
Quiz
•
2nd - 5th Grade

20 questions
Multiplication facts 1-12
Quiz
•
2nd - 3rd Grade

10 questions
Movie Trivia
Quiz
•
KG - 2nd Grade