

Termokimia
Presentation
•
Chemistry
•
11th Grade
•
Hard
MERY FANGGI
FREE Resource
11 Slides • 7 Questions
1
Termokimia
oleh : Mery o. Fanggi

2
Tujuan Pembelajaran:
Menjelaskan konsep dasar reaksi eksoterm dan endoterm berdasarkan perubahan entalpi
peserta didik dapat menuliskan dan menjelaskan diagram entalpi
3
1. sistem dan lingkungan
Segala sesuatu yang menjadi pusat pengamatan disebut sistem sedangkan segala sesuatu di luar sistem dan dapat mempengaruhi sistem disebut lingkungan.
Berdasarkan perpindahan kalor dan materi, sistem dibedakan menjadi 3 jenis :
Sistem Terbuka : merupakan suatu sistem dimana dapat dimungkinkan terjadinya perpindahan kalor serta materi.
Sistem Tertutup : merupakan suatu sistem dimana dapat dimungkinkan terjadinya perpindahan kalor, tetapi tidak terjadi perpindahan materi.
Sistem Terisolasi : merupakan suatu sistem dimana tidak dimungkinkan terjadinya perpindahan kalor dan materi.
4

5
2. Jenis-jenis Reaksi Berdasarkan Perubahan Energi
Eksoterm : Reaksi perpindahan kalor dari sistem menuju lingkungan

∆H = H akhir – H awal
∆H = kecil – besar
∆H < 0 , atau bertanda negatif ( – )
Ciri reaksi eksoterm ini terjadi pada reaksi yang mengalami kenaikan suhu.
6
Endoterm : Reaksi perpindahan kalor dari lingkungan ke sistem
∆H = H akhir – H awa
∆H = besar – kecil;
∆H > 0 , atau bertanda positif ( + )

Ciri reaksi endoterm ini terjadi pada reaksi yang mengalami penurunan suhu.
7
Persamaan termokimia adalah persamaan reaksi kimia yang diikuti dengan nilai perubahan entalpi.
contoh : 2 H2 (g) + O2 (g) → 2 H2O (g) ΔH = -489,6 kj
Persamaan Termokimia
8
Contoh:
Persamaan reaksi (1) dan (2) termasuk persamaan termokimia karena persamaan reaksinya dilengkapi dengan data perubahan entalpi (ΔH)

9

contoh : pencairan es batu
H2O (s) → H2O (l) ΔH= + 6,01 kj
Diagram tingkat energi
10
contoh : pembekuan air
H2O (l) → H2O (s) ΔH= - 6,01 kj

11
Multiple Choice

Dari gambar tersebut, manakah yang dikatakan mengalami reaksi endoterm?
1 (menyerap/menerima kalor)
2 (melepaskan kalor)
12
Multiple Choice
Reaksi : 2H2 (g) + O2 (g) -------> 2 H2O (l) ΔH = - 572 kJ
Persamaan reaksi diatas berarti....
Reaksi pembentukan 1 mol air diperlukan kalor 286 kJ
Reaksi pembentukan 2 mol air diperlukan kalor 286 kJ
Reaksi pembakaran 1 mol hidrogen dilepaskan kalor 572 kJ
Reaksi pembentukan uap air adalah -286 kJ
Reaksi pembentukan 2 mol air dilepaskan kalor 572 kJ
13
Multiple Choice
Diketahui persamaan termokimia berikut.
N2(g) + 3H2(g) ----> 2NH3(g) ∆H = -92,4 kJ
Perubahan entalpi untuk reaksi :
NH3(g) -----> 1/2N2(g) + 3/2H2(g) adalah .... kJ
+92,4 kJ
+46,2 kJ
-46,2 kJ
-92,4 kJ
-184,8 kJ
14
Multiple Choice
Diketahui persamaan termokimia
C6H6(g) ------> 6C(s) + 3H2(g) ∆H = - 49 kJ
Pernyataan berikut dari reaksi diatas adalah ....
Pembentukan 1 mol benzena (C6H6) memerlukan kalor sebesar 8,16 kJ
Pembentukan 1 mol benzena (C6H6) memerlukan kalor sebesar 49 kJ
Pembentukan 1 mol benzena (C6H6) membebaskan kalor sebesar 49 kJ
Perurian 1 mol benzena (C6H6) memerlukan kalor sebesar 49 kJ
Peruraian 1 mol benzena (C6H6) membebaskan kalor sebesar 49 kJ
15
Multiple Choice

Diketahui diagram energy suatu reaksi sebagai berikut:
Berdasarkan diagram tersebut, dapat disimpulkan bahwa . .
Reaksi bersifat endoterm
Entalpi pereaksi lebih kecil daripada entalpi hasil reaksi
Terjadi pelepasan kalor dari system ke lingkungan
Contoh reaksi tersebut adalah rekasi fotosintesis
Reaksi berlangsung pada suhu tetap.
16
Multiple Choice

Perhatikan gambar berikut ini !
Reaksi tersebut termasuk ke dalam reaksi ....
eksoterm, karena H pereaksi < H hasil reaksi, ΔH = -
endoterm, karena H pereaksi < H hasil reaksi, ΔH = +
eksoterm, karena H pereaksi > H hasil reaksi, ΔH = +
endoterm, karena H pereaksi > H hasil reaksi, ΔH = -
endoterm, karena H pereaksi = H hasil reaksi, ΔH = +
17
Multiple Choice
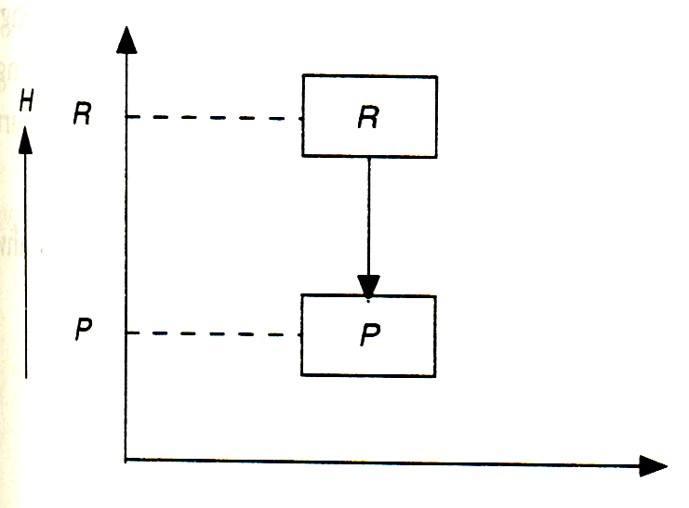
Diagram berikut adalah diagram dari reaksi….
Entalpi
Endoterm
Eksoterm
Sistem
Lingkungan
18

Termokimia
oleh : Mery o. Fanggi

Show answer
Auto Play
Slide 1 / 18
SLIDE
Popular Resources on Wayground

10 questions
5.P.1.3 Distance/Time Graphs
Quiz
•
5th Grade

10 questions
Fire Drill
Quiz
•
2nd - 5th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

22 questions
School Wide Vocab Group 1 Master
Quiz
•
6th - 8th Grade

20 questions
Main Idea and Details
Quiz
•
5th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

12 questions
What makes Nebraska's government unique?
Quiz
•
4th - 5th Grade
Discover more resources for Chemistry

15 questions
Ionic Compounds: Naming and Formula Writing
Quiz
•
9th - 12th Grade

10 questions
Exploring the Ideal Gas Law and Its Applications
Interactive video
•
9th - 12th Grade

15 questions
Balancing Chemical Equations
Quiz
•
10th - 12th Grade

6 questions
Single Replacement Reaction Lesson
Presentation
•
9th - 12th Grade

14 questions
Temp & Pressure Conversions & Daltons Law
Quiz
•
10th - 11th Grade

10 questions
Exploring Saturated, Unsaturated, and Supersaturated Solutions
Interactive video
•
9th - 12th Grade

42 questions
Practice Regents #1 (126)
Quiz
•
11th Grade

10 questions
One Step Molar Conversions
Quiz
•
9th - 12th Grade