

Le leggi dei gas
Presentation
•
Chemistry
•
9th - 12th Grade
•
Practice Problem
•
Easy
Pietro Blu Giandonato
Used 2+ times
FREE Resource
35 Slides • 25 Questions
1

2

3

4
5

6

7

8

9
Multiple Choice
Pressione, volume e temperatura di un gas vengono definite variabili...
di controllo
di misura
di stato
indipendenti
10
Drag and Drop
11
Drag and Drop
12
Multiple Choice
Quali sono le variabili di stato che caratterizzano lo stato di un gas?
Volume, pressione e temperatura
Volume, densità e massa
Pressione, densità e temperatura
Volume, massa e temperatura
13
Multiple Choice
Qual è l'unità di misura della temperatura nel SI?
14
Multiple Choice
Qual è l'unità di misura della pressione nel SI?
15
Legge di Boyle
(isoterma)

La legge isoterma (o legge di Boyle) stabilisce che, a temperatura costante, per una determinata quantità di gas, il volume è inversamente proporzionale alla pressione: p . V = k
16
17

18

19
Multiple Choice
Se la temperatura rimane costante, come varia il volume di un gas quando la pressione aumenta?
Il volume aumenta
Il volume diminuisce
Il volume rimane costante
Il volume si azzera
20
Multiple Choice
Qual è la relazione tra pressione e volume secondo la legge isoterma di Boyle?
Il volume è direttamente proporzionale alla pressione.
Il volume è inversamente proporzionale alla pressione.
Il volume è indipendente dalla pressione.
Il volume è proporzionale al quadrato della pressione.
21
Multiple Choice
Come cambia la curva isoterma nei grafici della pressione rispetto al volume quando la temperatura aumenta?
La curva si avvicina all'origine degli assi.
La curva si allontana dall'origine degli assi.
La curva rimane invariata.
La curva diventa una retta.
22

23

24
Open Ended
Spiega in che modo si applica la legge di Boyle alla respirazione polmonare
25

26
Multiple Select
Quali affermazioni sono corrette riguardo al modello particellare dei gas e la legge di Boyle?
Comprimendo un gas, il suo volume aumenta.
A temperatura costante, la pressione aumenta se il volume diminuisce.
Le particelle del gas urtano più frequentemente le pareti se il volume diminuisce.
La pressione diminuisce se il volume diminuisce.
27

La legge isobara (o legge di Charles) stabilisce che a pressione costante, per una determinata quantità di gas, il volume è direttamente proporzionale alla temperatura assoluta: V/T = k
Legge di Charles
(isobara)
28
29

30

31
Drag and Drop
32
Multiple Choice
Quale affermazione è corretta riguardo la legge di Charles?
33

34
Open Ended

Spiega come la legge di Charles si manifesta nell'esperimento con i palloncini immersi in azoto liquido e successivamente riportati a temperatura ambiente.
35

La legge isocora (o legge di Gay-Lussac) stabilisce che, a volume costante, per una determinata quantità di gas, la pressione è direttamente proporzionale alla temperatura assoluta: p/T = k
Legge isocora
di Gay-Lussac
36
37

38
Drag and Drop
39

40

A bassa pressione o a elevate temperature il comportamento di un gas reale si può considerare simile a quello di un gas ideale
La legge dei
gas ideali
41

42

43
Multiple Select
In quali delle leggi dei gas la proporzionalità è diretta?
Legge isoterma
(di Boyle)
Legge isocora
(di Gay-Lussac)
Legge isobara
(di Charles)
Legge dei gas perfetti
44
Multiple Choice
In quali delle leggi dei gas la proporzionalità è inversa?
Legge isoterma
(di Boyle)
Legge isocora
(di Gay-Lussac)
Legge isobara
(di Charles)
Legge dei gas perfetti
45
Multiple Choice
Quale delle seguenti equazioni rappresenta la legge combinata dei gas ideali?
p·V = k
V/T = k
p/T = k
p·V/T = k
46

47

48

49
Drag and Drop
50
Multiple Choice
A bassa pressione, perché il comportamento di un gas reale si avvicina a quello di un gas ideale?
Perché le particelle sono molto distanti e non ci sono forze attrattive o repulsive
Perché le particelle sono molto vicine e si attraggono
Perché la temperatura è molto bassa
Perché il volume delle particelle è rilevante
51
Multiple Choice
A alta temperatura, perché il comportamento di un gas reale si avvicina a quello di un gas ideale?
Perché la temperatura influisce sul volume.
52

53

54
Multiple Choice
Se si ha una miscela di elio e cloro in un recipiente, come si calcola la pressione totale esercitata dalla miscela?
Si sommano le pressioni parziali dei singoli gas
Si moltiplicano le pressioni parziali dei singoli gas
Si prende la pressione del gas più abbondante
Si divide la pressione totale per il numero di gas
55
Drag and Drop
56

57

58

59
Open Ended
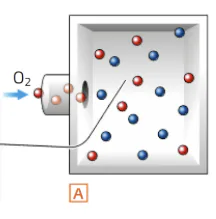
Spiega in cosa consiste il fenomeno della diffusione di un gas
60
Open Ended

Spiega in cosa consiste il fenomeno della effusione di un gas

Show answer
Auto Play
Slide 1 / 60
SLIDE
Similar Resources on Wayground

54 questions
Latin/Greek Roots: Lime Set
Presentation
•
9th - 12th Grade

57 questions
Les Adjectifs Possessifs
Presentation
•
9th - 12th Grade

56 questions
BL Ch 10 Gasses ppt
Presentation
•
9th - 12th Grade

53 questions
Minerals
Presentation
•
9th - 12th Grade

51 questions
Chemistry 1-4: Electrons in Atoms
Presentation
•
10th - 12th Grade

52 questions
Ambiguity, Paradox, Understatement, Overstatement
Presentation
•
9th - 12th Grade

55 questions
Would you rather...
Presentation
•
9th - 12th Grade

53 questions
12.5 Permutations and Combinations
Presentation
•
9th - 12th Grade
Popular Resources on Wayground

20 questions
STAAR Review Quiz #3
Quiz
•
8th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

6 questions
Marshmallow Farm Quiz
Quiz
•
2nd - 5th Grade

20 questions
Main Idea and Details
Quiz
•
5th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

19 questions
Classifying Quadrilaterals
Quiz
•
3rd Grade

12 questions
What makes Nebraska's government unique?
Quiz
•
4th - 5th Grade