

02x01 - Forma e polarità delle molecole
Presentation
•
Chemistry
•
10th Grade
•
Practice Problem
•
Hard
Pietro Blu Giandonato
Used 8+ times
FREE Resource
10 Slides • 11 Questions
1
Forma e polarità delle molecole
Un'analisi delle caratteristiche delle sostanze polari e apolari, con un focus sulle loro proprietà chimiche e fisiche. Scopri come queste differenze influenzano il comportamento delle sostanze in vari contesti.
2
La polarità di una molecola dipende, oltre che dalla presenza di legami covalenti eteropolari, anche dalla sua forma.
Le molecole polari hanno un dipolo permanente, ovvero una parte carica positivamente e una negativamente.
Polarità delle molecole

3
Nella molecola dell'acqua l'ossigeno ha una elettronegatività pari a 3,16 mentre l'idrogeno 2,2 la differenza è 0,96 a favore dell'ossigeno, che sposta su di sé gli elettroni di legame con gli idrogeni. La molecola ha una forma piegata, è asimmetrica dunque è un dipolo elettrico, polare.
Polarità delle molecole


4
Anche nella molecola della CO2 l'ossigeno ha una elettronegatività pari a 3,16 mentre il carbonio 2,55 la differenza è 0,61 a favore dell'ossigeno, che sposta su di sé gli elettroni di legame con il carbonio. Ma la molecola della CO2 poiché è lineare e simmetrica non è un dipolo, è apolare.
Polarità delle molecole



5
Regole generali per prevedere la polarità delle molecole:
molecole biatomiche con legami covalenti polari sono sempre polari, es. CO
molecole pluriatomiche con legami coval. polari sono apolari se l’atomo centrale non ha doppietti elettronici liberi e gli atomi legati sono identici, es. CO2 e CCl4
molecole pluriatomiche con legami covalenti polari sono polari se l’atomo centrale non ha doppietti elettronici liberi e gli atomi legati sono diversi, es. CHCl3
mol. pluriatom. con legami cov. polari sono polari se l’atomo centrale ha doppietti elettronici liberi, es. H2O, NH3
Polarità delle molecole

6
Le molecole apolari si legano con difficoltà e con poca forza e si trovano in natura come particelle isolate allo stato gassoso.
Ad esempio anidride carbonica (CO2), metano (CH4).
Le molecole polari sono soggette a legarsi fortemente tra loro e con altre molecole o ioni attraverso legami ioni-dipolo, legami idrogeno e interazioni di Van der Waals e si trovano in natura in uno stato condensato.
Ad esempio l'acqua (H2O) è liquida temperatura ambiente.
Polarità delle molecole
7
Anche la miscibilità e la solubilità delle sostanze sono influenzate dalla polarità delle loro molecole.
Le sostanze polari si sciolgono in quelle polari, le sostanze apolari si sciolgono nelle apolari: il simile scioglie il simile.
Polarità delle molecole



L'olio, sostanza apolare, non si miscela con l'acqua, sostanza polare.
8
Nelle molecole più grandi, alcuni atomi possono conferire ad esse una parziale polarità, come nel caso degli alcoli e degli zuccheri, che possiedono gruppi O-H polari. Alcool e zucchero infatti sono solubili in solventi polari come l'acqua.
Polarità delle molecole


9
Molecole biatomiche


10
Molecole tetraedriche


11
Multiple Select
Quali tra queste sostanze sono apolari?
Acqua
Olio
Zucchero
Sale da cucina
12
Multiple Select
Quali tra queste sostanze sono polari?
Acqua
Olio
Zucchero
Sale da cucina
13
Multiple Select
Quali tra queste sostanze sono miscibili in acqua?
Olio
Zucchero
Sale da cucina
14
Multiple Select
La polarità delle molecole dipende da:
differenza di elettronegatività
differenza di n. di ossidazione
forma delle molecole
tipo di atomi
15
Multiple Select
Quali forme possono avere le molecole polari?
lineare
piegata
tetraedrica
piramidale trigonale
16
Multiple Choice
Una molecola non polare è sempre costituita da legami covalenti non polari.
17
Multiple Select
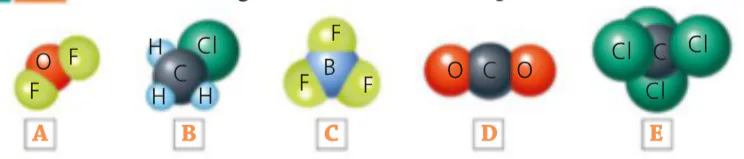
Quali tra queste sono molecole polari?
A
B
C
D
E
18
Multiple Choice
Le molecole biatomiche formate da atomi uguali sono sicuramente apolari
19
Multiple Choice
Le molecole biatomiche formate da atomi diversi sono sicuramente polari
20
Multiple Choice
Le molecole poliatomiche formate da atomi che hanno diversa elettronegatività sono sicuramente polari
21
Multiple Choice
Le molecole tetraedriche sono sicuramente apolari
Forma e polarità delle molecole
Un'analisi delle caratteristiche delle sostanze polari e apolari, con un focus sulle loro proprietà chimiche e fisiche. Scopri come queste differenze influenzano il comportamento delle sostanze in vari contesti.
Show answer
Auto Play
Slide 1 / 21
SLIDE
Similar Resources on Wayground

14 questions
In preparazione alla verifica di latino
Presentation
•
11th Grade

21 questions
participio futuro e perifrastica attiva
Presentation
•
10th Grade

14 questions
GESTIONE DELLA SICUREZZA A BORDO V F LOG
Presentation
•
5th Grade

14 questions
La letteratura religiosa delle origini - 3B CAT
Presentation
•
10th Grade

19 questions
L’economia circolare
Presentation
•
10th Grade

20 questions
Parabola nel piano cartesiano per liceo
Presentation
•
10th Grade

16 questions
La civiltà micenea: un viaggio nel passato
Presentation
•
9th Grade

15 questions
Il fenomeno dei Beatles
Presentation
•
11th Grade
Popular Resources on Wayground

20 questions
"What is the question asking??" Grades 3-5
Quiz
•
1st - 5th Grade

20 questions
“What is the question asking??” Grades 6-8
Quiz
•
6th - 8th Grade

10 questions
Fire Safety Quiz
Quiz
•
12th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

34 questions
STAAR Review 6th - 8th grade Reading Part 1
Quiz
•
6th - 8th Grade

20 questions
“What is the question asking??” English I-II
Quiz
•
9th - 12th Grade

20 questions
Main Idea and Details
Quiz
•
5th Grade

47 questions
8th Grade Reading STAAR Ultimate Review!
Quiz
•
8th Grade
Discover more resources for Chemistry

15 questions
Balancing and Reaction Types
Quiz
•
10th Grade

22 questions
Solubility Curve Practice
Quiz
•
10th Grade

16 questions
STAAR Review Quizziz 5
Quiz
•
10th Grade

20 questions
Types of Chemical Reactions
Quiz
•
9th - 12th Grade

5 questions
DOL REC: pH and pOH Calculations
Quiz
•
10th - 11th Grade

20 questions
Naming & Writing Chemical Formulas
Quiz
•
10th Grade

5 questions
DOL PreAP: pH and pOH Calculations
Quiz
•
10th Grade

13 questions
IP PREAP: pH and pOH Calculations
Quiz
•
10th - 11th Grade