

Números cuánticos
Presentation
•
Chemistry
•
1st Grade
•
Hard
Lynn Zambrano
Used 14+ times
FREE Resource
12 Slides • 0 Questions
1
Números cuánticos
Propósito : el propósito de la sesión es que identifiques los 4 número cuánticos dentro de un orbital.

2
3
Números cuánticos.
Los números cuánticos son parámetros que describen el estado energético de un electrón y las características de un orbital.
4

5
1.Número cuántico principal (n)
El nivel
de energía principal que ocupa el electrón. Por ejemplo:§ Si : n = 2 ; entonces el electrón ocupa el nivel 2
§ Si : n = 5 ; entonces el electrón ocupa el nivel 5
A a mayor valor de “n” , mayor es tamaño del orbital.
Valores Permitidos:
El número cuántico principal toma valores enteros positivos, sin considerar el cero.
n = 1 ; 2 ; 3 ; 4 ; 5 ……… ∞

6
2. Número Cuántico Secundario (l)
También es denominado número cuántico azimutal o del momento angular.
Para el electrón determina el subnivel de energía donde este debe encontrarse dentro de un nivel “n”.
Además define la forma geométrica del orbital o nube electrónica.
Para cada nivel de energía se cumple que “l” puede tomar valores enteros desde cero hasta (n-1)
l = 0 ; 1 ; 2 ; 3 ; … (n-1)

7

8
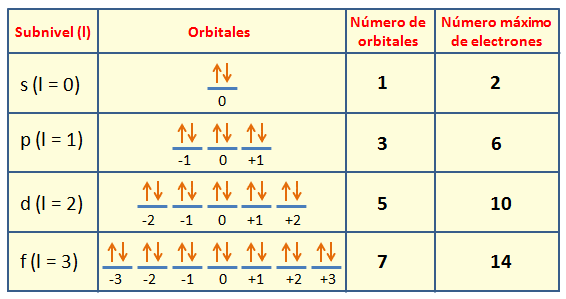
3. Número cuántico magnético (ml)
Para el electrón, indica el orbital donde se encuentra dentro de un determinado subnivel de energía. En cada subnivel (l), “m” puede tomar
valores permitidos : 0 , +/- 1 , +/- 2 , +/- 3 , …. +/- l
§ El subnivel “s”, toma valor de 0
§ El subnivel “p”, toma un valor de -1,0,1
§ El subnivel “d”, toma un valor de -2,-1,0,1,2
§ El subnivel “f”, toma un valor de -3,-2,-1,0,1,2,3

9
10
11
4. Número cuántico Spin Magnético (ms)
indica el sentido de rotación del electrón
alrededor de su propio eje. Sus valores permitidos son: ms = +1/2 y -1/2
Cuando un electrón gira o rota genera un pequeño campo magnético, es decir actúa como un pequeño microimán. En base a esta cualidad del electrón en el sistema atómico y molecular, se logra explicar las propiedades magnéticas de una sustancia química.

12

Números cuánticos
Propósito : el propósito de la sesión es que identifiques los 4 número cuánticos dentro de un orbital.

Show answer
Auto Play
Slide 1 / 12
SLIDE
Similar Resources on Wayground

7 questions
Química I
Presentation
•
1st Grade

10 questions
Disney
Presentation
•
1st - 2nd Grade

8 questions
Fenotipos vemos, genotipos no sabemos
Presentation
•
1st - 2nd Grade

9 questions
DESAFIO_PROVAPR_2_EM_MAT_005
Presentation
•
2nd Grade

9 questions
Justicia 2. La igualdad
Presentation
•
KG

8 questions
Radioatividade
Presentation
•
1st Grade

8 questions
ÓXIDOS
Presentation
•
1st Grade

9 questions
¿De que esta hecha la materia?
Presentation
•
1st Grade
Popular Resources on Wayground

20 questions
Math Review
Quiz
•
3rd Grade

15 questions
Fast food
Quiz
•
7th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

19 questions
Classifying Quadrilaterals
Quiz
•
3rd Grade

20 questions
Figurative Language Review
Quiz
•
6th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

10 questions
Identify Fractions, Mixed Numbers & Improper Fractions
Quiz
•
3rd - 4th Grade
Discover more resources for Chemistry

20 questions
Telling Time to the Hour and Half hour
Quiz
•
1st Grade

20 questions
Cartoon Characters!
Quiz
•
KG - 5th Grade

12 questions
Summer Trivia
Quiz
•
1st - 5th Grade

15 questions
Place Value tens and ones
Quiz
•
1st Grade

10 questions
Movie Trivia
Quiz
•
KG - 2nd Grade

15 questions
Memorial Day Trivia
Quiz
•
KG - 12th Grade

12 questions
Name that Candy
Quiz
•
KG - 12th Grade

26 questions
End of Year Math Review
Quiz
•
1st - 2nd Grade