

ESTRUCTURA DE LEWIS
Presentation
•
Chemistry
•
10th - 11th Grade
•
Practice Problem
•
Medium
Paula Pinto
Used 121+ times
FREE Resource
11 Slides • 10 Questions
1
ESTRUCTURA DE LEWIS
SESION 1 -GUIA 3

2
META DE COMPRENSIÓN
El estudiante comprenderá que los compuestos se originan por la asociación de átomos a través de la formación de enlaces químicos y como los enlaces químicos se pueden clasificar en iónicos y covalentes en cuya formación intervienen fuerzas estabilizadoras.
3
Open Ended
Realizar la configuración electrónica de Z= 8 y determina cuantos electrones tiene en el ultimo nivel de energía
4
ELECTRONES DE VALENCIA
Son los e- que ocupan el nivel cuántico principal (n; cada uno de los renglones en la tabla periódica) más externo del átomo
Los e- de valencia son importantes en química porque participan en la formación de enlaces.

5
Multiple Choice
Cuantos electrones de valencia tiene Berilio Z= 4,teniendo en cuenta su configuración electrónica 1s2 2s2
4 e-
3 e-
2 e-
1 e-
6
Open Ended

Para el siguiente átomo Li+1
Cual es la configuración electrónica correspondiente si sabemos que su numero atómico es 3
7
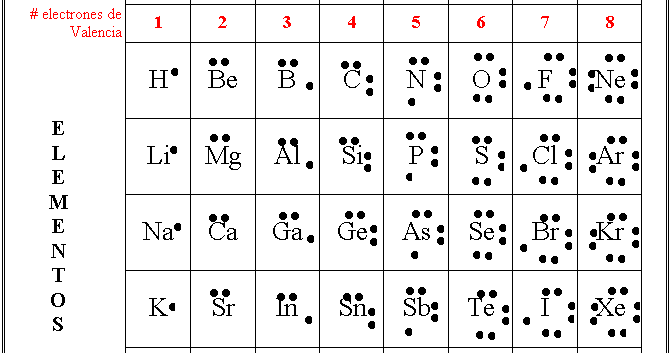
ESTRUCTURA DE LEWIS
Es una representación gráfica que se emplea para indicar el número de electrones que posee cada elemento en su último nivel energético, tales se conocen como electrones de valencia, en dicha representación se emplean puntos para ejemplificar los electrones
8
Multiple Choice
De acuerdo a la siguiente configuración electrónica
1s2 2s2 2p6 3s2
La estructura de Lewis corresponde a:
9
Multiple Choice

De acuerdo a la estructura de Lewis para Z= 53, cual seria la configuración electrónica correcta
1s2 2s2 2p6 3s2 3p6 4s2
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p5
1s2 2s2 2p6 3s2
10

11
Open Ended
Completar la frase
Hoy aprendí que ___________________ y lo considero para :
12
REGLA DEL OCTETO
SESION 2 -GUIA 3
13
Open Ended

¿Cómo es posible que haya interacción entre el Magnesio y Flúor?
14
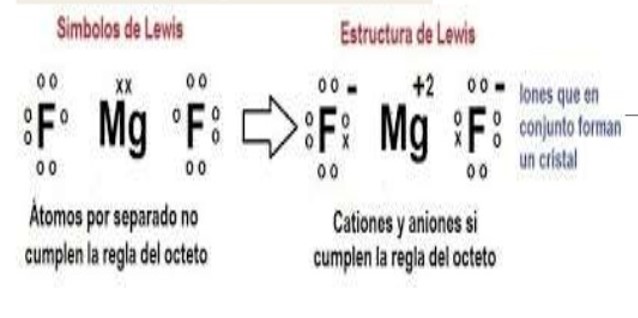
Interacción entre 2 átomos
F-->Z= 9 --> 1s2 2s2 2p5 = 7 electrones de valencia
Mg --> Z= 12 --> 1s2 2s2 2p6 3s2 = 2 electrones de valencia
15
REGLA DEL OCTETO
Lewis postuló en 1916 la regla del octeto, por la que se establece que la tendencia de los iones de los elementos es completar sus últimos niveles de energía con una cantidad de 8 electrones.

16
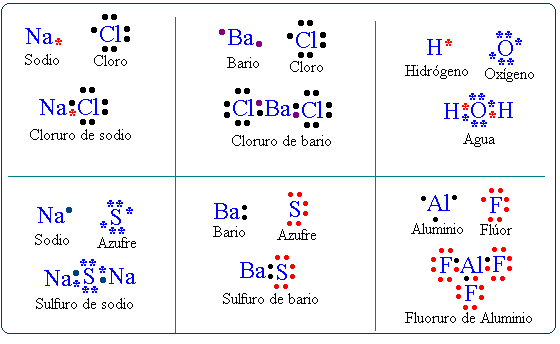
REGLA DEL OCTETO
Indica que dos átomos iguales, al enlazarse, desarrollan una organización específica. Al constituirse el enlace por la compartición de los pares de electrones, cada átomo adquiere la estructura del gas noble mas cercano. Así, ambos átomos se encontrarán rodeados de ocho electrones en su última capa energética.
17
Multiple Select
Si tenemos los siguientes elementos y de acuerdo a su configuración electrónica determinamos sus electrones de valencia
S = 6 electrones de valencia
Mg = 2 electrones de valencia
Cl= 7 electrones de valencia
F= 7 electrones de valencia
K = 1 electrón de valencia
Na= 1 electrón de valencia
Cuales son las posibles combinaciones para cumplir con la regla del octeto
Mg+2K+1
Mg+2S-2
K+1Na+1
Na+1Cl-1
18
CONSTRUCCION ESTRUCTURA LEWIS
Realizar el diagrama de Lewis para MgCl2
1. Realizar la configuración electrónica de cada elemento
2. Determinar los electrones de valencia en total del compuesto

19
3. Definir el átomo central que debe ser el átomo menos electronegativo, excepto el H
4. Dibuja el enlace entre los átomos, por cada enlace son 2 e-
5. Toma los electrones de valencia totales (16) y resta lo que ya coloco (4)
6. Pinta los electrones que faltan de acuerdo a los electrones de valencia de cada elemento

20
Multiple Choice
Cual es la estructura de Lewis para la interacción entre Mg y I --> (MgI2)
Mg= 2 e- valencia
I= 7 e- valencia
21
Open Ended
¿Teniendo en cuenta los electrones de valencia cómo permiten que haya estabilidad en una molécula?
ESTRUCTURA DE LEWIS
SESION 1 -GUIA 3

Show answer
Auto Play
Slide 1 / 21
SLIDE
Similar Resources on Wayground

15 questions
diagnostico
Presentation
•
10th Grade

16 questions
Reacciones Químicas
Presentation
•
10th Grade

16 questions
Función Hidróxido o Base
Presentation
•
10th Grade

15 questions
Repaso de Enlace Químico, Lewis y geometría molecular
Presentation
•
11th Grade

16 questions
Electron Configurations 2021
Presentation
•
10th - 12th Grade

16 questions
Revisão - Características Atômicas
Presentation
•
KG

20 questions
Soluciones Químicas
Presentation
•
11th Grade

17 questions
Preterite tense of -er & -ir verbs
Presentation
•
10th - 12th Grade
Popular Resources on Wayground

20 questions
Math Review
Quiz
•
3rd Grade

15 questions
Fast food
Quiz
•
7th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

19 questions
Classifying Quadrilaterals
Quiz
•
3rd Grade

20 questions
Figurative Language Review
Quiz
•
6th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

10 questions
Identify Fractions, Mixed Numbers & Improper Fractions
Quiz
•
3rd - 4th Grade