

UNIDADES DE CONCENTRACION QUIMICA
Presentation
•
Chemistry
•
11th Grade
•
Practice Problem
•
Easy
Paula Pinto
Used 36+ times
FREE Resource
17 Slides • 6 Questions
1
UNIDADES DE CONCENTRACION QUIMICA

2
META DE COMPRENSION
El estudiante comprenderá que la solubilidad de una disolución depende de factores como la temperatura, la presión y la naturaleza de las sustancias.
3
Open Ended
¿Cuáles son los factores que afectan la solubilidad ?
4
TIPOS DE DISOLUCIONES
Soluciones diluidas: La cantidad de soluto se encuentra en una mínima proporción en relación al volumen de la solución.
Soluciones concentradas: La cantidad de soluto en un volumen determinado es considerable.

5
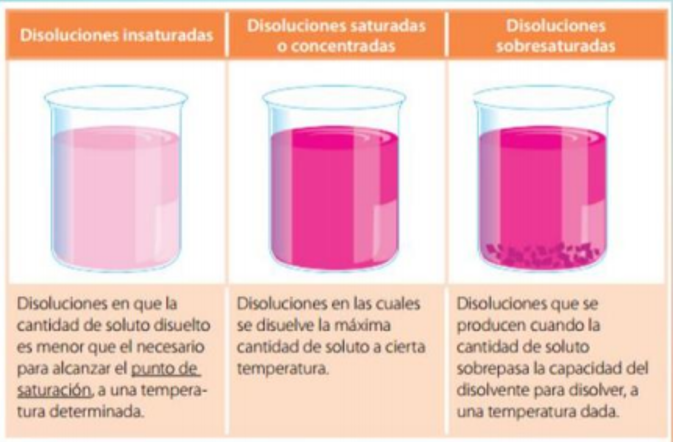
Soluciones insaturadas: El soluto no alcanza la cantidad máxima posible.
Soluciones saturadas: Se ha alcanzado la mayor cantidad de soluto posible para diluir.
Soluciones sobresaturadas: Contiene más soluto del que puede existir para ser diluido.
6
Unidades de concentración
Gran parte de las propiedades de las disoluciones dependen de las cantidades relativas del soluto y del disolvente, es decir, de su concentración. De manera general, para expresar cuantitativamente la concentración de una disolución se puede establecer la proporción en la que se encuentra la cantidad de soluto y del solvente o la cantidad de solución.
7
Unidades de concentracion quimicas
Molaridad o concentración molar (M) :es el número de moles de soluto por litro de solución, lo cual se puede calcular utilizando la siguiente ecuación:

8
Ejercicio
Calcular la molaridad de una disolución de 250 ml en la que está disueltos 30 gramos de cloruro sódico (NaCl).
Datos: pesos atómicos Na=23, Cl=35,45.
9
PASO A PASO
1. Determinar el peso molecular del soluto NaCl
Na = 23 g
Cl = 35,4g
NaCl= 23g + 35,4 g = 58,4 g
2. Realizar la conversión de gramos a moles
30g NaCl x 58,4 g NaCl1 mol NaCl=0,513 moles
10
3. Realizar la conversión de volumen de la disolución de ml a L 250 ml x1000ml1L=0,25L
4. Aplicar la formula correspondiente a la Molaridad
M =L disolucionmoles de soluto M= 0,25 L 0,513 moles NaCl=2,052 Lmol
11
Open Ended
Determinar la concentración molar o molaridad de una disolución de 2 L , en la que están disueltos 12g de KNO3
K: 39 g
N: 14g
O: 16 g
12
UNIDADES DE CONCENTRACION QUIMICAS
META DE LA SESION: Determinar la concentración en las disoluciones y su utilidad
13
Open Ended

Responder a partir de la imagen ¿Qué veo ? ¿Qué pienso? ¿Qué me pregunto?
14
Concentración
Cantidad de soluto disuelta en una cantidad dada de disolvente o de solución. Entre mayor sea la cantidad de soluto disuelta más concentrada estará la solución.
15
MOLALIDAD (m)
La Molalidad (m) o Concentración Molal es el número de moles de soluto que están disueltos en kilogramo de disolvente.

16
Ejercicio
Calcule la molalidad de una disolución de ácido sulfúrico que contiene 24.4 g de ácido sulfúrico H2SO4 en 198 g de agua. La masa molar del ácido sulfúrico es de 98.09 g.
17
PASO A PASO
1. Realizar la conversión de gramos a moles
24,4 g H2SO4 X98 g H2SO41mol H2SO4=0,248 moles H2SO4
2.Realizar la conversión de g del solvente a Kg
198 g H2O X1000 g1 Kg= 0.198 Kg
18
3. Aplicar la formula de la molalidad
m =Kg solvente moles soluto m=0,198 Kg H2O 0,248 moles H2SO4= 1,26 m
19
Multiple Choice
El análisis de un jugo de naranja indico que contenía 85 g de acido cítrico (C3H8O7), por cada vaso que equivale a 250 g de la solución .
Calcula la molalidad del acido cítrico en el jugo si su masa molar es 192 g
0,442 moles /l
0,25 Kg
1,76 moles /Kg
1,76 M
20
Fracción molar
Es la relación entre el numero de moles de un componente y el numero de moles totales de la solución
La suma de las fracciones molares de una solución es igual a uno

21

22
Open Ended

25g Cafeína(C8H10N4O2 )
40g H2O
¿Para determinar la fracción molar de la cafeína en el café que debemos hacer ?
23
Open Ended
Completar la frase
Las unidades de concentración nos sirven para : ___________________
UNIDADES DE CONCENTRACION QUIMICA

Show answer
Auto Play
Slide 1 / 23
SLIDE
Similar Resources on Wayground

18 questions
Gilded Age: Capital and Labor
Presentation
•
11th Grade

20 questions
POLINOMIAL (MAT MINAT KELAS XI)
Presentation
•
11th Grade

20 questions
Propiedades periódicas y formación de iones
Presentation
•
11th Grade

18 questions
GUIA 6 - HIDROCARBUROS
Presentation
•
11th Grade

16 questions
Mole Conversions & Percent Composition Practice
Presentation
•
10th - 12th Grade

17 questions
Konstanta Kesetimbangan
Presentation
•
11th Grade

20 questions
Stoichiometry, Mole Ratio Bellringer
Presentation
•
10th Grade
Popular Resources on Wayground

10 questions
Factors 4th grade
Quiz
•
4th Grade

10 questions
Cinco de Mayo Trivia Questions
Interactive video
•
3rd - 5th Grade

13 questions
Cinco de mayo
Interactive video
•
6th - 8th Grade

20 questions
Math Review
Quiz
•
3rd Grade

20 questions
Main Idea and Details
Quiz
•
5th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

19 questions
Classifying Quadrilaterals
Quiz
•
3rd Grade
Discover more resources for Chemistry

20 questions
Types of Chemical Reactions
Quiz
•
9th - 12th Grade

25 questions
Enthalpy - endo/exo and PED
Quiz
•
11th - 12th Grade

17 questions
Types of Chemical Reaction
Presentation
•
7th - 12th Grade

120 questions
Chemistry Final Review
Quiz
•
9th - 12th Grade

47 questions
Q1 Chem Review
Quiz
•
10th - 12th Grade

10 questions
Stoichiometry Mole to Mole
Quiz
•
10th - 11th Grade

15 questions
Half-Life
Quiz
•
9th - 12th Grade

15 questions
Unit 10 Review
Quiz
•
9th - 12th Grade