

COMPOSICIÓN PORCENTUAL
Presentation
•
Chemistry
•
10th Grade
•
Practice Problem
•
Easy
Paula Pinto
Used 8+ times
FREE Resource
19 Slides • 7 Questions
1
COMPOSICIÓN PORCENTUAL
SESIÓN 5

2
META DE COMPRENSIÓN
El estudiante comprenderá cómo se determina la composición porcentual de los elementos en un compuesto.
3
Multiple Choice
¿Cuántas moléculas hay en 1 mol de [(NH2)2CO]?
2 moléculas [(NH2)2CO]
1 molécula [(NH2)2CO]
6,022 x 1023 moléculas [(NH2)2CO]
4
Open Ended
Cuantos atomos de H hay en [(NH2)2CO]
5
COMPOSICIÓN PORCENTUAL
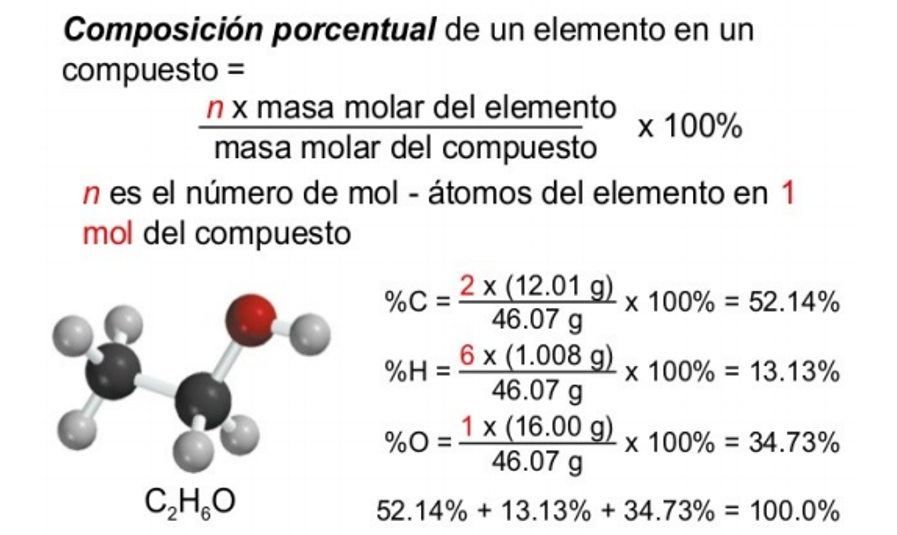
Cuando se conoce la fórmula de un compuesto, su composición química puede expresarse como la masa porcentual de cada elemento en el compuesto
Indica el porcentaje en masa, de cada elemento que forma parte de un compuesto. Básicamente se puede definir como: una parte dividida entre todas las partes multiplicada por 100.
6
Ejemplo
Una molécula de dióxido de carbono, CO2,
tiene un átomo de C y dos átomos de O. Determinar su composición porcentual
7
Paso 1: Identificar en la fórmula molecular la cantidad de átomos de cada elemento CO2
C: 1 átomo
O:2 átomos
Paso: 2 Determinar la masa molecular del compuesto CO2
C : 1 X 12g = 12 g
O: 2 X 16 g = 32 g
12 g + 32 g = 44 g -> 1 mol CO2
8

9
Open Ended

Calcule la composición porcentual en masa del HNO3.
H: 1 g
N: 14g
O: 16 g
10
Open Ended
Complete la frase Hoy aprendí que __________________
11
FÓRMULA EMPÍRICA Y FÓRMULA MOLECULAR
SESIÓN 6
12
META DE COMPRENSIÓN
El estudiante comprenderá cómo determinar la formula empirica y molecular de un compuesto
13
Open Ended

A partir de la imagen responder
¿ Qué veo?
¿Que pienso?
¿Que pregunto?
14
Fórmula empírica
Es la proporción más pequeña en números enteros de átomos presentes. En los compuestos moleculares, la fórmula molecular indica el número real de átomos presentes en una molécula del compuesto. Puede ser igual al de la fórmula mínima o un múltiplo entero de ésta.

15
Ejercicio
El análisis de un compuesto puro indica que contiene el 50.1% de azufre y el 49.9% de oxígeno en masa. ¿Cuál es la fórmula mínima del compuesto?
16

17

18
Fórmula molecular
Representa la cantidad real de átomos que hacen parte de una molécula. Las fórmulas moleculares están compuestas de símbolos y subíndices numéricos, cada símbolo representa un elemento y los subíndices la cantidad de cada uno de estos elementos.

19
Determinación de fórmulas moleculares
Para determinar la fórmula molecular de un compuesto molecular, debe conocerse tanto su fórmula empírica como su masa molecular

20
Ejemplo: Determinar la formula molecular de un compuesto el cual
contiene 50.1 g de S y 49.9 g de O. Y que su masa molecular es de 128g
21
PASO A PASO
Paso 1 : Determinar fórmula empírica o mínima
(Ejercicio anterior)
Fórmula empírica: SO2
22
Paso 2: Determinar la masa molecular de la formula empirica
SO2
S: 1X 32 g = 32 g
O: 2 X 16 g = 32g
32g + 32g = 64 g ( masa molecular SO2)
23
Paso 3: aplicar la fórmula para determinar n , qué nos indicará el número para determinar la fórmula molecular
n=64 g128 g= 2

24
Paso 4: Multiplicamos los subíndices de la fórmula empírica (SO2) por el valor de n que fue hallado
SO2 X 2 = S2O4
S2O4---> FÓRMULA MOLECULAR
25
Open Ended
¿ Cual es la fórmula molecular del compuesto , cuya fórmula empírica es HO y la masa molecular del compuesto es 34 g
26
Open Ended
Teniendo en cuenta lo visto hoy en clase
Escriba :
1 palabra clave del tema
1 idea con esa palabra
COMPOSICIÓN PORCENTUAL
SESIÓN 5

Show answer
Auto Play
Slide 1 / 26
SLIDE
Similar Resources on Wayground

19 questions
Formación de enlaces
Presentation
•
10th Grade

17 questions
Law of Conservation of Mass
Presentation
•
10th Grade

17 questions
Introduction to Molar Mass
Presentation
•
10th Grade

20 questions
Unit 6 reactions: Lesson 1: conservation and balancing equations
Presentation
•
10th Grade

20 questions
Función Acido
Presentation
•
10th Grade

20 questions
ekonomi kelas X
Presentation
•
10th Grade

19 questions
CUARESMAIMT
Presentation
•
10th Grade

19 questions
Heat of Formation
Presentation
•
10th Grade
Popular Resources on Wayground

16 questions
Grade 3 Simulation Assessment 2
Quiz
•
3rd Grade

19 questions
HCS Grade 5 Simulation Assessment_1 2526sy
Quiz
•
5th Grade

10 questions
Cinco de Mayo Trivia Questions
Interactive video
•
3rd - 5th Grade

17 questions
HCS Grade 4 Simulation Assessment_2 2526sy
Quiz
•
4th Grade

24 questions
HCS Grade 5 Simulation Assessment_2 2526sy
Quiz
•
5th Grade

13 questions
Cinco de mayo
Interactive video
•
6th - 8th Grade

20 questions
Math Review
Quiz
•
3rd Grade

30 questions
GVMS House Trivia 2026
Quiz
•
6th - 8th Grade
Discover more resources for Chemistry

22 questions
Solubility Curve Practice
Quiz
•
10th Grade

25 questions
Unit 12 Thermochemistry Review
Quiz
•
10th Grade

20 questions
Types of Chemical Reactions
Quiz
•
9th - 12th Grade

20 questions
Interpreting Solubility Curves
Quiz
•
10th Grade

20 questions
Types of Chemical Reactions
Quiz
•
10th Grade

43 questions
Acids and Bases Review
Quiz
•
10th - 11th Grade

20 questions
Thermochemistry Review
Quiz
•
10th Grade

25 questions
Unit 4 (Mid) Rumble
Quiz
•
10th Grade