

Entalpi
Presentation
•
Chemistry
•
11th Grade
•
Hard
Rara Aprilia
Used 10+ times
FREE Resource
21 Slides • 8 Questions
1

TERMOKIMIA
PERSAMAAN TERMOKIMIA DAN
PERUBAHAN ENTALPI STANDAR
Some text here about the topic of discussion.
2
Menganalisis perubahan entalpi melalui hasil percobaan
Menyajikan diagram tingkat energy dari persamaan termokimia
4.4 Menyimpulkan hasil analisis data percobaan termokimia pada tekanan tetap
Menjelaskan persamaan termokimia
Menentukan jenis entalpi
Menghitung harga entalpi
Menentukan kalor reaksi perubahan entalpi standar.
3.4 Menjelaskan konsep perubahan entalpi reaksi pada tekanan tetap dalam persamaan termokimia
KOMPETENSI DASAR
TERMOKIMIA
3
PERSAMAAN TERMOKIMIA
KIMIA| RIA
Termokimia

Diperoleh informasi bahwa reaksi fotosintesis membutuhkan energi sebanyak 2820 KJ.
Maka persamaan termokimianya dapat dituliskan: :
6CO2 + 6 H2O → C6H12O6 + 6O2 ΔH = +2820 KJ
Data apa saja yang dapat diperoleh dari Persamaan termokimia reaksi FOTOSINTESIS???
A + B -------> C + D ΔH= ...... KJ
4
6CO2 + 6 H2O → C6H12O6 + 6O2 ΔH = +2820 KJ
reaksi yang terdapat :
persamaan reaksi kimia
perubahan entalpi
jumlah koefisien zat = jumlah mol zat
maka dijelaskan:
6 mol CO2 bereaksi dengan 6 mol H2O menghasilkan 1 mol C6H12O6 dengan membutuhkan energi sebesar 2820 KJ
TERMOKIMIA
5
JENIS-JENIS ΔHO
PERUBAHAN ENTALPI PENGURAIAN STANDAR (ΔHOd)
PERUBAHAN ENTALPI PEMBAKARAN STANDAR (ΔHOC)
PERUBAHAN ENTALPI PEMBENTUKAN STANDAR (ΔHOf)
6

Some text here about the topic of discussion.
ΔH untuk membentuk 1 mol senyawa langsung dari unsur-unsurnya yang diukur pada keadaan suhu 289 K dan tekanan 1 atm.
contoh : persamaan termokimia dari ΔHOf H2O= - 285,85 KJ/mol
H2 (g) + 1/2 O2(g) --> H2O (l) ΔHOf= -285,85 KJ/mol
PERUBAHAN ENTALPI PEMBENTUKAN STANDAR (ΔHOf)
(STANDART ENTHALPY FORMATION)
koefisien H2O 1 maka 1 mol H2O
NOTE:
unsur-unsur stabil di alam:
unsur diatomik
N2, O2, H2, Cl2, Br2, I2
unsur padatan
sesuai unsur
7

Some text here about the topic of discussion.
PERUBAHAN ENTALPI PENGURAIAN STANDAR (ΔHOD)
(STANDART ENTHALPY DISSOSIATION)
ΔH untuk menguraikan 1 mol senyawa langsung menjadi unsur-unsurnya yang diukur pada keadaan suhu 289 K dan tekanan 1 atm (kebalikan dari ΔH pembentukan)
contoh : persamaan termokimia dari ΔHOd H2O= +285,85 KJ/mol
H2O → H2 (g) + 1/2 O2 (g) ΔHOd= + 285,85 KJ/mol
Koefisien H2O (1) = 1 mol H2O
8

ΔH untuk pembakaran sempurna 1 mol senyawa dengan O2 diudara yang diukur pada keadaan suhu 289 K dan tekanan 1 atm
contoh : persamaan termokimia ΔHOC C8H18 = -5500 KJ/mol
C8H18 (l) + 25/2 O2 (g)→ 8CO2(g) + 9H2O(l) ΔHOC = -5500 KJ/mol
termokimia
PERUBAHAN ENTALPI PEMBAKARAN STANDAR (ΔHOC)
(STANDART ENTHALPY COMBUTION)
koefisien C8H18 (1) = 1 mol C8H18
9
10
Mari Kita Quis....
Dan nilai Pemahamanmu...
Temukan yang belum pasti, tanyakan!!!
11
Multiple Choice
Untuk reaksi : 2 C(s) + O2(g) → 2 CO 𝛥H = -221 kJ
Pernyataan berikut adalah benar kecuali :
Reaksi berjalan secara eksoterm
Entalpi pembakaran = –110,5 Kj/mol
. Entalpi pembentukkan CO =-221 kJ
Reaksi tersebut adalah reaksi pembakaran
Entalpi penguraian CO = 110, 5 kJ
12
Multiple Choice
Pada pembakaran 570 gram isooktana (C8H18 (belum setara), salah satu komponen yang ada dalam bensin, pada keadaan standar/STP dibebaskan kalor sebesar 27.500 kJ. tulislah persamaan termokimia pembakaraan isooktana tersebut!
C8H18 (l) + 25/2 O2 (g)→ 8CO2(g) + 9H2O(l) ΔHOC = -5500 KJ/mol
C8H18 (l) + O2 (g)→ CO2(g) + H2O(l) ΔHOC = -5500 KJ/mol
C8H18 (l) + 25/2 O2 (g)→ 8CO2(g) + 9H2O(l) ΔHOC = -27500 KJ/mol
C8H18 (l) + O2 (g)→ CO2(g) + H2O(l) ΔHOC = -27500 KJ/mol
13
Multiple Choice
Persamaan termokimia yang benar untuk pembentukan 1 mol H2O dari unsur – unsur nya adalah . . .
2H2 + O2 → 2H2O
H2 + 2O2 → H2O
2H2O → 2H2 + O2
½ H2 + O2 → H2O
H2 + ½ O2 → H2O
14
Multiple Choice
Diketahui : H2O(l)→ H2O(g) ΔH = + 40 kJ/mol
berapakah kalor yang diperlukan untuk penguapan 4,5 gram H2O (Ar H = 1,0 Ar O = 16)?
+8 kJ
+9 kJ
+10 kJ
+11 kJ
+12 kJ
15
Cara Menghitung Harga Entalpi
Tergantung soal dan data yang diberikan
16
1. Jika diberikan data entalpi pembentukan, maka
Some text here about the topic of discussion
∆H reaksi = ∑ ∆Hfo produk - ∑ ∆Hfo pereaksi
17
Diketahui entalpi pembakaran propena C3H6(g) = -a kJ/mol; entalpi pembentukan CO2(g) = -b kJ/mol; dan entalpi pembentukan H2O(g) = -c kJ/mol. Entalpi pembentukan propena (dalam kJ/mol) adalah....
C3H6(g) + 9/2O2(g) → 3CO2(g) + 3H2O(g)
∆H pembakaran propena = ∑ ∆Hof produk - ∑ ∆Hof reaktan
∆H = (3. ∆Hof CO2 + 3. ∆Hof H2O) -( ∆Hof C3H8 + 9/2. ∆Hof O2)
-a = (3. -b + 4. -c) -( ∆Hof C3H8 + 0)
∆Hof C3H8 = a - 3b - 4c
18
Multiple Choice
Bila data entalpi pembentukan standar:
C3H8 (g) = – 104 kJ mol–1
CO2 (g) = – 394 kJ mol–1
H2O (g) = – 286 kJ mol–1
maka harga ΔH reaksi :
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(l) adalah …
–1.024 kJ
–1.121 kJ
–1.134 kJ
–2.232 kJ
-2.430 kJ
19
Amatilah reaksi berikut ini:
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(L) ∆Ho = -177,8 kJ/mol
Diketahui :
∆HfoNaOH(aq) = -426,7 kJ mol-1 ∆HfoNaCl(aq) = -411,0 kJ mol-1
∆HfoHCl(aq) = -92,3 kJ mol-1
∆HfoH2O(l) = -285,8 kJ mol-1
Some text here about the topic of discussion
20
NaCl(aq) + H2O(l)
{(-411 kJ/mol) + (-285,8 kJ/mol)}
(-696,8 kJ/mol)
∆H hasil reaksi (produk)
NaOH(aq) + HCl(aq)
{(-426,7 kJ/mol)+ (-92,3 kJ/mol)}
(-519 kJ/mol)
∆H pereaksi
Berdasarkan data ∆Hfo hitunglah jumlah ∆H pereaksi dan jumlah ∆H hasil reaksi (produk)!
Some text here about the topic of discussion
21
2. Diberikan tahapan persamaan reaksi (Hk. Hess)
22
Multiple Choice
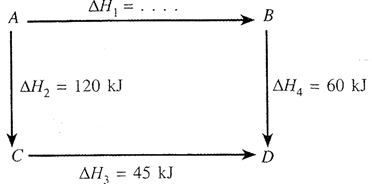
Siklus suatu reaksi ditunjukkan dengan diagram di atas ....
Dari siklus di atas harga ∆H1 adalah . . .
-225 kJ
+105 kJ
-135 kJ
+225 kJ
-105 kJ
23
Multiple Choice
Diketahui perubahan entalpi reaksi-reaksi berikut:
H2(g) + F2(g) → 2HF(g) ΔH = -537 kJ
C(s) + 2F2(g) → CF4(g) ΔH = -680 kJ
2C(s) + 2H2(g)→C2H4(g) ΔH = 52,3 kJ
Tentukan ΔH dari reaksi:
C2H4(g) + 6F2(g) → 2CF4(g) + 4HF(g)
-1234,5 kJ
-2486,3 kJ
-2642,6 kJ
-2467 kJ
-2592,6 kJ
24

3. Berdasarkan Energi Ikatan

C2H6
ΛH = jumlah energi ikatan pereaksi - jumlah energi ikatan produk
25
Multiple Choice

Jika energi ikatan rata- rata dari ;
– 510 kkal
– 72,8 kkal
– 12 kkal
+ 12 kkal
+ 510 kkal
26
4. Berdasarkan data percobaan
(kalorimeter)
Berdasarkan Azas Black = Jumlah kalor yang dilepaskan sama dengan jumlah kalor yang diterima
Q = m x c x ΔT
27
Di dalam suatu kalorimeter bom direaksikan 0,16 gram gas metana (CH4) dengan oksigen berlebih, sehingga terjadi reaksi sebagai berikut: CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (g) Ternyata terjadi kenaikan suhu sebesar 1,56°C. Diketahui kapasitas kalor kalorimeter yaitu 958 J/°C, massa air di dalam kalorimeter adalah 1.000 gram dan kalor jenis air 4,18 J/g°C. Tentukan kalor pembakaran gas metana dalam kJ/mol. (Ar C = 12, H = 1).
28
Pembahasan: Kalor yang dilepas selama reaksi sama dengan kalor yang diserap oleh air di dalam kalorimeter dan oleh kalorimeter, sehingga dapat dituliskan rumus sbb: qreaksi = – (qkalorimeter + qair) qair = mair x cair x ∆T = 1 x 4,18 J/g°C x 1,56 °C = 6.520 J qkalorimeter = Ckalorimeter x ∆T = 958 J/°C x 1,56°C = 1.494 J Maka, qreaksi = – (qkalorimeter + qair) = – (6.520 + 1.494) J = – 8.014 kJ Jumlah metana yang dibakar adalah 0,16 gram, sehingga jumlah molnya adalah sbb: Mol CH4=0,16 gram : 16 g/mol = 0,01 mol Untuk setiap reaksi pembakaran satu mol CH4 akan dilepaskan kalor sebanyak: qreaksi = – 8.014 kJ : 0,01 mol = – 801,4 kJ/mol Sehingga, besarnya ∆H = qreaksi= – 801,4 kJ/mol.
29
Apakah ada pertanyaan ????
Some text here about the topic of discussion


TERMOKIMIA
PERSAMAAN TERMOKIMIA DAN
PERUBAHAN ENTALPI STANDAR
Some text here about the topic of discussion.
Show answer
Auto Play
Slide 1 / 29
SLIDE
Similar Resources on Wayground

22 questions
Khái niệm pH. Ý nghĩa của pH.
Presentation
•
11th Grade

19 questions
PARTICULAS, ÁTOMOS Y MOLÉCULAS
Presentation
•
12th Grade

21 questions
Charles's Law and the Combined Gas Law
Presentation
•
11th - 12th Grade

20 questions
CM 02.2 Changes in Matter
Presentation
•
11th Grade

24 questions
PERADABAN ISLAM PADA MASA MODEREN
Presentation
•
11th Grade

24 questions
Government Response to the Great Depression
Presentation
•
11th Grade

21 questions
El Carbono
Presentation
•
11th Grade

23 questions
UNIDADES DE CONCENTRACION QUIMICA
Presentation
•
11th Grade
Popular Resources on Wayground

15 questions
Grade 3 Simulation Assessment 1
Quiz
•
3rd Grade

22 questions
HCS Grade 4 Simulation Assessment_1 2526sy
Quiz
•
4th Grade

16 questions
Grade 3 Simulation Assessment 2
Quiz
•
3rd Grade

19 questions
HCS Grade 5 Simulation Assessment_1 2526sy
Quiz
•
5th Grade

17 questions
HCS Grade 4 Simulation Assessment_2 2526sy
Quiz
•
4th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

24 questions
HCS Grade 5 Simulation Assessment_2 2526sy
Quiz
•
5th Grade

20 questions
Math Review
Quiz
•
3rd Grade
Discover more resources for Chemistry

20 questions
Types of Chemical Reactions
Quiz
•
9th - 12th Grade

20 questions
Redox Reactions
Quiz
•
10th - 12th Grade

20 questions
pH and pOH Calculations
Quiz
•
10th - 11th Grade

36 questions
Unit 4 (Part 2) Solutions
Quiz
•
10th - 12th Grade

30 questions
Final Exam Prep S22: 2.1.A.1 Isotopes
Quiz
•
9th - 12th Grade

25 questions
Stoichiometry Mass to Mass
Quiz
•
10th - 11th Grade

15 questions
Calculating pH and pOH
Quiz
•
10th - 12th Grade

15 questions
Balancing Chemical Equations
Quiz
•
10th - 12th Grade