

quizz- fisico quimica
Presentation
•
Chemistry
•
11th Grade
•
Practice Problem
•
Medium
Polina Gololobova
Used 1+ times
FREE Resource
7 Slides • 19 Questions
1

Aspetos quantitativos das reações químicas
trabalho de investigação - quiz

Polina Gololobova
Miguel Martinho
Tiago Martins
11CT3
2
Reações químicas e reagente limitante

3
Multiple Choice
Numa mistura reacional formada por 25,0 g de prata, Ag, e 5,00 g de enxofre, S, formou-se sulfureto de diprata, Ag2 S, de acordo com 2 Ag (s) + S (s) 🠖 Ag2 S (s)
Indique qual é o reagente limitante.
Prata, Ag
Enxofre, S
4
Multiple Choice

Na figura encontra-se uma representação da reação do sódio metálico, Na, com o cloro gasoso, Cℓ2.
Escreva a equação química da reação representada.
5
Multiple Choice
Identifique o reagente limitante.
todos
NaCL
Na
Cl
6
Multiple Choice

Tendo em conta a seguinte equação química, pode afirmar-se que:
1. A quantidade de hidrogénio formado é tripla da quantidade de água consumida.
2. A quantidade de hidrogénio formado é tripla da quantidade de monóxido de carbono.
3. A quantidade de metano consumido é tripla da quantidade de monóxido de carbono.
4. O metano e a água são consumidos na mesma proporção.
Apenas a afirmação 3 está correta.
Verdadeiro
Falso
7
Química verde

8
Multiple Choice
Classifique a seguinte afirmação em verdadeiro ou falso.
A química verde tem por base o aumento de resíduos.
Verdadeiro
Falso
9
Multiple Choice
O titânio pode ser extraído por dois processos distintos.
Um dos processos utiliza um metal mais reativo para provocar o deslocamento do titânio, de acordo com a seguinte equação química:
TiO2 (s) + 2 Mg (s) → Ti (s) + 2 MgO (s)
Outro processo consiste na eletrólise do TiO2, de acordo com a seguinte equação química:
TiO2 (l) → Ti (l) + O2 (g)
Calcula a economia atómica percentual para cada um dos processos.
59,9 % e 40,1% , respetivamente
20,5% e 30,9%, respetivamente
59,9% e 48,5% , respetivamente
20,5% e 60,9 %, respetivamente
10
Rendimento de uma reação química

11
Multiple Choice

O hidrogénio pode ser obtido a partir do metano, CH4, de acordo com a seguinte equação química
A partir de uma amostra de 80g de metano, utilizando água em excesso, obtiveram-se 15g de hidrogénio.
Selecione a opção que corresponde ao rendimento da reação.
19%
29%
91%
81%
12

Grandezas químicas
13
Multiple Choice

A cada uma das grandezas físicas A a D associe as medidas 1 a 4.
A-3, B-4, C-1, D-2
A-1, B-4 , C-2 ; D-3
A-4, B-1, C-3, D-2
A-3, B-4, C-2, D-1
14
Multiple Choice
Determina o volume ocupado por 10 g de oxigénio molecular, nas condições PTN.
5 dm3
10 dm 3
6,1 dm3
7,1 dm3
15
Multiple Choice
Uma garrafa de dioxigénio, O2 , contém 224 litros desse gás nas condições PTN. Se aquele volume de gás for comprimido:
(A) a quantidade de matéria de dioxigénio aumenta e a massa diminui.
(B) a quantidade de matéria de dioxigénio diminui e a massa também.
(C) a quantidade de matéria de dioxigénio mantém-se e o volume diminui.
(D) a quantidade de matéria de dioxigénio mantém-se e o volume aumenta.
16
Multiple Choice
No rótulo de uma garrafa de água surge a informação relativa à concentração mássica de iões de sódio, sendo esse valor igual a 7,1 mg/L. Determina a massa de sódio pressente em 100mL de água.
7,7 x 10-4 g
1,5 x 10-4g
5,0 x 10-4g
3,7 x 10-4 g
17
Multiple Choice
Considere as verdadeiras e falsas.
A) A grandeza de quantidade de matéria representa-se por N, e a sua unidade é mole.
B) Quando há conservação de massa não significa haver conservação de volume nem da quantidade de matéria de moléculas de gases.
C) Na maioria das reações, um ou mais reagentes são consumidores completamente.
D) O reagente que se esgota primeiro é o fator limitante que dirige a toda a reação.
A-F, B-V , C-F,
D-V
A-V, B-V, C-V
D-V
A-F, B-F, C-F,
D-V
A-F, B-V, C-F
D-F
18
Multiple Choice
O tetracloreto de tiânio, TiCl4, é usado na produção de titânio. Para produzir TiCl4 misturaram-se 40g de dióxido de titânio,TiO2, e 63 g de dicloro Cl2, também sabemos que no carbono, C temos 1,50 mol.A reação ocorreu de acordo com a equação:
TiO2 (s) + 2 Cl2 (g) + 2 C (s) ➝ TiCl4 (l) + 2CO (g)
Determina o reagente limitante.
Cl
TiO
C
CO
19
Reações químicas e reagente limitante

20
Multiple Choice
A adição de água líquida a cálcio sólido origina uma solução aquosa de cálcio(2) e de hi-dróxido, OH ,
com libertação de di-hidrogénio gasoso.
A equação química que representa a reação descrita é :
Ca (s) + 2 H2O (l) →Ca 2(aq) + 2 OH (aq) + H2(g)
Verdadeiro
Falso
21
Multiple Choice
O tricloreto de ferro, FeCl3 , uma substânciausada no tratamento de águas efluentes,pode ser
obtido pela reação traduzida pelaequação química
2 Fe (s) + 3 Cl2 (g) 2 FeCl3 (s)
Considere a reação completa a partir damistura de 200 g de Fe (M = 55,85 g mol−1) e500 g de Cl2 (M =
70,90 g mol–1).
Qual é o reagente limitante?
Cl
Fe
22
Multiple Choice
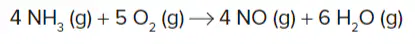
A seguinte equação está acertada?
Sim
Não
23

Grandezas químicas
24
Multiple Choice

Calcula a massa molar de CuSO4.
210,1 g/mol
157,30 g/mol
69,54 g/mol
159,65 g/mol
25
Multiple Choice
Na sequência da explosão do tanque da Apollo 13, a tripulação diminuiu o consumo de água para
200 mL por dia por pessoa. Este valor é 1/5 do consumo normal por dia por astronauta.
Considere ρ(H2O) = 1,00 kg dm−3. Calcule, para o consumo normal diário de um astronauta:
o número de moléculas de água.
3,34 x 1025
2,34 x 1025
3,24x 1025
2,24x 1025
26
Multiple Choice
A produção de trióxido de enxofre, importante na indústria de produção de ácido sulfúrico, é traduzida pela equação 2 SO2 (g) + O2 (g) 2 SO 3 (g) Sendo a reação completa, e mantendo cons- tantes as condições de pressão e de tempe- ratura, quando se misturam 3,0 L de SO 2 com 2,0 L de O2 o volume total de gases...
diminui em 1,5 L.
diminui em 1,0 L.
não se altera.
aumenta em 0,50 L.

Aspetos quantitativos das reações químicas
trabalho de investigação - quiz

Polina Gololobova
Miguel Martinho
Tiago Martins
11CT3
Show answer
Auto Play
Slide 1 / 26
SLIDE
Similar Resources on Wayground

19 questions
ENLACE QUIMICO
Presentation
•
11th Grade

21 questions
Oxidation States
Presentation
•
10th Grade

19 questions
Periodic Trends
Presentation
•
10th - 12th Grade

19 questions
Reviewing Atoms, Ions, the Periodic Table, and Lewis dots
Presentation
•
10th - 12th Grade

20 questions
Road Signs #4
Presentation
•
11th Grade

20 questions
Vocabulary Things Fall Apart
Presentation
•
KG

20 questions
Energetics Lecture 1 Review
Presentation
•
11th - 12th Grade

20 questions
Atomic Structure
Presentation
•
10th Grade
Popular Resources on Wayground

10 questions
Factors 4th grade
Quiz
•
4th Grade

10 questions
Cinco de Mayo Trivia Questions
Interactive video
•
3rd - 5th Grade

13 questions
Cinco de mayo
Interactive video
•
6th - 8th Grade

20 questions
Math Review
Quiz
•
3rd Grade

20 questions
Main Idea and Details
Quiz
•
5th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

19 questions
Classifying Quadrilaterals
Quiz
•
3rd Grade
Discover more resources for Chemistry

20 questions
Types of Chemical Reactions
Quiz
•
9th - 12th Grade

25 questions
Enthalpy - endo/exo and PED
Quiz
•
11th - 12th Grade

17 questions
Types of Chemical Reaction
Presentation
•
7th - 12th Grade

120 questions
Chemistry Final Review
Quiz
•
9th - 12th Grade

47 questions
Q1 Chem Review
Quiz
•
10th - 12th Grade

10 questions
Stoichiometry Mole to Mole
Quiz
•
10th - 11th Grade

15 questions
Half-Life
Quiz
•
9th - 12th Grade

15 questions
Unit 10 Review
Quiz
•
9th - 12th Grade