

Korosi
Presentation
•
Chemistry
•
12th Grade
•
Practice Problem
•
Easy
Chintya Hutagalung
Used 4+ times
FREE Resource
12 Slides • 12 Questions
1
Korosi
By Chintya DEH, S.Pd

2
Open Ended
Jelaskan pengertian reaksi oksidasi
3
Open Ended
Jelaskan makna posisi logam yang terdapat pada deret volta
4

Lihatlah bahwa kerusakan besi pada anjungan berkarat dimulai dari besi bagian bawah atau kontak dengan air. Sedangkan pada motor bagian knalpot akan mengalami perkaratan terlebih dahulu dibanding bagian lainnya.
Perhatikan ilustrasi berikut!
5
Korosi
Proses elektrokimia yang terjadi di alam sekitar kita dapat menimbulkan reaksi kimia pada logam-logam yang kita pergunakan sehari-hari. Proses tersebut dinamakan korosi.
Biasanya logam besi mudah mengalami korosi yang dikenal debagai peristiwa perkaratan.
6

Untuk melindungi menara/konstruksi dari besi agar tidak mudah terkena perkaratan (korosi), yaitu dengan menanamkan kaki-kaki menara dalam tanah yang dihubungkan dengan logam Mg yang ditimbun pasir dan kerikil kering.
Melindungi menara besi dari perkaratan
7
Mengapa logam Mg ditimbun dengan kerikil dan pasir kering?
Logam magnesium memiliki potensial reduksi yang lebih rendah dibandingkan besi. Hal ini menyebabkan magnesium lebih mudah teroksidasi (berkarat) daripada besi. Dalam sistem ini, magnesium bertindak sebagai anode, yaitu elektrode yang melepaskan elektron.
Elektron yang dilepaskan oleh magnesium akan mengalir menuju besi. Akibatnya, besi menjadi katoda dan terlindungi dari oksidasi. Proses ini dikenal sebagai perlindungan katodik.
Tanah di sekitar konstruksi biasanya mengandung kelembaban yang cukup untuk bertindak sebagai elektrolit. Elektrolit ini memungkinkan aliran ion-ion antara magnesium dan besi, sehingga proses perlindungan katodik dapat berlangsung.
8
Mengapa logam Mg ditimbun dengan kerikil dan pasir kering?
Kerikil dan pasir kering berfungsi sebagai isolator yang mencegah kontak langsung antara magnesium dengan tanah yang terlalu lembap. Hal ini akan memperlambat laju korosi pada magnesium dan memperpanjang umur layanannya.
Dengan mengubur magnesium di sekitar konstruksi, perlindungan katodik dapat diberikan secara merata ke seluruh permukaan besi yang tertanam di dalam tanah. Magnesium relatif murah dan mudah didapatkan, sehingga metode ini cukup ekonomis. Setelah dipasang, sistem perlindungan katodik ini tidak memerlukan perawatan yang rumit.
9
Mengapa logam Mg digunakan dalam cara tersebut di atas?
Magnesium memiliki potensial reduksi yang sangat negatif, sehingga sangat efektif dalam melindungi besi.
Magnesium mudah didapatkan dan harganya relatif terjangkau.
Magnesium telah terbukti memberikan kinerja yang baik dalam berbagai aplikasi perlindungan katodik.
10
Coba terangkan dengan proses elektro kimia, kalau diketahui:
Fe2+ + 2e → Fe; E° = -0,41 volt
Mg2+ + 2e → Mg; E° = -2,34 volt
Sehingga menara besi dapat terlindung dari perkaratan.
Memahami Potensial Elektroda Standar (E°) :
Nilai E° yang lebih negatif menunjukkan kecenderungan suatu zat untuk melepas elektron (teroksidasi) lebih besar.
Dengan nilai E° -0,41 volt, besi cenderung mudah teroksidasi (berkarat) dalam kondisi tertentu.
Dengan nilai E° -2,34 volt, magnesium jauh lebih mudah teroksidasi dibandingkan besi. Ini berarti magnesium akan lebih mudah melepaskan elektron.
Ketika logam besi dan magnesium dihubungkan dalam tanah yang mengandung elektrolit (air dan mineral dalam tanah), terbentuklah sebuah sel volta.
Logam magnesium dengan potensial reduksi lebih negatif akan menjadi anode, sementara besi menjadi katode.
11
Dapatkah logam Mg diganti dengan logam lain? Bila jawaban dapat, beri contoh!
Logam lain yang umum digunakan sebagai anode dalam perlindungan katodik antara lain:
Aluminium, memiliki potensial reduksi yang lebih negatif dibandingkan besi, sehingga dapat berfungsi sebagai anode. Namun, lapisan oksida yang terbentuk pada aluminium dapat menghambat kinerja perlindungan katodik.
Seng, sering digunakan dalam pelapisan galvanis pada besi. Seng juga memiliki potensial reduksi yang lebih negatif daripada besi, sehingga dapat melindungi besi dari korosi.
12
Kalau dalam peristiwa di atas ada proses elektrokimia, tunjukkan logam yang bertindak sebagai anoda dan katoda!
Logam magnesium memiliki potensial reduksi yang lebih rendah dibandingkan besi. Hal ini menyebabkan magnesium lebih mudah teroksidasi (berkarat) daripada besi. Dalam sistem ini, magnesium bertindak sebagai anode, yaitu elektrode yang melepaskan elektron.
Elektron yang dilepaskan oleh magnesium akan mengalir menuju besi. Akibatnya, besi menjadi katoda dan terlindungi dari oksidasi. Proses ini dikenal sebagai perlindungan katodik.
Tanah di sekitar konstruksi biasanya mengandung kelembaban yang cukup untuk bertindak sebagai elektrolit. Elektrolit ini memungkinkan aliran ion-ion antara magnesium dan besi, sehingga proses perlindungan katodik dapat berlangsung.
13
zat Elektrolit (asam, basa, dan garam)
permukaan besi yang tidak merata
Faktor Pendukung
Gas Oksigen dan air
Faktor Utama
Faktor yang mempengaruhi proses korosi
14
Pengorbanan anoda
Menggunakan arus paksa (Impressed current)
2. Teknik perlindungan katoda atau proteksi katoda.
Pengecatan
Pelapisan dengan Plastik
Pelapisan dengan minyak atau oli
Tin plating (pelapisan dengan timah)
Chrome plating (pelapisan dengan krom)
Pelapisan dengan Seng (Galvanisasi)
1. Teknik pelapisan logam.
Pencegahan Korosi
15
Multiple Choice
Berikut ini yang merupakan faktor-faktor penyebab terjadinya korosi adalah …
Air dan oksigen
Oksigen dan tanah
Tanah dan minyak
Minyak dan larutan asam
Minyak dan air
16
Multiple Choice
Dalam proses perkaratan besi, besi bertindak sebagai …
katoda
anoda
katalis
jembatan garam
elektrolit
17
Multiple Choice
Jika diketahui larutan A, B, C, D dan E berturut-turut mempunyai pH = 4, 6, 7, 8 dan 9, manakah dari larutan tersebut yang paling cepat menyebabkan perkaratan pada besi?
Larutan A
Larutan B
Larutan C
Larutan D
Larutan E
18
Multiple Choice
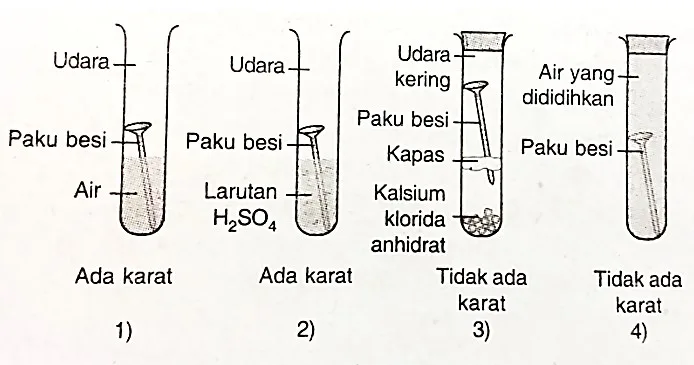
Diketahui gambar percobaan tentang korosi besi berikut:
Catatan :
- Air mendidih mengandung lebih sedikit gas oksigen terlarut.
- Senyawa anhidrat mempunyai sifat mudah menyerap air.
Berdasarkan data tersebut urutan terbentuknya korosi dari yang paling cepat adalah .. . .
1 – 2 – 4 – 3
2 – 1 – 4 – 3
3 – 1 – 2 – 4
3 – 4 – 1 – 2
4 – 2 – 1 – 3
19
Multiple Choice

Perhatikan gambar proses korosi berikut!
Proses korosi yang berlangsung paling lambat adalah ….
1
2
3
4
5
20
Multiple Choice
Salah satu kelebihan pencegahan perkaratan pada besi dengan cara pengecatan adalah…
Tidak bisa rusak.
Tidak mudah patah.
Tidak mudah terbakar.
Mempunyai nilai estetika.
Tidak mudah tergores.
21
Multiple Choice
Berikut tentang cara pencegahan perkaratan dengan cara pelapisan logam menggunakan logam krom (Cr) kecuali …
Dilakukan dengan elektrolisis.
Tidak mudah berkarat.
Memberikan penampilan mengkilat.
Biasa digunakan untuk melapisi bamper mobil.
Besi tidak berkarat meskipun sebagian lapisan crom rusak.
22
Multiple Choice
Salah satu kelemahan pada cat berbahan dasar minyak adalah…
Mudah terbakar.
Mudah berkarat.
Lengket
Mudah meleleh.
Mudah patah.
23
Multiple Choice
Pencegahan perkaratan menggunakan pelumuran oli atau minyak lebih cocok untuk benda …
Gear pada mesin motor.
Pagar
Kompor
Kawat
paku
24
Multiple Choice
Pada Teknik perlindungan katodik, anoda dipilih dari logam yang memenuhi spesifikasi berikut …
lebih murah dari besi
lebih kuat dari besi
lebih tahan karat dari besi.
potensial reduksi lebih kecil dari pada besi.
lebih mudah memuai dari pada besi
Korosi
By Chintya DEH, S.Pd

Show answer
Auto Play
Slide 1 / 24
SLIDE
Similar Resources on Wayground

18 questions
Surat Lamaran Pekerjaan
Presentation
•
12th Grade

20 questions
Korosi
Presentation
•
12th Grade

19 questions
BENZENA & TURUNANNYA
Presentation
•
12th Grade

17 questions
Sifat Koligatif Larutan
Presentation
•
12th Grade

19 questions
Materi Norma - Observasi
Presentation
•
12th Grade

20 questions
Prinsip & Fungsi Manajemen Pergelaran Tari KD 3.1_Teleportasi
Presentation
•
12th Grade

19 questions
Materi asam basa
Presentation
•
11th - 12th Grade

19 questions
BIOTEKNOLOGI
Presentation
•
12th Grade
Popular Resources on Wayground

20 questions
Math Review
Quiz
•
3rd Grade

15 questions
Fast food
Quiz
•
7th Grade

20 questions
Context Clues
Quiz
•
6th Grade

20 questions
Inferences
Quiz
•
4th Grade

19 questions
Classifying Quadrilaterals
Quiz
•
3rd Grade

20 questions
Figurative Language Review
Quiz
•
6th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

10 questions
Identify Fractions, Mixed Numbers & Improper Fractions
Quiz
•
3rd - 4th Grade