

Clase 6a Estequiometría
Presentation
•
Chemistry
•
University
•
Easy
Rocio Rosado
Used 3+ times
FREE Resource
24 Slides • 26 Questions
1

2

3
Multiple Choice
¿Cuál es la función de los coeficientes en una ecuación química?
Indicar el número relativo de moléculas de cada tipo involucradas en la reacción.
Mostrar la energía liberada en la reacción.
Identificar los productos de la reacción.
Determinar la velocidad de la reacción.
4
Open Ended
¿Cuántos átomos de Mg, H y O hay en 3Mg(OH)₂?
5

6
Multiple Choice
¿Cuál es el primer paso recomendado para balancear una ecuación química según el texto?
Balancear el oxígeno primero
Balancear el hidrógeno primero
Balancear el carbono primero
Balancear los elementos que aparecen en menor número de fórmulas químicas
7

8
Multiple Choice
¿Qué elementos y cuántos átomos de cada uno están presentes en ambos lados de la ecuación balanceada de la reacción entre CH₄ y O₂?
CH4 + 2O2 --> CO2 + 2H2O
1 C, 4 H, 4 O
2 C, 4 H, 2 O
1 C, 2 H, 4 O
1 C, 4 H, 2 O
9

10
Fill in the Blanks

11

12
Open Ended
Balancee la ecuación de la reacción mostrada:
H₂O → H₂ + O2
13

14
Open Ended
¿Cuál es la ecuación balanceada para la descomposición del nitrato de amonio para formar nitrógeno, oxígeno molecular y agua?
NH4NO3 --> N2 + O2 + H2O
15
Multiple Choice
¿Por qué a veces es conveniente usar fracciones al balancear ecuaciones químicas antes de multiplicar por un factor entero?
Porque simplifica el proceso de balanceo y evita errores.
Porque las fracciones son más fáciles de manejar que los números enteros.
Porque siempre se obtienen números enteros al final.
Porque las fracciones permiten identificar los reactivos limitantes.
16

17
Multiple Choice
¿Qué información adicional se puede incluir en una ecuación química además de los reactivos y productos?
Estados físicos de las sustancias y condiciones de la reacción.
El color de los reactivos.
La masa de cada compuesto.
El costo de los reactivos.
18
Dropdown
19
Dropdown
20
Dropdown
21
Fill in the Blanks
22

23

24
Multiple Choice
¿Cuál es la relación estequiométrica entre huevos y pancakes (8 panckaes/1 huevo) según el ejemplo dado, y cuántos huevos se necesitan para preparar 40 pancakes?
1 huevo por cada 8 pancakes; 5 huevos para 40 pancakes.
1 huevo por cada 4 pancakes; 10 huevos para 40 pancakes.
1 huevo por cada 6 pancakes; 6 huevos para 40 pancakes.
2 huevos por cada 8 pancakes; 10 huevos para 40 pancakes.
25

26
Multiple Choice
¿Cuál es la relación estequiométrica correcta entre el potasio (K) y el bromo (Br2) en la reacción: 2K(s) + Br2(l) → 2KBr(s)?
2 mol K / 1 mol Br2
1 mol K / 2 mol Br2
2 mol Br2 / 2 mol K
1 mol Br2 / 1 mol K
27

28
Multiple Choice
¿Cuántos moles de Ca(OH)2 se requieren para reaccionar con 1.36 moles de H3PO4 y producir Ca3(PO4)2 de acuerdo con la ecuación:
3Ca(OH)2 + 2H3PO4 → Ca3(PO4)2 + 6H2O?
2.04 moles
1.36 moles
3.00 moles
0.91 moles
29

30
Multiple Select
Selecciona todas las afirmaciones correctas sobre la conversión de moles a moléculas en una reacción química.
Se utiliza el número de Avogadro para convertir moles a moléculas.
La relación molar de la ecuación balanceada es esencial para el cálculo.
Solo se puede convertir moles de reactivos, no de productos.
La cantidad de moléculas depende de la cantidad de moles presentes.
31

32
Open Ended
¿Qué masa de MgCl2 se requiere para producir 16g de Mg(OH)2 ? según la ecuación:
MgCl2(ac) + 2NaOH(ac) → Mg(OH)2(s) + 2NaCl(ac)
33
Open Ended
¿Qué masa de óxido de galio, Ga2O3, se preparan con 29.0g de galio metálico de acuerdo con la ecuación?:
4Ga + 3O2 → 2Ga2O3
34

35
Open Ended
¿Cuál es el procedimiento para calcular la masa de oxígeno gaseoso O2 que se consume en la combustión de 72g de butano C4H10?
36
Open Ended
¿Qué masa de CO se requieren para reaccionar con 23.13g de Fe2O3 de acuerdo con la ecuación: Fe2O3 + 3CO → 2Fe + 3CO2?
37

38
Multiple Choice
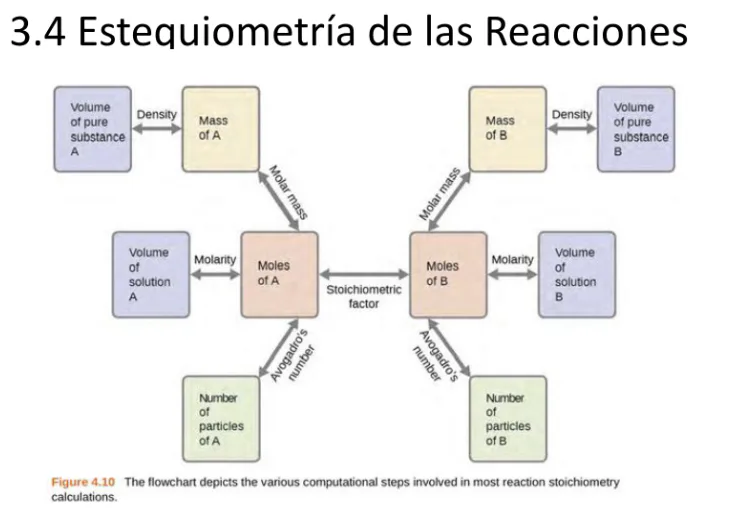
¿Cuál es el propósito del diagrama de flujo mostrado para los cálculos estequiométricos de las reacciones químicas?
Mostrar los pasos para calcular la masa de reactivos y productos en una reacción.
Explicar cómo balancear ecuaciones químicas.
Identificar los reactivos limitantes en una reacción.
Describir la energía liberada en una reacción.
39

40

41
Open Ended
En la preparación de sándwiches, si tienes 28 lonjas de pan y 11 lonjas de queso, ¿cuántos sándwiches puedes preparar?
42
Multiple Choice
¿Qué conceptos de la estequiometría se pueden ilustrar con la analogía de preparar sándwiches usando pan y queso?
Reactivo limitante y reactivo en exceso.
Balanceo de ecuaciones químicas.
Ley de conservación de la masa.
Cálculo de la energía de reacción.
43

44

45

46

47
Open Ended
¿Cuál es el reactivo limitante cuando 5.00g de H2 y 10.0g de O2 reaccionan para formar agua?
48

49

50
Open Ended
¿Cuál es el por ciento de rendimiento de una reacción que produce 12.5g de freón CF2Cl2 apartir de 32.9g de CCl4 y un exceso de HF?
CCl4n+ 2HF --> CF2Cl2 + 2HCl

Show answer
Auto Play
Slide 1 / 50
SLIDE
Similar Resources on Wayground

45 questions
Lilie Quiz 40ans
Presentation
•
University

42 questions
forest
Presentation
•
University

44 questions
Introducción al estudio de Química
Presentation
•
12th Grade

45 questions
Toma de muestras sanguíneas
Presentation
•
University

47 questions
Fruit and Vegetables/Imperatives - CAp
Presentation
•
12th Grade

46 questions
Les pronoms rélatifs
Presentation
•
University

45 questions
Examen Repaso Semana 2
Presentation
•
KG - University

45 questions
Sensores_6IA2
Presentation
•
University
Popular Resources on Wayground

15 questions
Grade 3 Simulation Assessment 1
Quiz
•
3rd Grade

22 questions
HCS Grade 4 Simulation Assessment_1 2526sy
Quiz
•
4th Grade

16 questions
Grade 3 Simulation Assessment 2
Quiz
•
3rd Grade

19 questions
HCS Grade 5 Simulation Assessment_1 2526sy
Quiz
•
5th Grade

17 questions
HCS Grade 4 Simulation Assessment_2 2526sy
Quiz
•
4th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

24 questions
HCS Grade 5 Simulation Assessment_2 2526sy
Quiz
•
5th Grade

20 questions
Math Review
Quiz
•
3rd Grade
Discover more resources for Chemistry

36 questions
8th Grade US History STAAR Review
Quiz
•
KG - University

25 questions
Spanish future tense
Quiz
•
10th Grade - University

55 questions
Post Malone Addtion (Tres)
Quiz
•
12th Grade - University

15 questions
Quotation Marks vs. Italics for MLA
Quiz
•
9th Grade - University

20 questions
Disney Trivia
Quiz
•
University

50 questions
AP Biology Exam Review 2017
Quiz
•
11th Grade - University

215 questions
8th Physical Science GA Milestones Review
Quiz
•
KG - University

20 questions
Ch15_review_TEACHER
Quiz
•
University