

Termokimia
Presentation
•
Chemistry
•
11th Grade
•
Hard
Sintya Ariasih
Used 25+ times
FREE Resource
19 Slides • 4 Questions
1
by Ibu Sintya
2
Kegiatan apakah di bawah ini?
Tubuh terasa hangat ketika berada di dekat api unggun.
Hal tersebut menunjukkan panas dari api unggun berpindah ke lingkungan.
Peristiwa tersebut merupakan salah satu peristiwa dalam materi TERMOKIMIA

3
Pada saat mempelajari termokimia, kita harus paham mana yang menjadi pusat pengamatan, mana yang bukan.
Segala sesuatu yang menjadi pusat pengamatan disebut sistem, sedangkan segala sesuatu di luar sistem dan dapat mempengaruhi sistem disebut lingkungan
4
Berdasarkan perpindahan kalor dan materi, sistem dibedakan menjadi 3 jenis, yaitu:
- Sistem Terbuka merupakan suatu sistem dimana dapat dimungkinkan terjadinya perpindahan kalor serta materi.
- Sistem Tertutup merupakan suatu sistem dimana dapat dimungkinkan terjadinya perpindahan kalor, tetapi tidak terjadi perpindahan materi.
- Sistem Terisolasi merupakan suatu sistem dimana tidak dimungkinkan terjadinya perpindahan kalor dan materi.

5
Nahhh mari kita kuis dulu, untuk menguji apakah kalian sudah memahami materi ini
SIAP ?
6
Multiple Choice
Terdapat beberapa benda dalam kehidupan sekitar kita:
a. Segelas kopi panas dengan tutup
b. Segelas teh panas tanpa tutup
c. Termos air panas
Ketiga benda bila diasumsikan menjadi sistem yang diurutkan menjadi sistem terisolasi, sistem tertutup dan sistem terbuka, maka urutan yang tepat adalah ....
a – b – c
a – c – b
b – a – c
c – b – a
c – a – b
7
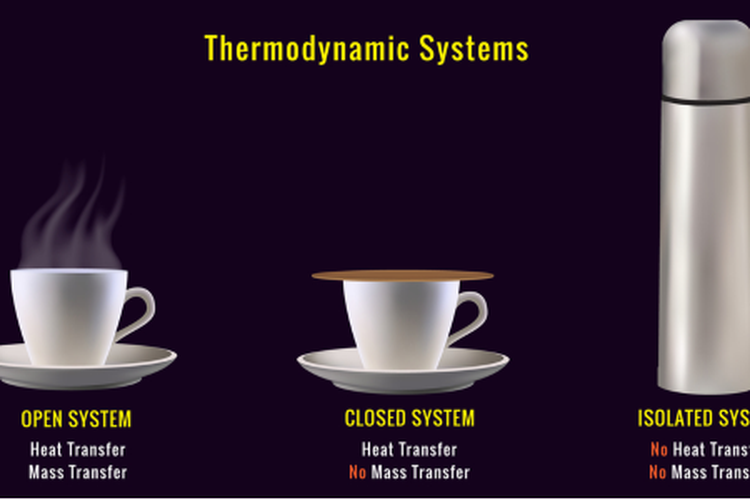
Apakah jawaban kalian sudah tepat? Jika masih salah, perhatikan gambar di bawah
a. Segelas kopi panas dengan tutup termasuk sistem tertutup karena hanya ada perpindahan panas (kalor ) saja
b. Segelas teh panas tanpa tutup termasuk sistem terbuka karena ada perpindahan panas (kalor) dan materi berupa uap air
c. Termos air panas termasuk sistem terisolasi karena tidak terjadi perpindahan panas ataupun materi
8
Sesuai hukum Termodinamika, perpindahan kalor secara spontan terjadi pada benda yang memiliki perbedaan suhu.
Dalam termokimia, hanya ada 2 kemungkinan perbedaan suhu, yaitu suhu sistem lebih tinggi dari suhu lingkungan atau suhu sistem yang lebih rendah dari suhu lingkungan.
suhu sistem lebih tinggi dari suhu lingkungan : Reaksi Eksoterm
suhu sistem yang lebih rendah dari suhu lingkungan : Reaksi Endoterm

9
1. Reaksi eksoterm
Pada keadaan di mana suhu sistem lebih tinggi maka akan terjadi aliran kalor dari sistem menuju lingkungan, dengan kata lain kalor akan keluar menuju lingkungan.
Pada keadaan seperti ini kalor sistem dikeluarkan menuju lingkungan, maka entalpi akhir reaksi akan menjadi lebih kecil dibanding entalpi awal sebelum reaksi, besarnya perubahan entalpi (𝛥H) adalah: 𝛥H = H akhir – H awal
𝛥H = kecil – besar
𝛥H < 0 , atau bertanda negatif ( – )
Maka, reaksi eksoterm 𝛥H bertanda negatif (-)

10
2. Reaksi endoterm
Pada keadaan dimana sistem lebih rendah dari suhu lingkungan maka akan terjadi aliran kalor dari lingkungan menuju sistem, dengan kata lain kalor akan masuk menuju sistem. Hal ini dikenal dengan proses endoterm.
kalor sistem bertambah, maka entalpi akhir reaksi akan menjadi lebih besar dibanding entalpi awal sebelum reaksi.
Dengan demikian besarnya perubahan entalpi (𝛥H) adalah:
𝛥H = H akhir – H awal, 𝛥H = besar – kecil;
𝛥H > 0 , atau bertanda positif ( + )
Dengan demikian pada reaksi endoterm besarnya nilai perubahan entalpi bertanda positif. (+)

11
Multiple Choice
Berikut di bawah ini yang bukan merupakan peristiwa endoterm adalah ....
Proses pencairan es batu
Pernafasan
Fotosintesis
Proses penjemuran baju
Proses memasak
12
Apa jawaban kamu sudah tepat?
Reaksi endoterm merupakan reaksi yang terjadi dengan menyerap kalor dari lingkungan.
Bernafas bukan termasuk reaksi endoterm karena tidak menyerap panas, melainkan menghasilkan panas, coba saja kalian rasakan nafas yang kalian hembuskan.

13
Selanjutnya,
mengenai
Persamaan Reaksi Termokimia
14
Persamaan Termokimia
Persamaan reaksi termokimia adalah
Suatu persamaan reaksi kimia yang diikuti dengan nilai perubahan entalpi yang menyertai reaksi tersebut
Sebagai contoh : 2 H2 (g) + O2 (g) ⟶ 2 H2O (g) 𝛥H = – 489,6 kJ
Pada reaksi kimia ini diikuti dengan nilai perubahan entalpi nya. (𝛥H )
15
Persamaan Termokimia
Perhatikan reaksi termokimia ini:
2 H2 (g) + O2 (g) ⟶ 2 H2O (g) 𝛥H = – 489,6 kJ
Dari persamaan termokimia di atas dapat disimpulkan bahwa dalam pembentukan 2 mol uap air (H2O) akan disertai pelepasan energi sebesar 489,6 kJ.
Tanda negatif pada nilai 𝛥H persamaan termokimia di atas bukan menunjukan nilai sebenarnya, tetapi menunjukan bahwa pada reaksi tersebut terjadi pelepasan kalor atau bersifat eksoterm.
16
Nahhh mari kita kuis dulu, untuk menguji apakah kalian sudah memahami mengenai persamaan reaksi termokimia
17
Multiple Choice
Perhatikan data berikut :
Reaksi I : C3H8 + 5 O2 ⟶ 3 CO2 + 4 H2O ΔH = – P kJ
Reaksi II : NH4Cl + NaOH ⟶ NH3 + NaCl ΔH = + Q kJ
Pernyataan yang benar dari data tersebut adalah ....
Reaksi I : sistem melepas kalor dilihat dari tanda negatif termasuk reaksi eksoterm
Reaksi II : sistem menyerap kalor dilihat dari tanda positif termasuk reaksi eksoterm
Reaksi II : sistem lingkungan melepas kalor dilihat dari tanda positif termasuk reaksi eksoterm
Reaksi I : lingkungan menyerap kalor dilihat dari tanda negatif termasuk, reaksi endoterm
18
Sudah benar jawaban kalian ?
Reaksi I : C3H8 + 5 O2 --> 3 CO2 + 4 H2O 𝛥H = - P kJ
Ini termasuk reaksi eksoterm, lihat nilai 𝛥H nya adalah - , yang berarti sistem melepas kalor .
Reaksi II : NH4Cl + NaOH --> NH3 + NaCl 𝛥H = + Q kJ
Ini termasuk reaksi endoterm, lihat nilai 𝛥H nya adalah + , yang berarti sistem menyerap kalor .
19
Siapkan buku latihan kalian, mari kita koreksi bersama tugas yang sudah kalian kerjakan
20
Di dalam gelas kimia direaksikan amonium klorida dengan barium hidroksida padat, sehingga dihasilkan barium klorida, air dan gas amonia. Pada reaksi ternyata suhu sistem turun dari 25o menjadi 12o C.
a. Tunjukkan yang menjadi sistem dan lingkungan
b. Tentukan jenis reaksinya
Jawab:
a. Sistem : amonium klorida dengan barium hidroksida padat, barium klorida, air dan gas amonia.
Lingkungan: gelas dan udara di sekitar
b. Jenis reaksinya eksoterm karena nilai entalpi akhir reaksi menjadi lebih kecil dibanding entalpi awal sebelum reaksi atau terjadi penurunan suhu.
21
Jika diketahui : N2 (g) + 3 H2 (g) --> 2 NH3 (g) ΔH = - 92 kJ. Perubahan entalpi pembentukan 1 mol gas NH3 adalah ... .
Pada reaksi tersebut merupakan pembentukan 2 mol NH3, 2 mol terlihat dari koefisien NH3 pada persamaan reaksi adalah 2
lalu yang ditanyakan hanya pembentukan 1 mol, maka reaksi serta nilai 𝛥H-nya juga harus disesuaikan dengan dibagi menjadi 2.
maka nilai
22
Multiple Choice
Tuliskan persamaan termokimia untuk pembentukan 1 mol uap air bila diketahui reaksi sebagai berikut: 2 H2 (g) + O2 (g) ⟶ 2 H2O (g) 𝛥H = – 489,6 kJ
2 H2 (g) + O2 (g) ⟶ H2O (g) 𝛥H = – 489,6 kJ
H2 (g) + 21 O2 (g) ⟶ H2O (g) 𝛥H = – 242,8 kJ
23
SEKIAN PEMBELAJARAN KALI INI
by Ibu Sintya
Show answer
Auto Play
Slide 1 / 23
SLIDE
Similar Resources on Wayground

16 questions
Teori konflik
Presentation
•
11th Grade

21 questions
PERSAMAAN LAJU REAKSI
Presentation
•
11th Grade

14 questions
Koloid
Presentation
•
11th Grade

19 questions
Tata Surya dan Luar Angkasa
Presentation
•
KG

17 questions
Pengertian Laju Reaksi
Presentation
•
11th Grade

20 questions
Kesetimbangan Kimia A1.P1
Presentation
•
11th Grade

15 questions
Termokimia
Presentation
•
11th Grade

14 questions
Kolonialisme Barat di Indonesia
Presentation
•
11th Grade
Popular Resources on Wayground

15 questions
Grade 3 Simulation Assessment 1
Quiz
•
3rd Grade

22 questions
HCS Grade 4 Simulation Assessment_1 2526sy
Quiz
•
4th Grade

16 questions
Grade 3 Simulation Assessment 2
Quiz
•
3rd Grade

19 questions
HCS Grade 5 Simulation Assessment_1 2526sy
Quiz
•
5th Grade

17 questions
HCS Grade 4 Simulation Assessment_2 2526sy
Quiz
•
4th Grade

20 questions
Equivalent Fractions
Quiz
•
3rd Grade

24 questions
HCS Grade 5 Simulation Assessment_2 2526sy
Quiz
•
5th Grade

20 questions
Math Review
Quiz
•
3rd Grade
Discover more resources for Chemistry

20 questions
Types of Chemical Reactions
Quiz
•
9th - 12th Grade

20 questions
Redox Reactions
Quiz
•
10th - 12th Grade

20 questions
pH and pOH Calculations
Quiz
•
10th - 11th Grade

36 questions
Unit 4 (Part 2) Solutions
Quiz
•
10th - 12th Grade

30 questions
Final Exam Prep S22: 2.1.A.1 Isotopes
Quiz
•
9th - 12th Grade

25 questions
Stoichiometry Mass to Mass
Quiz
•
10th - 11th Grade

15 questions
Calculating pH and pOH
Quiz
•
10th - 12th Grade

15 questions
Balancing Chemical Equations
Quiz
•
10th - 12th Grade