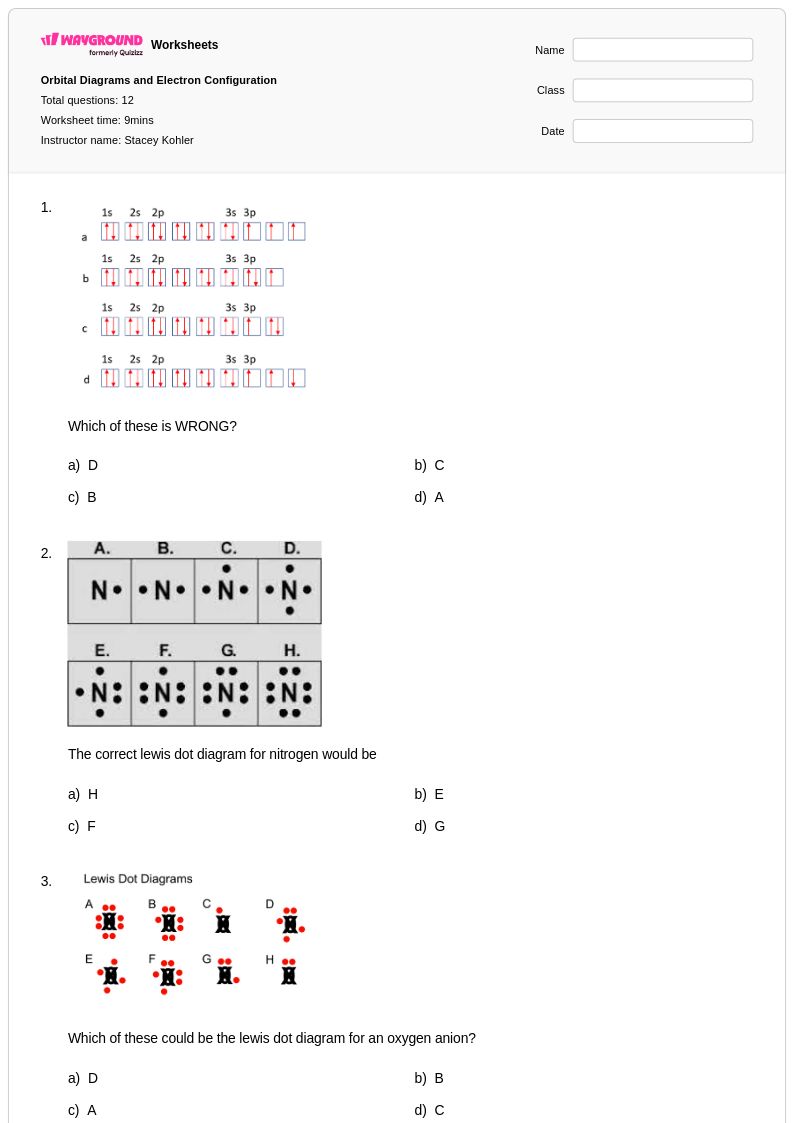
Orbital Diagrams and Electron Configuration

Orbital Diagrams Rules and Principles

Energy Levels, Sublevels, and Atomic Orbitals

Electron Configuration

Orbital Diagram Practice

Quantum Numbers and Electron Configurations

Atomic Structure and Models Quiz
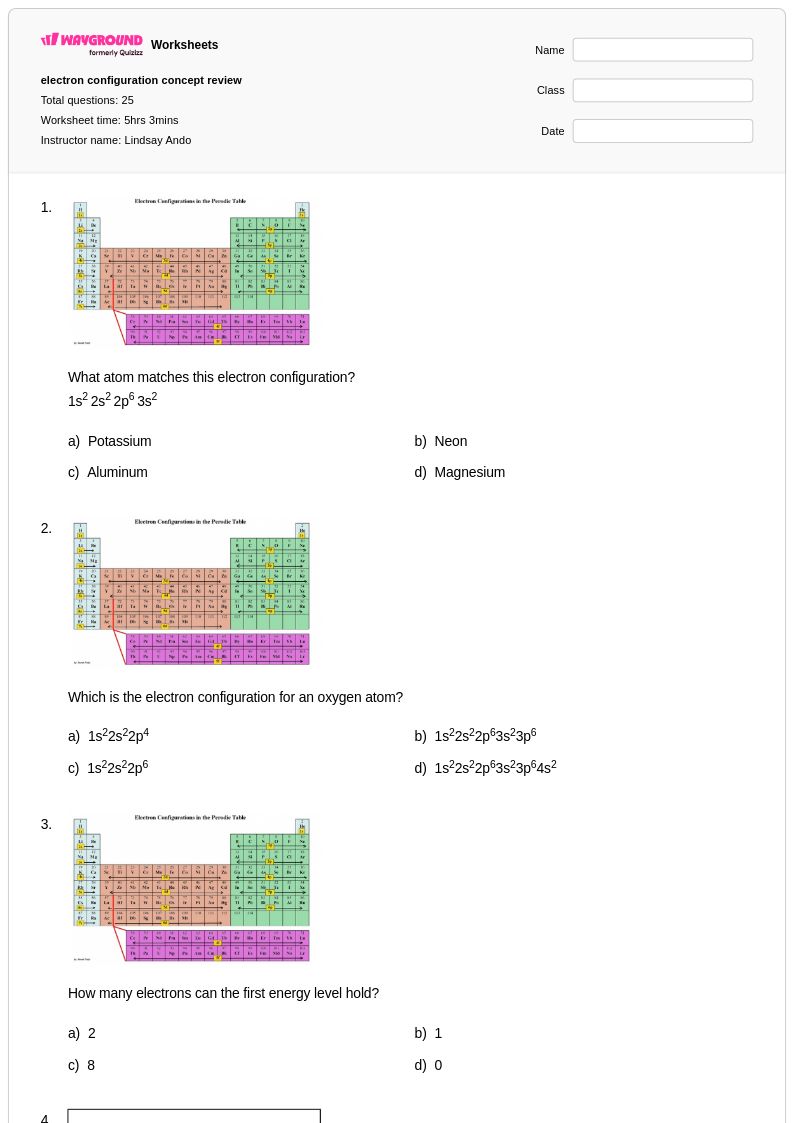
electron configuration concept review

Electron Configuration & Groups on the Periodic table

Unit 2 Test Practice (Atomic Theory)

4.3 Electron Configuration

1.5 - Electron Configuration

Unit 7 (The Atom) Quiz Review

Chemistry Fourth Quarter Extra Credit
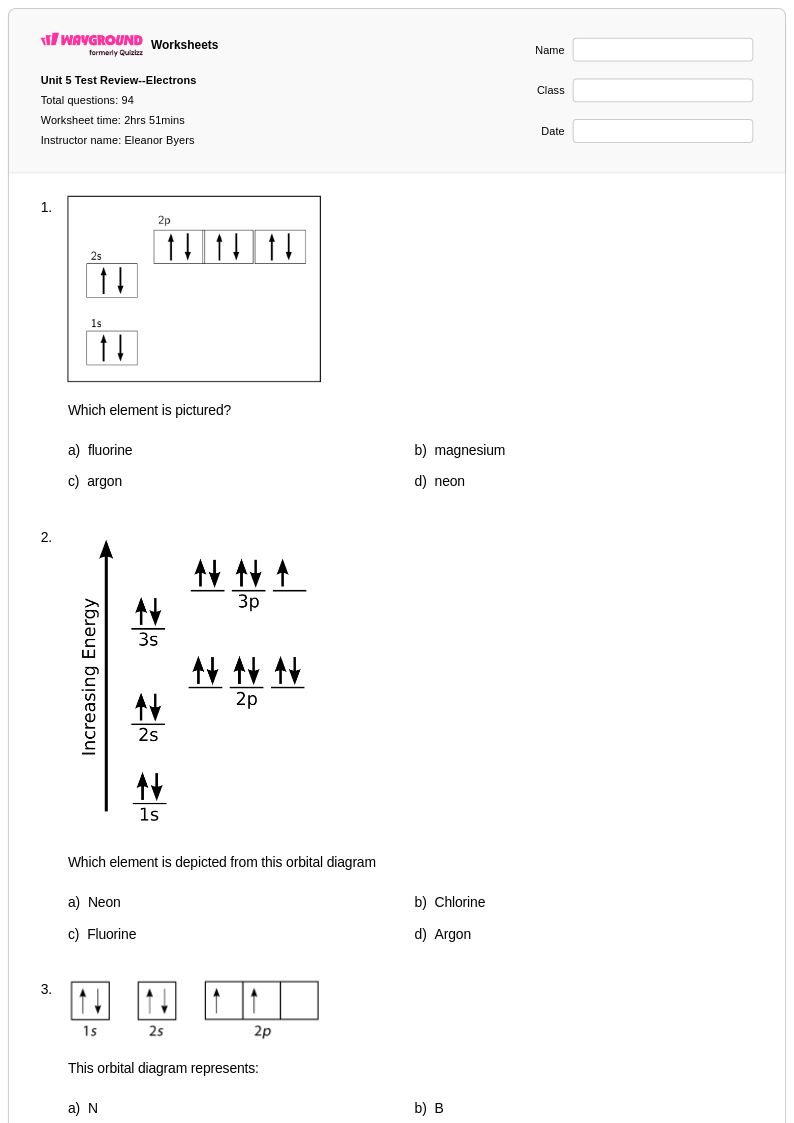
Unit 5 Test Review--Electrons

Modern Atomic Theory Quiz
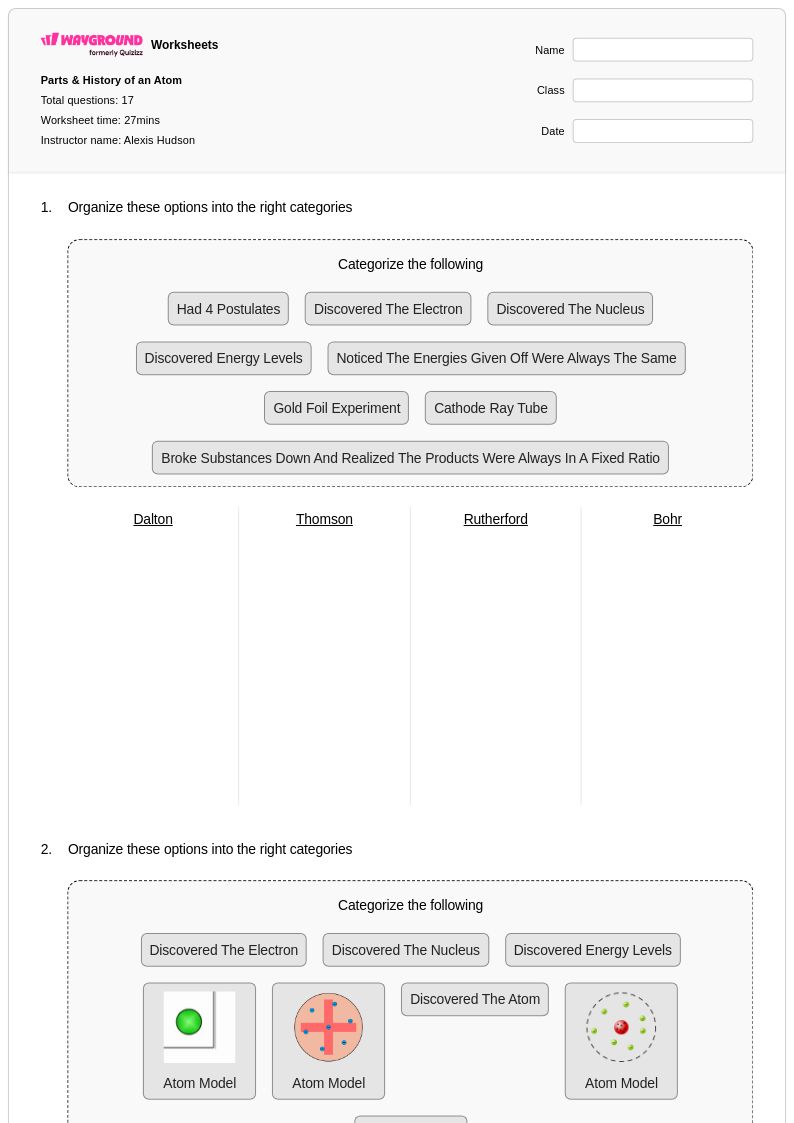
Parts & History of an Atom
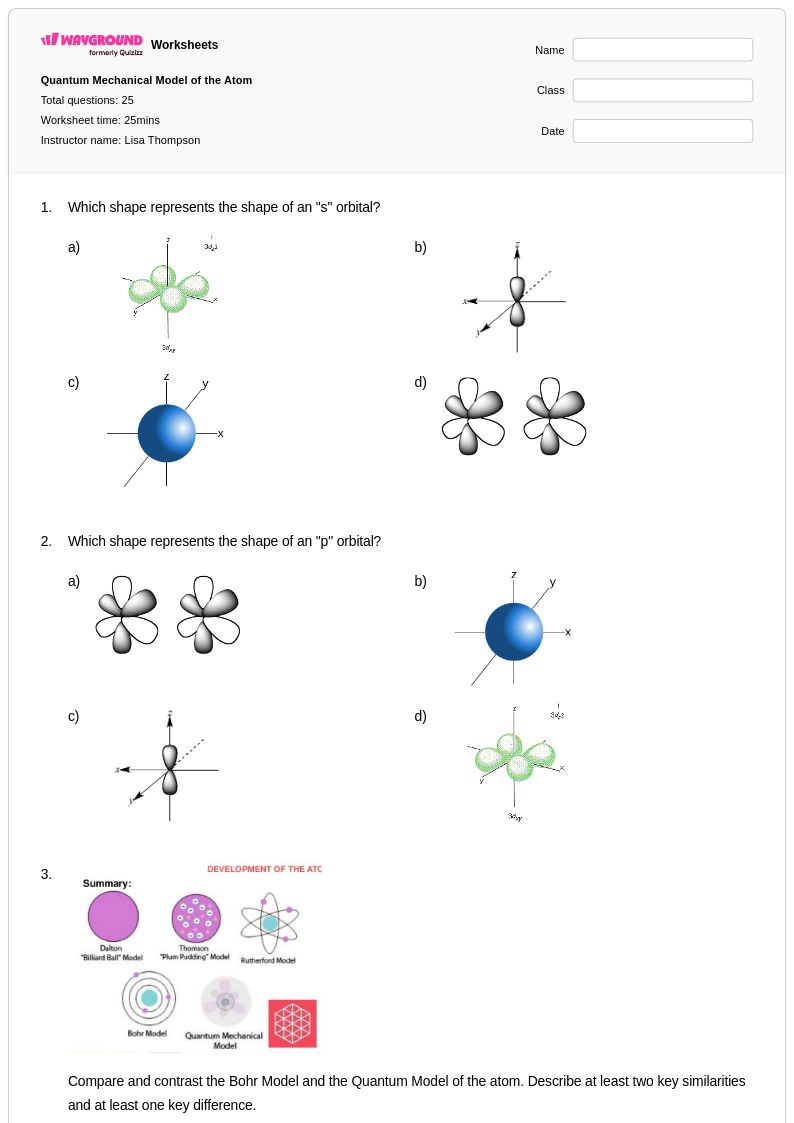
Quantum Mechanical Model of the Atom

The Periodic Table

Periodic Table Review Questions

Periodic Table Test Review

Atomic Structure
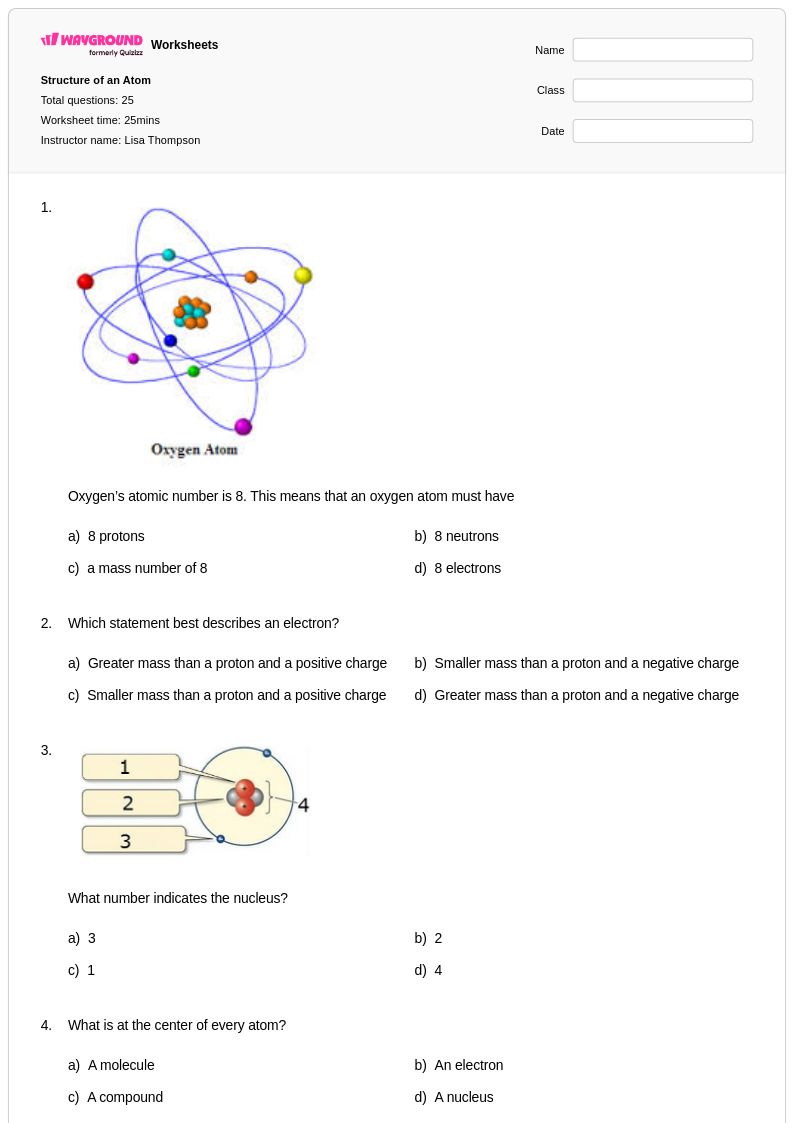
Structure of an Atom

Chemistry Q2 Review
Explore แผนภาพวงโคจรอะตอม Worksheets by Grades
Explore Other Subject Worksheets for ระดับ 10
สำรวจแผ่นงาน แผนภาพวงโคจรอะตอม ที่พิมพ์ได้สำหรับ ชั้นประถมศึกษาปีที่ 10
แผนภาพวงโคจรอะตอมเป็นพื้นฐานสำคัญในวิชาเคมีระดับชั้นมัธยมศึกษาปีที่ 4 ช่วยให้นักเรียนเห็นภาพการจัดเรียงอิเล็กตรอนภายในอะตอมและเข้าใจแบบจำลองกลศาสตร์ควอนตัมของโครงสร้างอะตอม ชุดแบบฝึกหัดแผนภาพวงโคจรอะตอมที่ครอบคลุมของ Wayground ช่วยให้นักเรียนได้ฝึกฝนอย่างเป็นระบบในการวาดและตีความวงโคจร s, p, d และ f การกำหนดการจัดเรียงอิเล็กตรอน และการประยุกต์ใช้กฎของฮุนด์และหลักการกีดกันของเปาลี แบบฝึกหัดเหล่านี้มีโจทย์ฝึกฝนอย่างเป็นระบบที่แนะนำนักเรียนเกี่ยวกับลำดับการเติมวงโคจร สัญลักษณ์สปินของอิเล็กตรอน และความสัมพันธ์ระหว่างรูปร่างวงโคจรและการกระจายความน่าจะเป็นของอิเล็กตรอน แบบฝึกหัดแต่ละแผ่นมีเฉลยโดยละเอียดที่อธิบายเหตุผลเบื้องหลังการจัดเรียงวงโคจร ทำให้แหล่งข้อมูลฟรีเหล่านี้มีค่าอย่างยิ่งสำหรับการเรียนการสอนในห้องเรียนและการศึกษาด้วยตนเองในขณะที่นักเรียนเชี่ยวชาญแนวคิดทางเคมีที่ซับซ้อนแต่สำคัญนี้
คลังแบบฝึกหัดแผนภาพวงโคจรอะตอมที่สร้างโดยครูผู้สอนจำนวนมากของ Wayground ช่วยให้ผู้สอนมีความยืดหยุ่นอย่างเหนือชั้นในการสอนหัวข้อเคมีระดับชั้นมัธยมศึกษาปีที่ 4 ที่ท้าทายนี้ ด้วยทรัพยากรนับล้านที่พร้อมใช้งาน ครูสามารถค้นหาและคัดกรองสื่อได้อย่างง่ายดาย เพื่อค้นหาแบบฝึกหัดที่สอดคล้องกับมาตรฐานหลักสูตรเฉพาะ และเหมาะสมกับระดับความสามารถที่แตกต่างกันของนักเรียน เครื่องมือการปรับระดับความยากง่ายของแพลตฟอร์มช่วยให้ผู้สอนสามารถปรับแต่งแบบฝึกหัดเพื่อการแก้ไขหรือเสริมความรู้ ในขณะที่รูปแบบไฟล์ PDF ที่พิมพ์ได้และเวอร์ชันดิจิทัลช่วยรองรับสภาพแวดล้อมในห้องเรียนและวิธีการเรียนรู้ที่หลากหลาย คุณสมบัติเหล่านี้ช่วยให้การวางแผนบทเรียนง่ายขึ้น โดยการจัดเตรียมสื่อที่พร้อมใช้งาน ซึ่งสามารถบูรณาการเข้ากับการเรียนรู้ในหน่วยโครงสร้างอะตอม การจัดเรียงอิเล็กตรอน และพันธะเคมีได้อย่างราบรื่น ทำให้มั่นใจได้ว่านักเรียนจะได้รับการฝึกฝนทักษะที่จำเป็นต่อความเป็นเลิศในแนวคิดทางเคมีขั้นสูง
FAQs
ฉันจะสอนแผนภาพวงโคจรอะตอมให้แก่นักเรียนวิชาเคมีได้อย่างไร?
เริ่มต้นด้วยการอธิบายกฎหลักสามข้อที่ควบคุมการจัดเรียงอิเล็กตรอนให้แก่นักเรียน ได้แก่ หลักการเอาฟ์บาว (เติมออร์บิทัลที่มีพลังงานต่ำที่สุดก่อน) หลักการกีดกันของเปาลี (อิเล็กตรอนสองตัวจะไม่ใช้เลขควอนตัมสี่ตัวเดียวกัน) และกฎของฮุนด์ (เพิ่มจำนวนอิเล็กตรอนที่ไม่จับคู่ภายในซับเชลล์ให้มากที่สุดก่อนที่จะจับคู่) เริ่มจากอะตอมอย่างง่าย เช่น ไฮโดรเจนและฮีเลียม ก่อนที่จะไปยังอะตอมที่มีอิเล็กตรอนหลายตัว โดยใช้แผนภาพที่มีลูกศรเพื่อแสดงทิศทางการหมุน การเชื่อมโยงสัญลักษณ์ออร์บิทัลเข้ากับสัญลักษณ์การจัดเรียงอิเล็กตรอนอย่างชัดเจนจะช่วยให้นักเรียนเห็นว่าทั้งสองแบบอธิบายโครงสร้างพื้นฐานเดียวกัน
แบบฝึกหัดใดบ้างที่ช่วยให้นักเรียนฝึกฝนการวาดแผนภาพวงโคจร?
การฝึกฝนที่มีประสิทธิภาพเริ่มต้นด้วยแผนภาพซับเชลล์เดี่ยวสำหรับธาตุในคาบที่ 1 และ 2 จากนั้นค่อยๆ แนะนำการเติมซับเชลล์ d สำหรับโลหะทรานซิชัน ซึ่งเป็นบริเวณที่มักเกิดข้อผิดพลาดบ่อยครั้ง แบบฝึกหัดที่ให้นักเรียนแปลงระหว่างสัญลักษณ์ออร์บิทัลและสัญลักษณ์การจัดเรียงอิเล็กตรอนจะช่วยเสริมความเข้าใจทั้งสองรูปแบบไปพร้อมๆ กัน การรวมปัญหาที่ต้องการให้นักเรียนระบุจำนวนอิเล็กตรอนที่ไม่มีคู่จากแผนภาพที่สมบูรณ์จะเพิ่มชั้นการประยุกต์ใช้ที่ช่วยให้เข้าใจแนวคิดได้ลึกซึ้งยิ่งขึ้น
นักเรียนมักทำผิดพลาดอะไรบ้างเมื่อวาดแผนภาพวงโคจรอะตอม?
ข้อผิดพลาดที่พบบ่อยที่สุดคือการละเมิดกฎของฮุนด์โดยการจับคู่อิเล็กตรอนในซับเชลล์ก่อนที่ออร์บิทัลทั้งหมดในซับเชลล์นั้นจะมีอิเล็กตรอนเพียงตัวเดียว นักเรียนมักเรียงลำดับระดับพลังงานของออร์บิทัลผิดพลาด โดยเฉพาะอย่างยิ่งการวาง 4s ไว้เหนือ 3d แทนที่จะอยู่ด้านล่างเมื่อทำการเติมอิเล็กตรอน ความเข้าใจผิดที่พบบ่อยประการที่สามคือการใช้แผนภาพออร์บิทัลแทนสัญลักษณ์การจัดเรียงอิเล็กตรอน โดยไม่ตระหนักว่าแผนภาพออร์บิทัลนั้นมีข้อมูลเพิ่มเติมเกี่ยวกับสปินของอิเล็กตรอนและการครอบครองซับเชลล์
ฉันจะใช้แบบฝึกหัดแผนภาพวงโคจรอะตอมในห้องเรียนได้อย่างไร?
แบบฝึกหัดแผนภาพวงโคจรอะตอมบน Wayground มีให้เลือกทั้งแบบไฟล์ PDF ที่สามารถพิมพ์ได้สำหรับการใช้งานในห้องเรียนแบบดั้งเดิม และแบบดิจิทัลสำหรับสภาพแวดล้อมที่บูรณาการเทคโนโลยี รวมถึงตัวเลือกในการจัดทำเป็นแบบทดสอบโดยตรงบน Wayground เวอร์ชันที่พิมพ์ได้เหมาะสำหรับการจดบันทึกประกอบการเรียนหรือการฝึกฝนแบบห้องปฏิบัติการ ในขณะที่รูปแบบดิจิทัลช่วยให้ครูสามารถมอบหมายงานแบบไม่พร้อมกันหรือติดตามการตอบสนองของนักเรียนได้แบบเรียลไทม์ แบบฝึกหัดแต่ละชุดมีเฉลยคำตอบโดยละเอียด ทำให้มีประโยชน์อย่างยิ่งสำหรับการฝึกฝนของนักเรียนด้วยตนเอง กิจกรรมการทบทวนโดยเพื่อน หรือการแก้ไขปัญหาเฉพาะด้าน
ฉันจะปรับวิธีการสอนเรื่องแผนภาพวงโคจรอะตอมให้เหมาะสมกับนักเรียนที่มีระดับความสามารถแตกต่างกันได้อย่างไร?
สำหรับนักเรียนที่ต้องการความช่วยเหลือเพิ่มเติม ให้ลดความซับซ้อนของอะตอมที่กำหนด และใช้แผนภาพที่สร้างเสร็จบางส่วนเป็นโครงร่างก่อนที่จะกำหนดให้สร้างแผนภาพด้วยตนเอง ใน Wayground ครูสามารถปรับการสอนเป็นรายบุคคลได้ เช่น การอ่านออกเสียงข้อความคำถาม หรือลดตัวเลือกคำตอบ เพื่อลดภาระทางความคิดสำหรับนักเรียนบางคน โดยไม่ส่งผลกระทบต่อประสบการณ์ของนักเรียนคนอื่นๆ ในชั้นเรียน นักเรียนที่มีความสามารถสูงสามารถได้รับความท้าทายเกี่ยวกับโครงสร้างอะตอมของโลหะทรานซิชัน และข้อยกเว้น เช่น โครเมียมและทองแดง ซึ่งรูปแบบการเติมแบบ aufbau ที่คาดไว้ไม่สามารถนำมาใช้ได้
เลขควอนตัมมีความสัมพันธ์กับแผนภาพวงโคจรอะตอมอย่างไร?
แต่ละออร์บิทัลในแผนภาพจะสอดคล้องกับชุดเลขควอนตัมที่ไม่ซ้ำกัน: เลขควอนตัมหลัก (n) กำหนดระดับพลังงาน เลขควอนตัมโมเมนตัมเชิงมุม (l) กำหนดรูปร่างของซับเชลล์ เลขควอนตัมแม่เหล็ก (ml) ระบุออร์บิทัลเฉพาะภายในซับเชลล์ และเลขควอนตัมสปิน (ms) แยกแยะอิเล็กตรอนสองตัวที่สามารถครอบครองออร์บิทัลเดียวได้ แผนภาพออร์บิทัลทำให้กรอบนามธรรมนี้เป็นรูปธรรมโดยการแสดงค่า ml ที่อนุญาตแต่ละค่าเป็นกล่อง และค่า ms ของอิเล็กตรอนแต่ละตัวเป็นลูกศรขึ้นหรือลง การเชื่อมโยงนี้ช่วยให้นักเรียนเข้าใจว่าทำไม ตัวอย่างเช่น ซับเชลล์ p จึงมีกล่องสามกล่องพอดีและสามารถบรรจุอิเล็กตรอนได้สูงสุดหกตัว
























