
Electron Configurations and Orbital Diagrams

Orbital Diagrams Rules and Principles

Energy Levels, Sublevels, and Atomic Orbitals

Electron Configuration and Quantum Numbers Review

Electron Configuration

Unit 6 Review
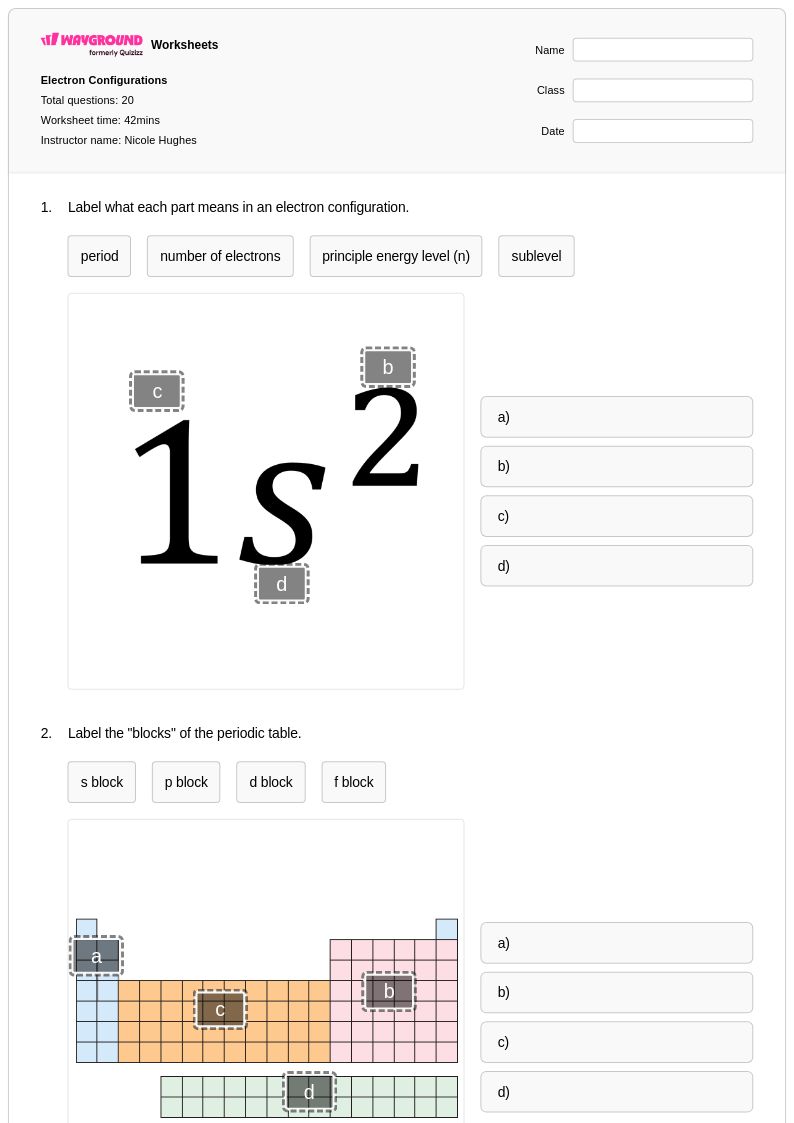
Electron Configurations

Orbital Diagram Practice

Quantum Numbers and Electron Configurations

Atomic Structure and Models Quiz
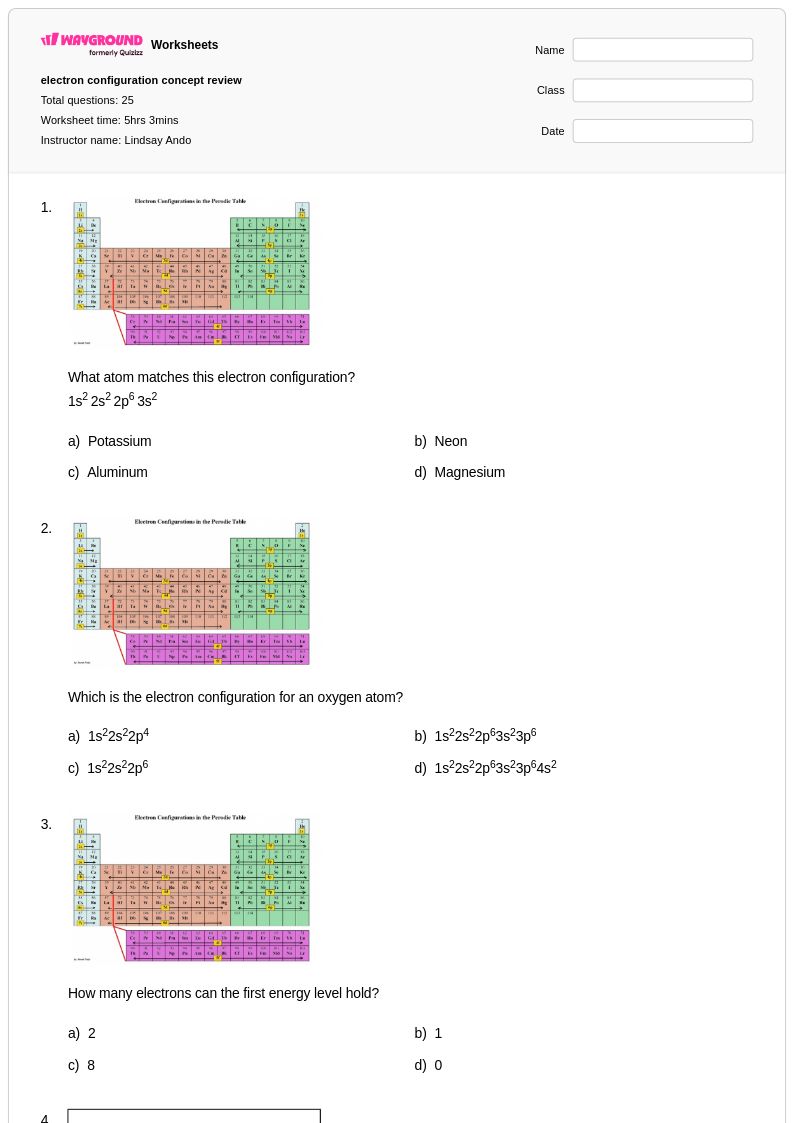
electron configuration concept review

Modern Atomic Theory

Topic Test: Atomic Structure and Chemical Bonding

Electron Configuration Practice

Quantum Mechanical Model & Orbitals
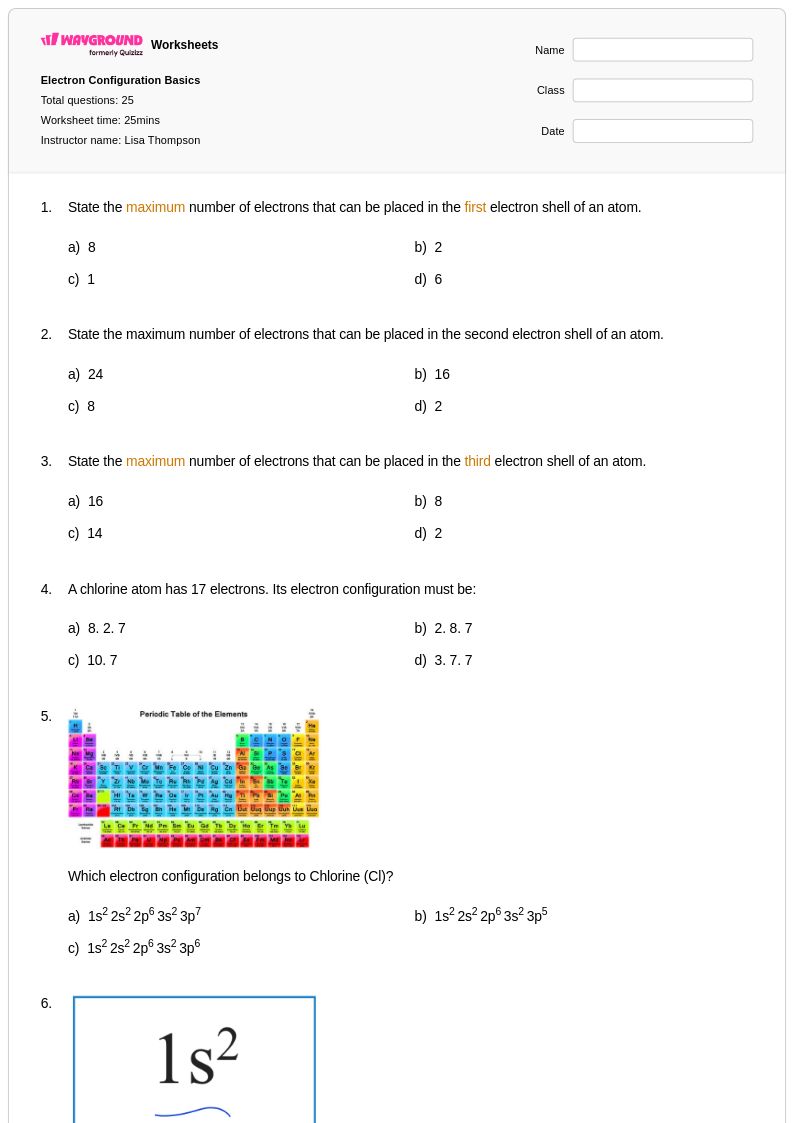
Electron Configuration Basics

24Unit 1: Atoms & Chemical Bonding/Reactions STUDY GUIDE

Chemistry Fourth Quarter Extra Credit
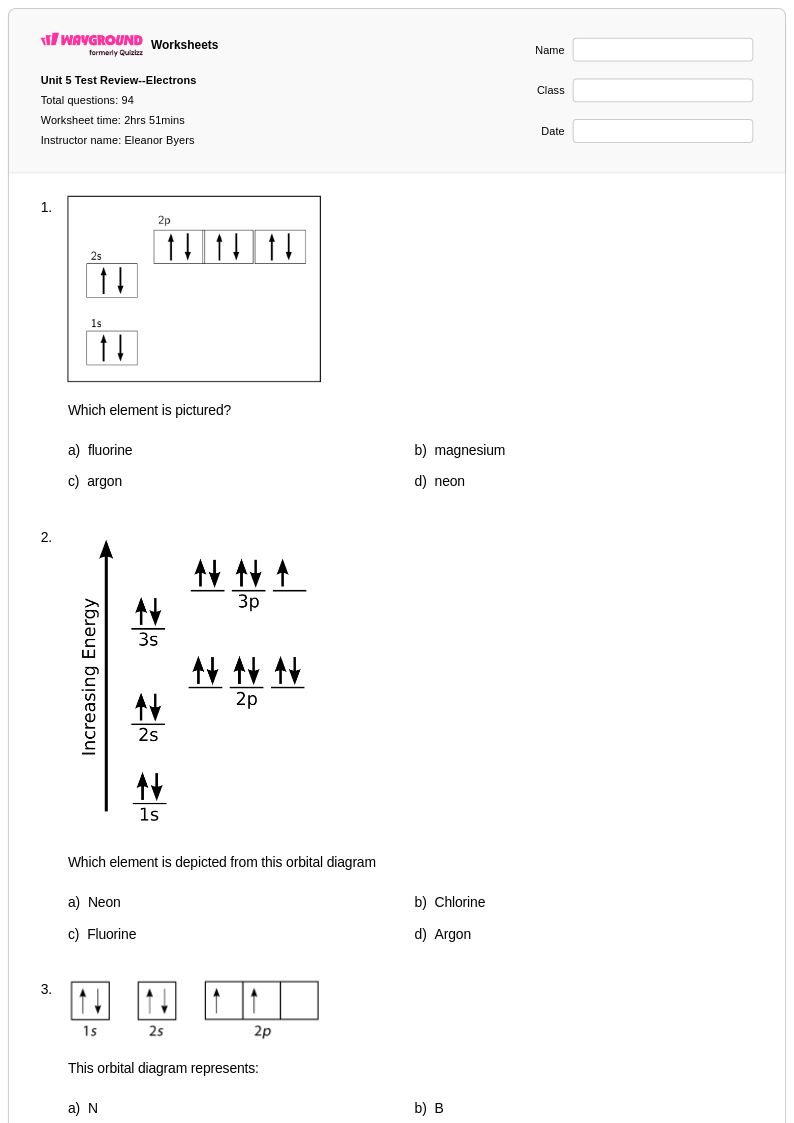
Unit 5 Test Review--Electrons
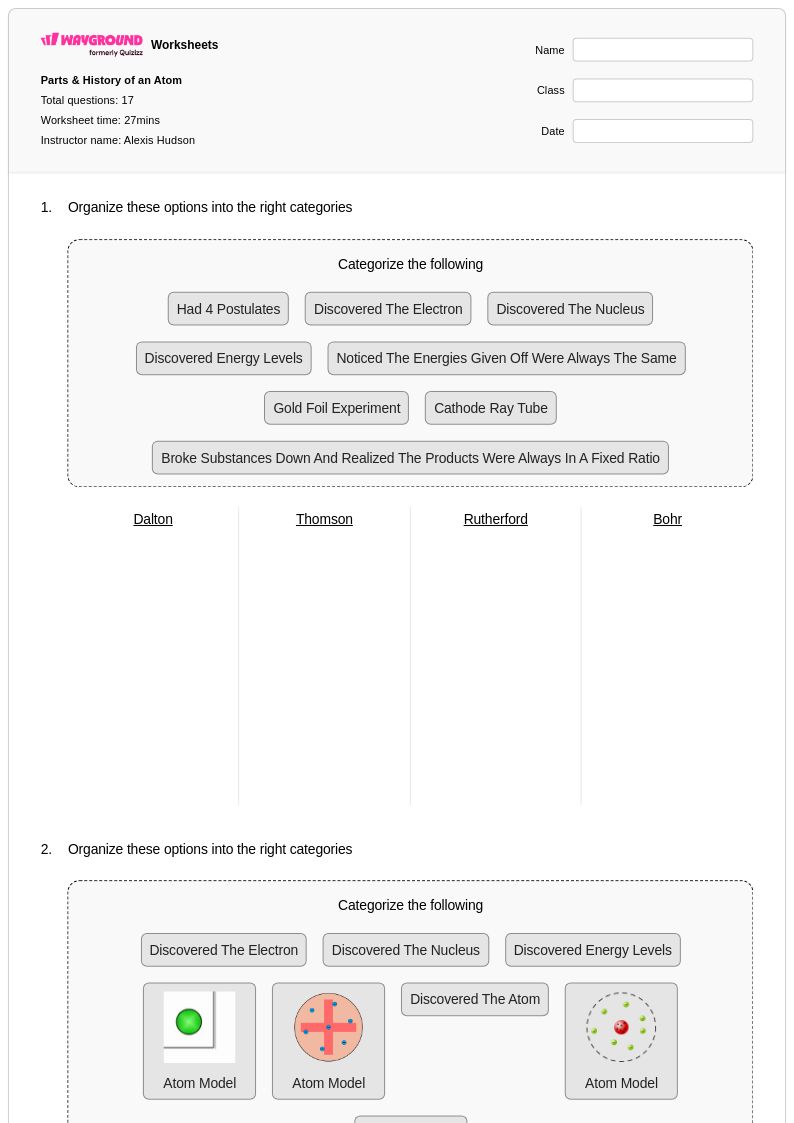
Parts & History of an Atom
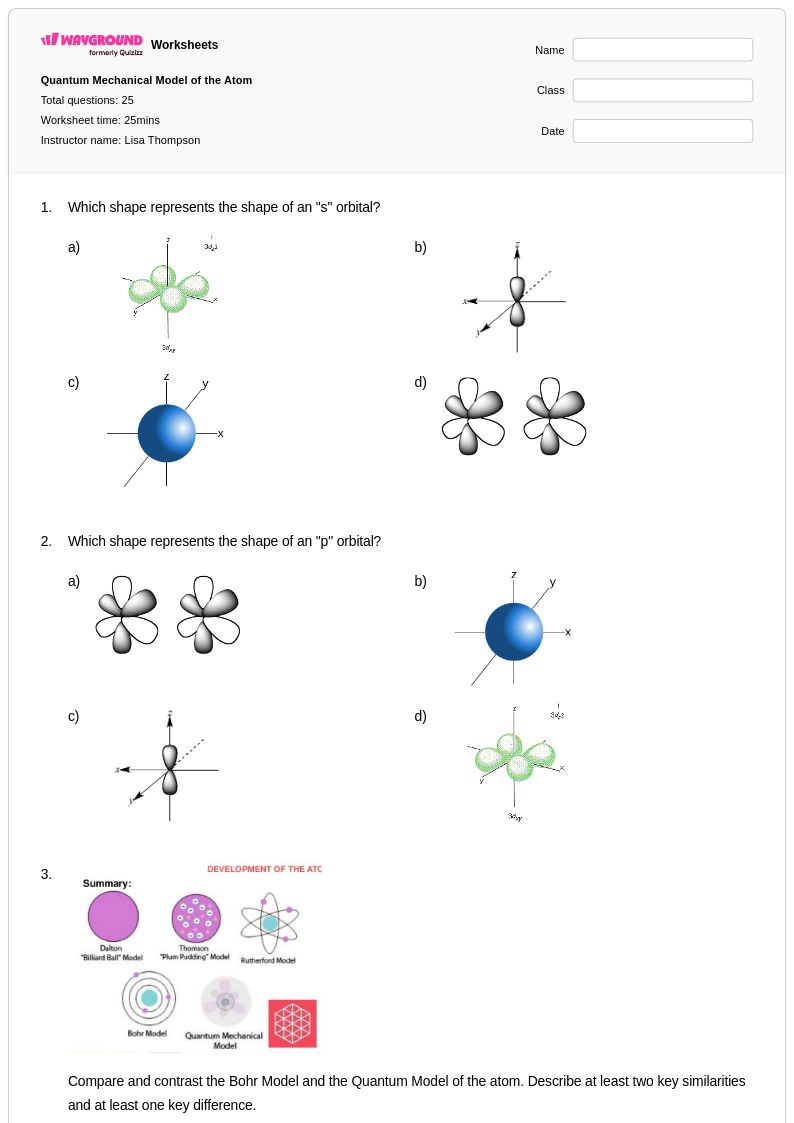
Quantum Mechanical Model of the Atom

Periodic Table Review Questions

Atomic Structure
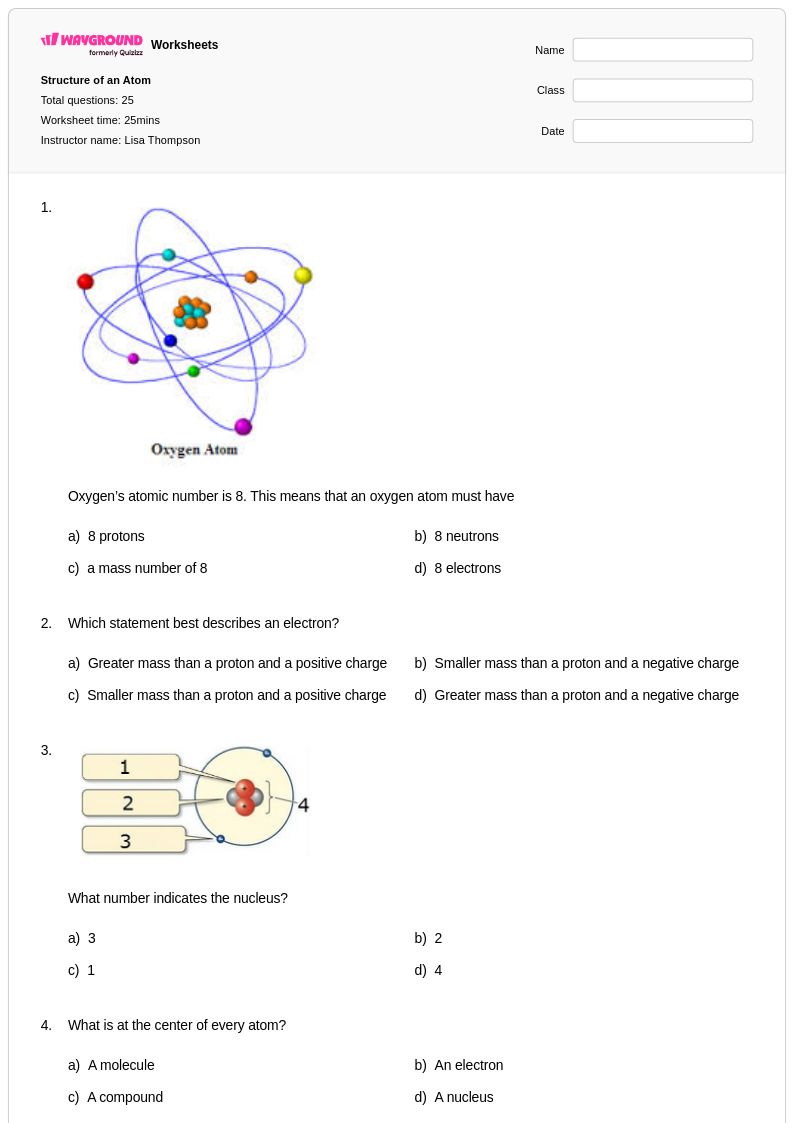
Structure of an Atom
Khám phá แผนภาพวงโคจรอะตอม Bảng tính theo cấp độ
Khám phá các bảng tính chủ đề khác cho ระดับ 11
สำรวจแผ่นงาน แผนภาพวงโคจรอะตอม ที่พิมพ์ได้สำหรับ ชั้นประถมศึกษาปีที่ 11
แบบฝึกหัดแผนภาพวงโคจรอะตอมสำหรับนักเรียนชั้นมัธยมศึกษาปีที่ 4 (เกรด 11) จาก Wayground (เดิมคือ Quizizz) ให้แบบฝึกหัดที่ครอบคลุมในการมองเห็นและทำความเข้าใจการจัดเรียงอิเล็กตรอนภายในอะตอม แบบฝึกหัดที่ออกแบบมาอย่างเชี่ยวชาญเหล่านี้ช่วยเสริมสร้างทักษะที่สำคัญในพื้นฐานกลศาสตร์ควอนตัม รวมถึงการระบุรูปร่างวงโคจร s, p, d และ f การกำหนดทิศทางการหมุนของอิเล็กตรอน และการประยุกต์ใช้กฎของฮุนด์และหลักการเอาฟ์เบา นักเรียนจะได้ฝึกฝนผ่านโจทย์ปัญหาอย่างเป็นระบบซึ่งช่วยเสริมสร้างความสามารถในการสร้างแผนภาพวงโคจรที่ถูกต้องสำหรับธาตุต่างๆ ทั่วตารางธาตุ ในขณะที่รูปแบบ PDF ที่พิมพ์ได้และเฉลยคำตอบที่สมบูรณ์ช่วยให้การเรียนรู้และการประเมินตนเองมีประสิทธิภาพ แหล่งข้อมูลฟรีเหล่านี้ครอบคลุมแนวคิดที่สำคัญตั้งแต่ระนาบวงโคจรของไฮโดรเจนอย่างง่ายไปจนถึงการจัดเรียงอิเล็กตรอนในโลหะทรานซิชันที่ซับซ้อน ช่วยให้นักเรียนเข้าใจความสัมพันธ์เชิงพื้นที่ระหว่างอิเล็กตรอนและระดับพลังงานของพวกมัน
Wayground (เดิมคือ Quizizz) ช่วยเสริมศักยภาพให้แก่ครูผู้สอนด้วยแหล่งข้อมูลแผนภาพวงโคจรอะตอมที่สร้างโดยครูหลายล้านรายการ ซึ่งสนับสนุนความต้องการและวัตถุประสงค์การเรียนรู้ที่หลากหลายในห้องเรียน แพลตฟอร์มนี้มีฟังก์ชันการค้นหาและการกรองที่ทรงประสิทธิภาพ ช่วยให้ครูสามารถค้นหาแบบฝึกหัดที่สอดคล้องกับมาตรฐานวิชาเคมีและหลักสูตรชั้นมัธยมศึกษาปีที่ 4 ได้อย่างรวดเร็ว ในขณะที่เครื่องมือการปรับระดับความยากง่ายช่วยให้สามารถสร้างเนื้อหาที่ปรับแต่งได้เพื่อตอบสนองระดับทักษะที่แตกต่างกันของนักเรียน ครูสามารถเข้าถึงทั้งรูปแบบที่พิมพ์ได้และรูปแบบดิจิทัลได้อย่างราบรื่น รวมถึงไฟล์ PDF ที่ดาวน์โหลดได้ ทำให้การวางแผนบทเรียนมีประสิทธิภาพมากขึ้น ไม่ว่าจะเป็นการสอนในห้องเรียนหรือการสอนทางไกล ชุดแบบฝึกหัดที่หลากหลายเหล่านี้ตอบสนองวัตถุประสงค์ทางการสอนหลายประการ ตั้งแต่การแนะนำทักษะเบื้องต้นและการฝึกฝนแบบมีผู้แนะนำ ไปจนถึงการแก้ไขปัญหาเฉพาะสำหรับนักเรียนที่ประสบปัญหา และกิจกรรมเสริมสำหรับผู้เรียนที่มีความสามารถสูง ซึ่งท้ายที่สุดแล้วจะช่วยสนับสนุนการเรียนรู้หลักการจัดเรียงอิเล็กตรอนอย่างครอบคลุม
FAQs
ฉันจะสอนแผนภาพวงโคจรอะตอมให้แก่นักเรียนวิชาเคมีได้อย่างไร?
เริ่มต้นด้วยการอธิบายกฎหลักสามข้อที่ควบคุมการจัดเรียงอิเล็กตรอนให้แก่นักเรียน ได้แก่ หลักการเอาฟ์บาว (เติมออร์บิทัลที่มีพลังงานต่ำที่สุดก่อน) หลักการกีดกันของเปาลี (อิเล็กตรอนสองตัวจะไม่ใช้เลขควอนตัมสี่ตัวเดียวกัน) และกฎของฮุนด์ (เพิ่มจำนวนอิเล็กตรอนที่ไม่จับคู่ภายในซับเชลล์ให้มากที่สุดก่อนที่จะจับคู่) เริ่มจากอะตอมอย่างง่าย เช่น ไฮโดรเจนและฮีเลียม ก่อนที่จะไปยังอะตอมที่มีอิเล็กตรอนหลายตัว โดยใช้แผนภาพที่มีลูกศรเพื่อแสดงทิศทางการหมุน การเชื่อมโยงสัญลักษณ์ออร์บิทัลเข้ากับสัญลักษณ์การจัดเรียงอิเล็กตรอนอย่างชัดเจนจะช่วยให้นักเรียนเห็นว่าทั้งสองแบบอธิบายโครงสร้างพื้นฐานเดียวกัน
แบบฝึกหัดใดบ้างที่ช่วยให้นักเรียนฝึกฝนการวาดแผนภาพวงโคจร?
การฝึกฝนที่มีประสิทธิภาพเริ่มต้นด้วยแผนภาพซับเชลล์เดี่ยวสำหรับธาตุในคาบที่ 1 และ 2 จากนั้นค่อยๆ แนะนำการเติมซับเชลล์ d สำหรับโลหะทรานซิชัน ซึ่งเป็นบริเวณที่มักเกิดข้อผิดพลาดบ่อยครั้ง แบบฝึกหัดที่ให้นักเรียนแปลงระหว่างสัญลักษณ์ออร์บิทัลและสัญลักษณ์การจัดเรียงอิเล็กตรอนจะช่วยเสริมความเข้าใจทั้งสองรูปแบบไปพร้อมๆ กัน การรวมปัญหาที่ต้องการให้นักเรียนระบุจำนวนอิเล็กตรอนที่ไม่มีคู่จากแผนภาพที่สมบูรณ์จะเพิ่มชั้นการประยุกต์ใช้ที่ช่วยให้เข้าใจแนวคิดได้ลึกซึ้งยิ่งขึ้น
นักเรียนมักทำผิดพลาดอะไรบ้างเมื่อวาดแผนภาพวงโคจรอะตอม?
ข้อผิดพลาดที่พบบ่อยที่สุดคือการละเมิดกฎของฮุนด์โดยการจับคู่อิเล็กตรอนในซับเชลล์ก่อนที่ออร์บิทัลทั้งหมดในซับเชลล์นั้นจะมีอิเล็กตรอนเพียงตัวเดียว นักเรียนมักเรียงลำดับระดับพลังงานของออร์บิทัลผิดพลาด โดยเฉพาะอย่างยิ่งการวาง 4s ไว้เหนือ 3d แทนที่จะอยู่ด้านล่างเมื่อทำการเติมอิเล็กตรอน ความเข้าใจผิดที่พบบ่อยประการที่สามคือการใช้แผนภาพออร์บิทัลแทนสัญลักษณ์การจัดเรียงอิเล็กตรอน โดยไม่ตระหนักว่าแผนภาพออร์บิทัลนั้นมีข้อมูลเพิ่มเติมเกี่ยวกับสปินของอิเล็กตรอนและการครอบครองซับเชลล์
ฉันจะใช้แบบฝึกหัดแผนภาพวงโคจรอะตอมในห้องเรียนได้อย่างไร?
แบบฝึกหัดแผนภาพวงโคจรอะตอมบน Wayground มีให้เลือกทั้งแบบไฟล์ PDF ที่สามารถพิมพ์ได้สำหรับการใช้งานในห้องเรียนแบบดั้งเดิม และแบบดิจิทัลสำหรับสภาพแวดล้อมที่บูรณาการเทคโนโลยี รวมถึงตัวเลือกในการจัดทำเป็นแบบทดสอบโดยตรงบน Wayground เวอร์ชันที่พิมพ์ได้เหมาะสำหรับการจดบันทึกประกอบการเรียนหรือการฝึกฝนแบบห้องปฏิบัติการ ในขณะที่รูปแบบดิจิทัลช่วยให้ครูสามารถมอบหมายงานแบบไม่พร้อมกันหรือติดตามการตอบสนองของนักเรียนได้แบบเรียลไทม์ แบบฝึกหัดแต่ละชุดมีเฉลยคำตอบโดยละเอียด ทำให้มีประโยชน์อย่างยิ่งสำหรับการฝึกฝนของนักเรียนด้วยตนเอง กิจกรรมการทบทวนโดยเพื่อน หรือการแก้ไขปัญหาเฉพาะด้าน
ฉันจะปรับวิธีการสอนเรื่องแผนภาพวงโคจรอะตอมให้เหมาะสมกับนักเรียนที่มีระดับความสามารถแตกต่างกันได้อย่างไร?
สำหรับนักเรียนที่ต้องการความช่วยเหลือเพิ่มเติม ให้ลดความซับซ้อนของอะตอมที่กำหนด และใช้แผนภาพที่สร้างเสร็จบางส่วนเป็นโครงร่างก่อนที่จะกำหนดให้สร้างแผนภาพด้วยตนเอง ใน Wayground ครูสามารถปรับการสอนเป็นรายบุคคลได้ เช่น การอ่านออกเสียงข้อความคำถาม หรือลดตัวเลือกคำตอบ เพื่อลดภาระทางความคิดสำหรับนักเรียนบางคน โดยไม่ส่งผลกระทบต่อประสบการณ์ของนักเรียนคนอื่นๆ ในชั้นเรียน นักเรียนที่มีความสามารถสูงสามารถได้รับความท้าทายเกี่ยวกับโครงสร้างอะตอมของโลหะทรานซิชัน และข้อยกเว้น เช่น โครเมียมและทองแดง ซึ่งรูปแบบการเติมแบบ aufbau ที่คาดไว้ไม่สามารถนำมาใช้ได้
เลขควอนตัมมีความสัมพันธ์กับแผนภาพวงโคจรอะตอมอย่างไร?
แต่ละออร์บิทัลในแผนภาพจะสอดคล้องกับชุดเลขควอนตัมที่ไม่ซ้ำกัน: เลขควอนตัมหลัก (n) กำหนดระดับพลังงาน เลขควอนตัมโมเมนตัมเชิงมุม (l) กำหนดรูปร่างของซับเชลล์ เลขควอนตัมแม่เหล็ก (ml) ระบุออร์บิทัลเฉพาะภายในซับเชลล์ และเลขควอนตัมสปิน (ms) แยกแยะอิเล็กตรอนสองตัวที่สามารถครอบครองออร์บิทัลเดียวได้ แผนภาพออร์บิทัลทำให้กรอบนามธรรมนี้เป็นรูปธรรมโดยการแสดงค่า ml ที่อนุญาตแต่ละค่าเป็นกล่อง และค่า ms ของอิเล็กตรอนแต่ละตัวเป็นลูกศรขึ้นหรือลง การเชื่อมโยงนี้ช่วยให้นักเรียนเข้าใจว่าทำไม ตัวอย่างเช่น ซับเชลล์ p จึงมีกล่องสามกล่องพอดีและสามารถบรรจุอิเล็กตรอนได้สูงสุดหกตัว
























