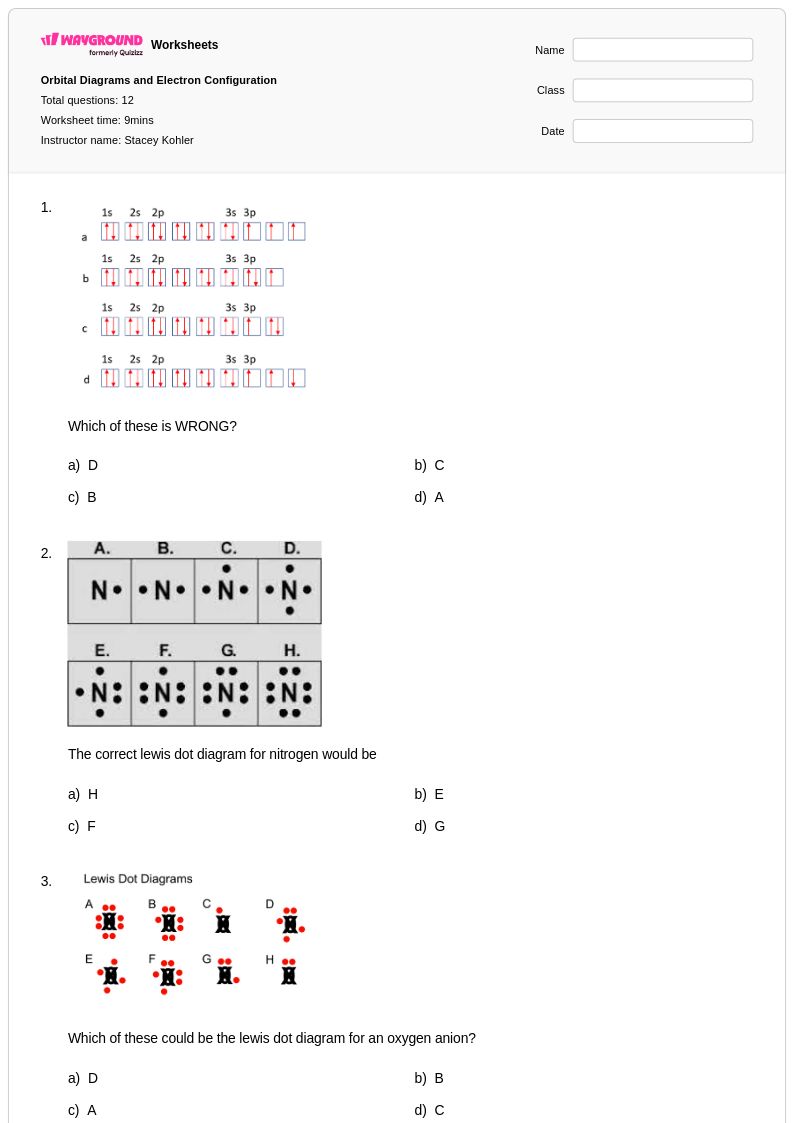
Orbital Diagrams and Electron Configuration

Orbital Diagrams Rules and Principles

Electron Configuration and Quantum Numbers Review

Electron Configuration

Unit 6 Review
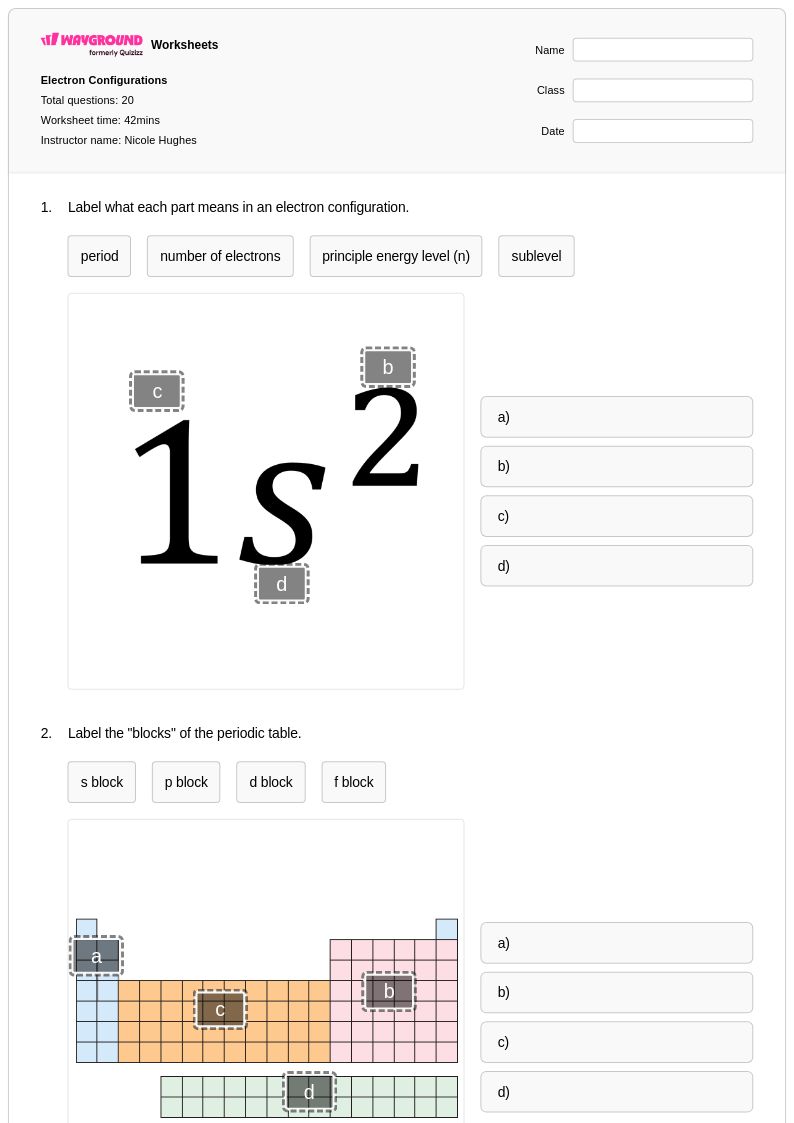
Electron Configurations

Electron Configuration

Atomic Structure

Electron Configuration & Groups on the Periodic table

Unit 2 Test Practice (Atomic Theory)

4.3 Electron Configuration
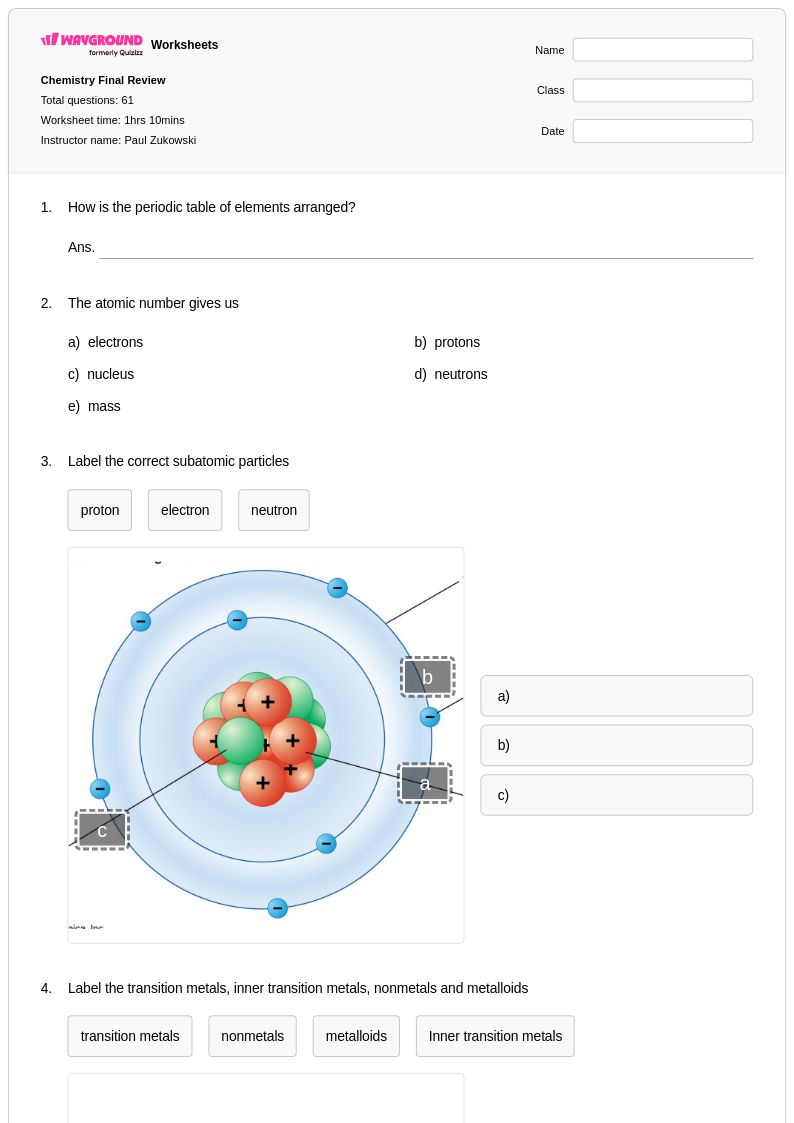
Chemistry Final Review

1.5 - Electron Configuration

Properties of Matter, the Atom, and Periodic Table

Matter and Atoms Test

Unit 7 (The Atom) Quiz Review

U1: Electron Configurations: Mastery Test

Atomic Structure Quiz

Chemistry Fourth Quarter Extra Credit

24Unit 1: Atoms & Chemical Bonding/Reactions STUDY GUIDE
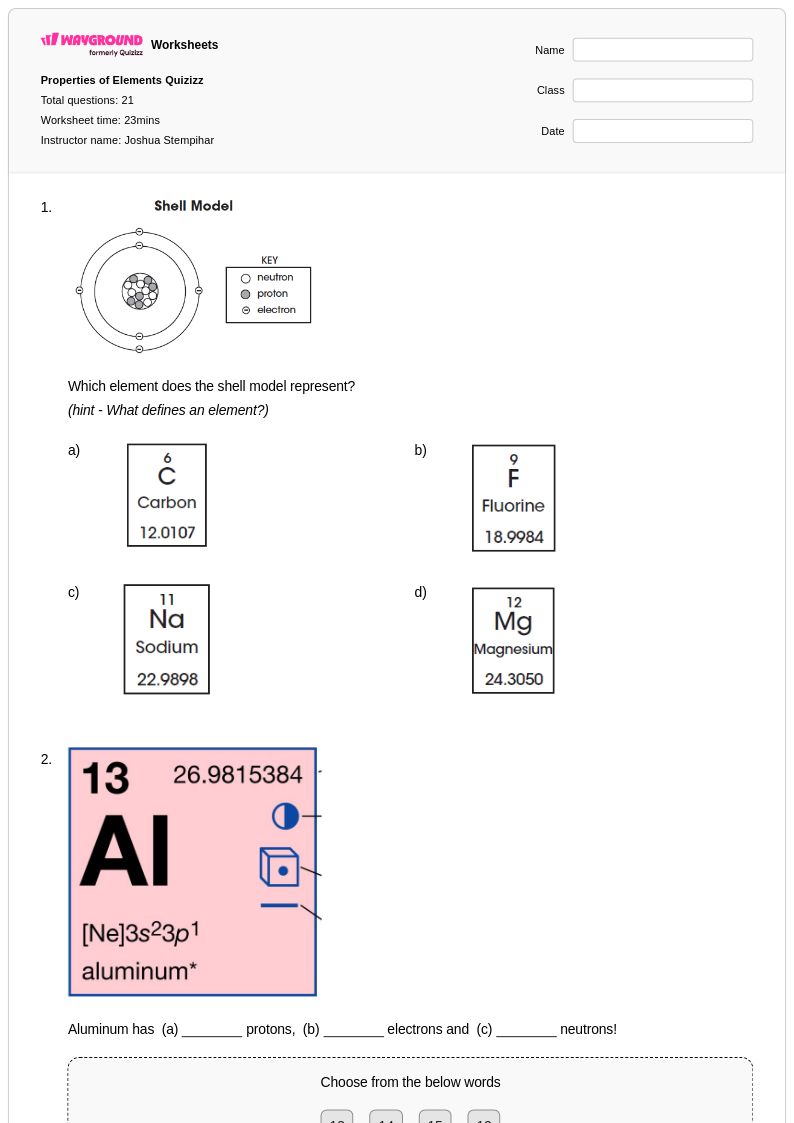
Properties of Elements Quizizz
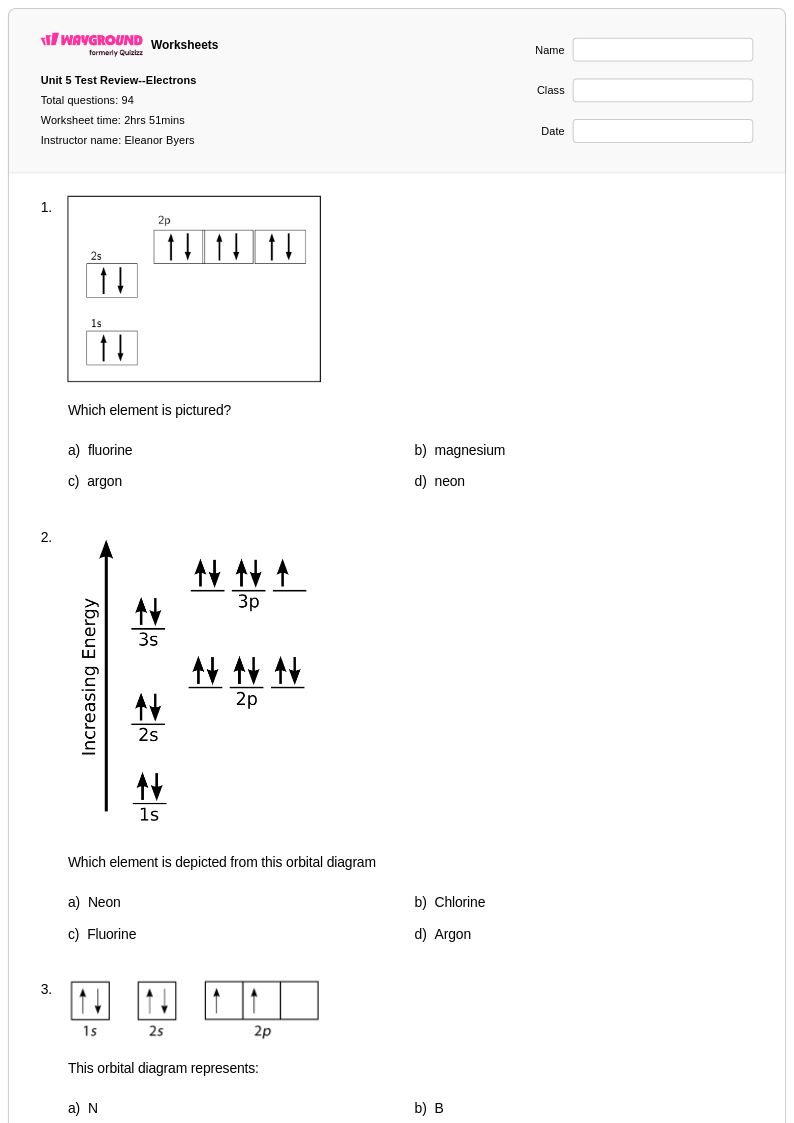
Unit 5 Test Review--Electrons
Electron Behavior and Arrangement Quiz

Chemistry Q2 Review
สำรวจแผ่นงาน แผนภาพวงโคจรอะตอม ที่พิมพ์ได้
แบบฝึกหัดแผนภาพวงโคจรอะตอมที่จัดทำโดย Wayground (เดิมคือ Quizizz) มอบโอกาสในการฝึกฝนอย่างครอบคลุมสำหรับนักเรียนในการเรียนรู้การมองเห็นและการทำความเข้าใจการจัดเรียงอิเล็กตรอนในอะตอม แบบฝึกหัดที่ออกแบบมาอย่างเชี่ยวชาญเหล่านี้ช่วยเสริมสร้างทักษะที่สำคัญ ได้แก่ การวาดแผนภาพวงโคจรโดยใช้ลูกศรเพื่อแสดงการหมุนของอิเล็กตรอน การประยุกต์ใช้กฎของฮุนด์สำหรับการจัดวางอิเล็กตรอนภายในซับเชลล์ และความเข้าใจความสัมพันธ์ระหว่างเลขควอนตัมและรูปร่างของวงโคจร นักเรียนจะได้ฝึกฝนผ่านโจทย์ปัญหาอย่างเป็นระบบที่ค่อยๆ พัฒนาจากโครงสร้างอะตอมไฮโดรเจนอย่างง่ายไปจนถึงอะตอมที่มีอิเล็กตรอนหลายตัวที่ซับซ้อนมากขึ้น โดยแบบฝึกหัดแต่ละชุดจะมีเฉลยคำตอบโดยละเอียดที่อธิบายขั้นตอนการสร้างแผนภาพวงโคจรที่ถูกต้องอย่างละเอียด เอกสารที่พิมพ์ได้ฟรีเหล่านี้ครอบคลุมแนวคิดที่สำคัญ เช่น การประยุกต์ใช้หลักการเอาฟ์บาว การเรียงลำดับระดับพลังงานของวงโคจร และความแตกต่างระหว่างสัญลักษณ์วงโคจรและสัญลักษณ์การจัดเรียงอิเล็กตรอน เพื่อให้แน่ใจว่านักเรียนจะพัฒนาทั้งความเข้าใจเชิงแนวคิดและทักษะการวาดแผนภาพในทางปฏิบัติ
Wayground (เดิมชื่อ Quizizz) ช่วยเสริมศักยภาพครูผู้สอนด้วยชุดสื่อการสอนเกี่ยวกับแผนภาพวงโคจรอะตอมที่สร้างโดยครูจำนวนมาก โดยดึงมาจากแบบฝึกหัดคุณภาพสูงนับล้านฉบับที่ผ่านการทดสอบและปรับปรุงในห้องเรียนแล้ว แพลตฟอร์มนี้มีฟังก์ชันการค้นหาและการกรองที่ทรงประสิทธิภาพ ช่วยให้ครูสามารถค้นหาสื่อที่สอดคล้องกับวัตถุประสงค์และมาตรฐานการเรียนรู้เฉพาะได้อย่างรวดเร็ว ในขณะที่เครื่องมือการปรับระดับความยากง่ายในตัวช่วยให้สามารถปรับแต่งตามความต้องการและระดับทักษะของนักเรียนแต่ละคนได้ แบบฝึกหัดแผนภาพวงโคจรเหล่านี้มีให้เลือกทั้งในรูปแบบไฟล์ PDF ที่พิมพ์ได้สำหรับการใช้งานในห้องเรียนแบบดั้งเดิม และรูปแบบดิจิทัลสำหรับสภาพแวดล้อมการเรียนรู้แบบโต้ตอบ ซึ่งให้ความยืดหยุ่นสูงสุดสำหรับการวางแผนและการดำเนินการสอน ครูสามารถบูรณาการแหล่งข้อมูลเหล่านี้เข้ากับหลักสูตรได้อย่างราบรื่นสำหรับการพัฒนาทักษะเบื้องต้น การแก้ไขความเข้าใจผิดเกี่ยวกับการจัดเรียงอิเล็กตรอน หรือกิจกรรมเสริมที่ท้าทายนักเรียนระดับสูงให้รับมือกับการจัดเรียงวงโคจรของโลหะทรานซิชันและแลนทานัมที่ซับซ้อน
FAQs
ฉันจะสอนแผนภาพวงโคจรอะตอมให้แก่นักเรียนวิชาเคมีได้อย่างไร?
เริ่มต้นด้วยการอธิบายกฎหลักสามข้อที่ควบคุมการจัดเรียงอิเล็กตรอนให้แก่นักเรียน ได้แก่ หลักการเอาฟ์บาว (เติมออร์บิทัลที่มีพลังงานต่ำที่สุดก่อน) หลักการกีดกันของเปาลี (อิเล็กตรอนสองตัวจะไม่ใช้เลขควอนตัมสี่ตัวเดียวกัน) และกฎของฮุนด์ (เพิ่มจำนวนอิเล็กตรอนที่ไม่จับคู่ภายในซับเชลล์ให้มากที่สุดก่อนที่จะจับคู่) เริ่มจากอะตอมอย่างง่าย เช่น ไฮโดรเจนและฮีเลียม ก่อนที่จะไปยังอะตอมที่มีอิเล็กตรอนหลายตัว โดยใช้แผนภาพที่มีลูกศรเพื่อแสดงทิศทางการหมุน การเชื่อมโยงสัญลักษณ์ออร์บิทัลเข้ากับสัญลักษณ์การจัดเรียงอิเล็กตรอนอย่างชัดเจนจะช่วยให้นักเรียนเห็นว่าทั้งสองแบบอธิบายโครงสร้างพื้นฐานเดียวกัน
แบบฝึกหัดใดบ้างที่ช่วยให้นักเรียนฝึกฝนการวาดแผนภาพวงโคจร?
การฝึกฝนที่มีประสิทธิภาพเริ่มต้นด้วยแผนภาพซับเชลล์เดี่ยวสำหรับธาตุในคาบที่ 1 และ 2 จากนั้นค่อยๆ แนะนำการเติมซับเชลล์ d สำหรับโลหะทรานซิชัน ซึ่งเป็นบริเวณที่มักเกิดข้อผิดพลาดบ่อยครั้ง แบบฝึกหัดที่ให้นักเรียนแปลงระหว่างสัญลักษณ์ออร์บิทัลและสัญลักษณ์การจัดเรียงอิเล็กตรอนจะช่วยเสริมความเข้าใจทั้งสองรูปแบบไปพร้อมๆ กัน การรวมปัญหาที่ต้องการให้นักเรียนระบุจำนวนอิเล็กตรอนที่ไม่มีคู่จากแผนภาพที่สมบูรณ์จะเพิ่มชั้นการประยุกต์ใช้ที่ช่วยให้เข้าใจแนวคิดได้ลึกซึ้งยิ่งขึ้น
นักเรียนมักทำผิดพลาดอะไรบ้างเมื่อวาดแผนภาพวงโคจรอะตอม?
ข้อผิดพลาดที่พบบ่อยที่สุดคือการละเมิดกฎของฮุนด์โดยการจับคู่อิเล็กตรอนในซับเชลล์ก่อนที่ออร์บิทัลทั้งหมดในซับเชลล์นั้นจะมีอิเล็กตรอนเพียงตัวเดียว นักเรียนมักเรียงลำดับระดับพลังงานของออร์บิทัลผิดพลาด โดยเฉพาะอย่างยิ่งการวาง 4s ไว้เหนือ 3d แทนที่จะอยู่ด้านล่างเมื่อทำการเติมอิเล็กตรอน ความเข้าใจผิดที่พบบ่อยประการที่สามคือการใช้แผนภาพออร์บิทัลแทนสัญลักษณ์การจัดเรียงอิเล็กตรอน โดยไม่ตระหนักว่าแผนภาพออร์บิทัลนั้นมีข้อมูลเพิ่มเติมเกี่ยวกับสปินของอิเล็กตรอนและการครอบครองซับเชลล์
ฉันจะใช้แบบฝึกหัดแผนภาพวงโคจรอะตอมในห้องเรียนได้อย่างไร?
แบบฝึกหัดแผนภาพวงโคจรอะตอมบน Wayground มีให้เลือกทั้งแบบไฟล์ PDF ที่สามารถพิมพ์ได้สำหรับการใช้งานในห้องเรียนแบบดั้งเดิม และแบบดิจิทัลสำหรับสภาพแวดล้อมที่บูรณาการเทคโนโลยี รวมถึงตัวเลือกในการจัดทำเป็นแบบทดสอบโดยตรงบน Wayground เวอร์ชันที่พิมพ์ได้เหมาะสำหรับการจดบันทึกประกอบการเรียนหรือการฝึกฝนแบบห้องปฏิบัติการ ในขณะที่รูปแบบดิจิทัลช่วยให้ครูสามารถมอบหมายงานแบบไม่พร้อมกันหรือติดตามการตอบสนองของนักเรียนได้แบบเรียลไทม์ แบบฝึกหัดแต่ละชุดมีเฉลยคำตอบโดยละเอียด ทำให้มีประโยชน์อย่างยิ่งสำหรับการฝึกฝนของนักเรียนด้วยตนเอง กิจกรรมการทบทวนโดยเพื่อน หรือการแก้ไขปัญหาเฉพาะด้าน
ฉันจะปรับวิธีการสอนเรื่องแผนภาพวงโคจรอะตอมให้เหมาะสมกับนักเรียนที่มีระดับความสามารถแตกต่างกันได้อย่างไร?
สำหรับนักเรียนที่ต้องการความช่วยเหลือเพิ่มเติม ให้ลดความซับซ้อนของอะตอมที่กำหนด และใช้แผนภาพที่สร้างเสร็จบางส่วนเป็นโครงร่างก่อนที่จะกำหนดให้สร้างแผนภาพด้วยตนเอง ใน Wayground ครูสามารถปรับการสอนเป็นรายบุคคลได้ เช่น การอ่านออกเสียงข้อความคำถาม หรือลดตัวเลือกคำตอบ เพื่อลดภาระทางความคิดสำหรับนักเรียนบางคน โดยไม่ส่งผลกระทบต่อประสบการณ์ของนักเรียนคนอื่นๆ ในชั้นเรียน นักเรียนที่มีความสามารถสูงสามารถได้รับความท้าทายเกี่ยวกับโครงสร้างอะตอมของโลหะทรานซิชัน และข้อยกเว้น เช่น โครเมียมและทองแดง ซึ่งรูปแบบการเติมแบบ aufbau ที่คาดไว้ไม่สามารถนำมาใช้ได้
เลขควอนตัมมีความสัมพันธ์กับแผนภาพวงโคจรอะตอมอย่างไร?
แต่ละออร์บิทัลในแผนภาพจะสอดคล้องกับชุดเลขควอนตัมที่ไม่ซ้ำกัน: เลขควอนตัมหลัก (n) กำหนดระดับพลังงาน เลขควอนตัมโมเมนตัมเชิงมุม (l) กำหนดรูปร่างของซับเชลล์ เลขควอนตัมแม่เหล็ก (ml) ระบุออร์บิทัลเฉพาะภายในซับเชลล์ และเลขควอนตัมสปิน (ms) แยกแยะอิเล็กตรอนสองตัวที่สามารถครอบครองออร์บิทัลเดียวได้ แผนภาพออร์บิทัลทำให้กรอบนามธรรมนี้เป็นรูปธรรมโดยการแสดงค่า ml ที่อนุญาตแต่ละค่าเป็นกล่อง และค่า ms ของอิเล็กตรอนแต่ละตัวเป็นลูกศรขึ้นหรือลง การเชื่อมโยงนี้ช่วยให้นักเรียนเข้าใจว่าทำไม ตัวอย่างเช่น ซับเชลล์ p จึงมีกล่องสามกล่องพอดีและสามารถบรรจุอิเล็กตรอนได้สูงสุดหกตัว
























