
Energy Levels, Sublevels, and Atomic Orbitals
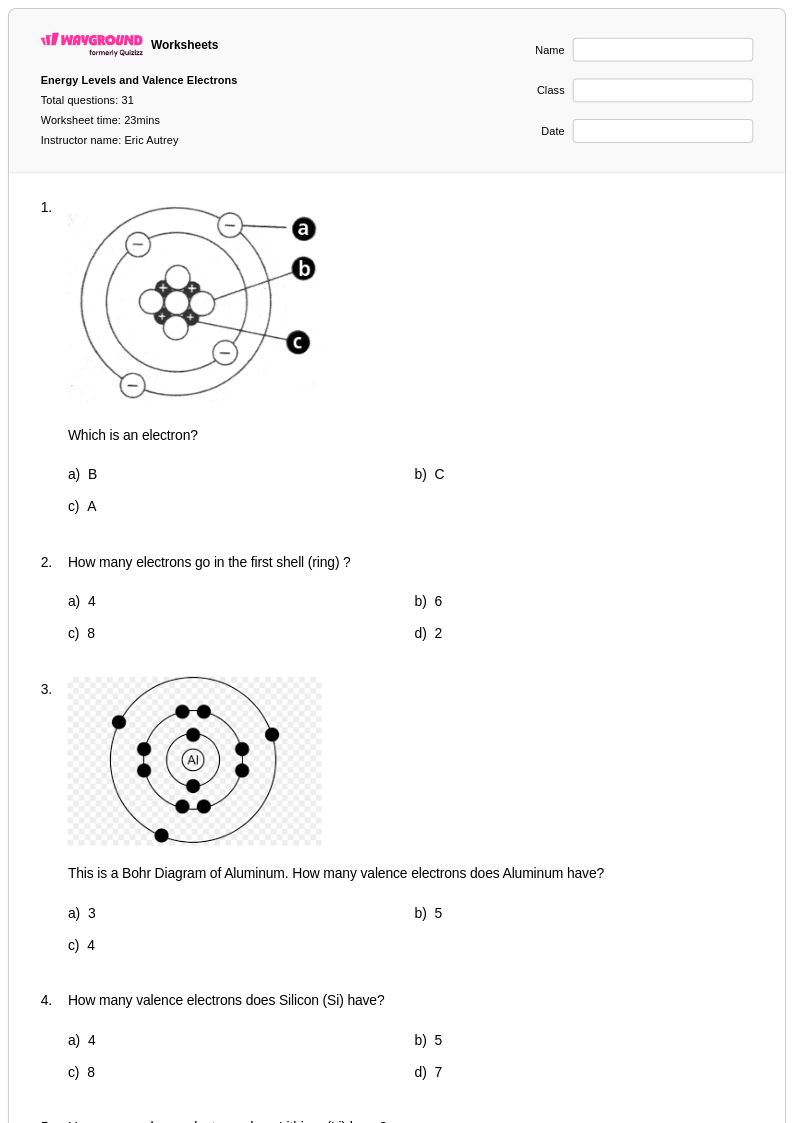
Energy Levels and Valence Electrons

Energy Flow
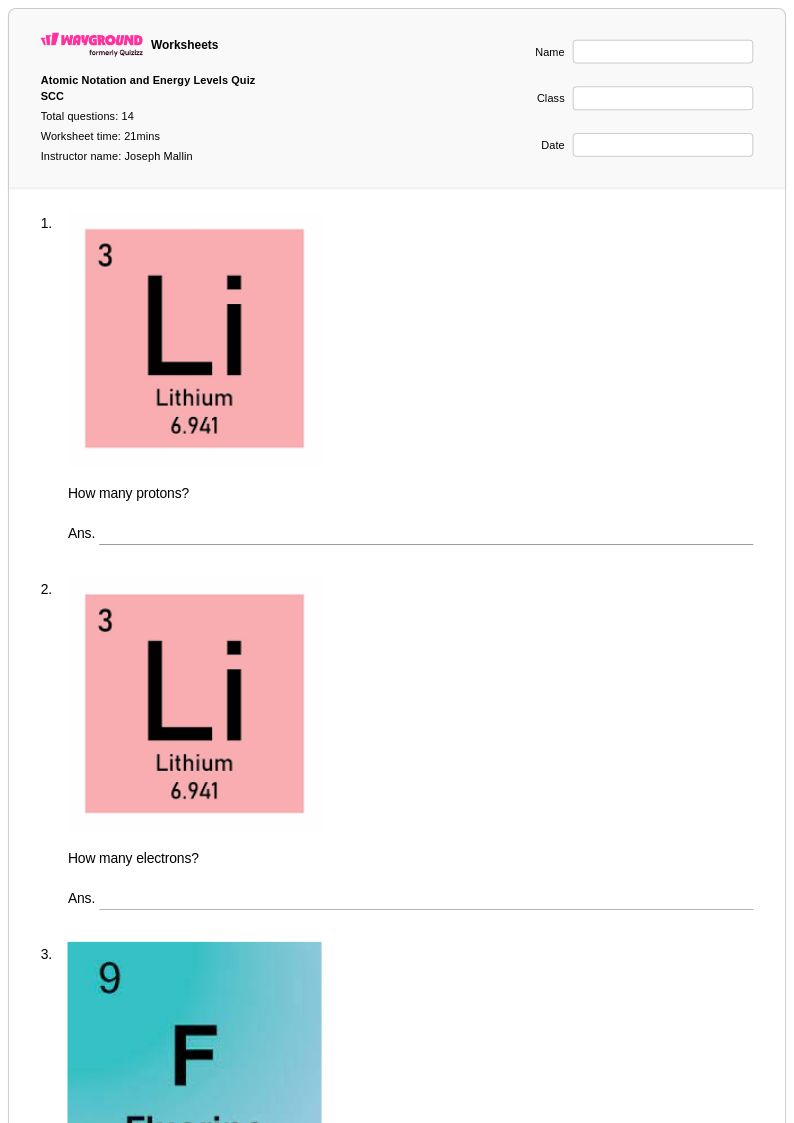
Atomic Notation and Energy Levels Quiz SCC

Energy Flow

Properties of Atoms Review

Food Webs & Chains
Levels of Organization
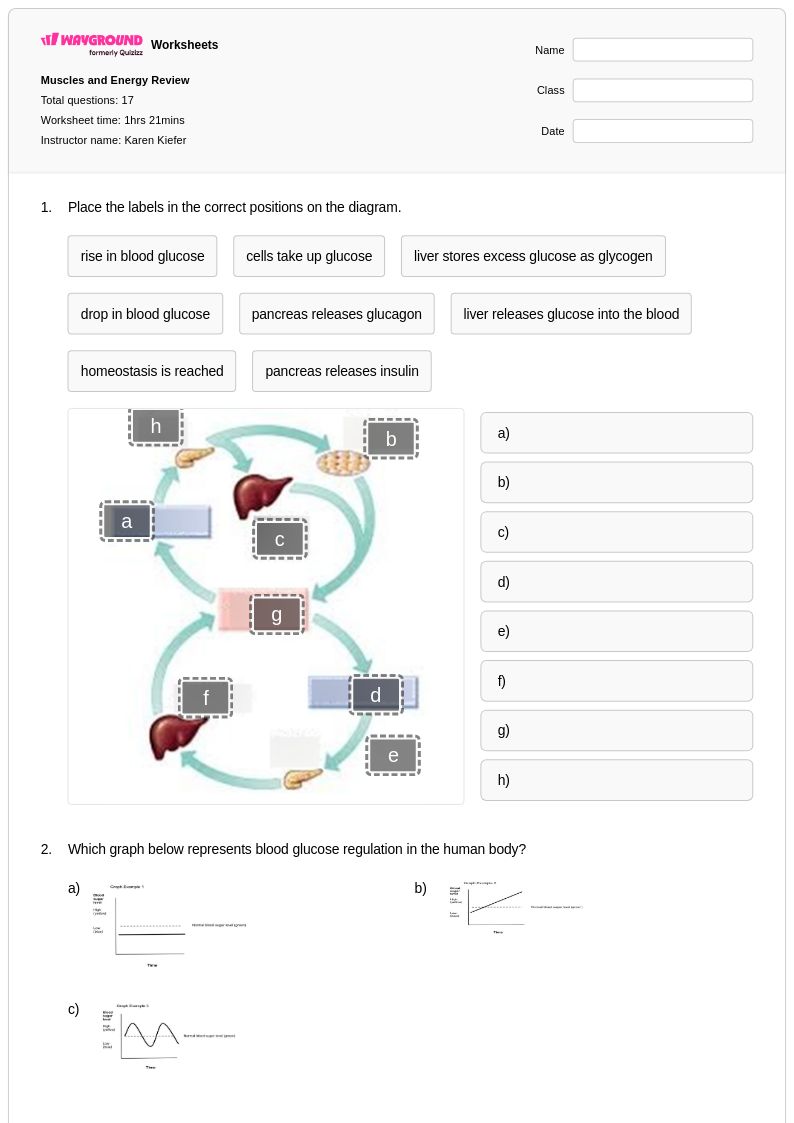
Muscles and Energy Review
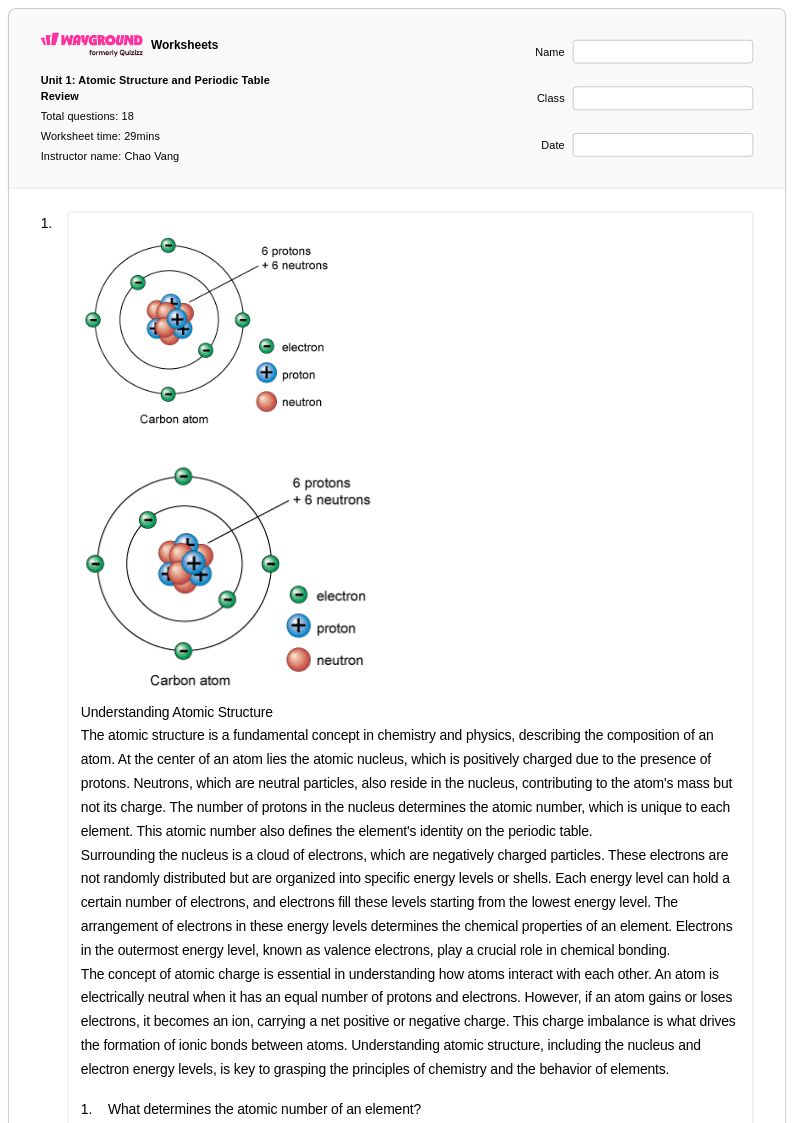
Unit 1: Atomic Structure and Periodic Table Review
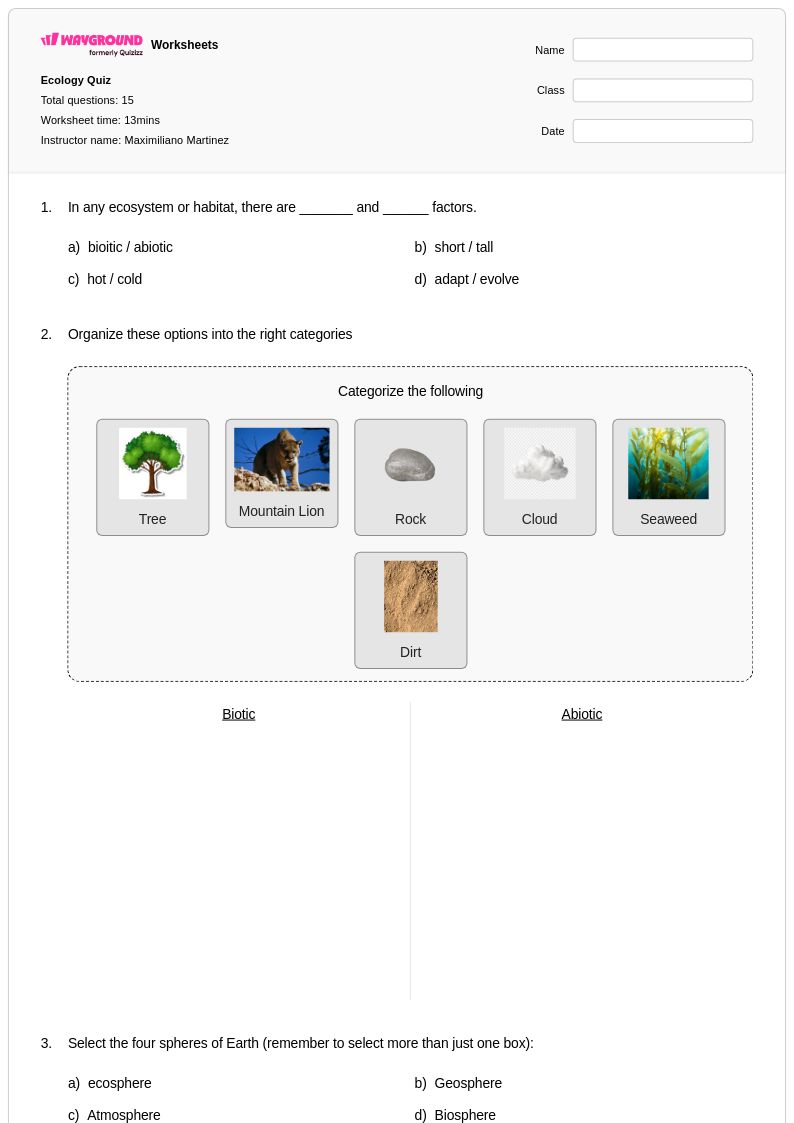
Ecology Quiz

Biology Energy Flow Review

Cell Energy Review

Chpt 2 Energy & Matter HonorsTest

Trophic Levels and Biodiversity Quiz

3.6 Bio Unit 3 Review: Ecosystems, Matter, and Populations Quiz

Biology Unit 3 Ecology Test 2024-2025

5.1 Atomic Structure Notes Practice
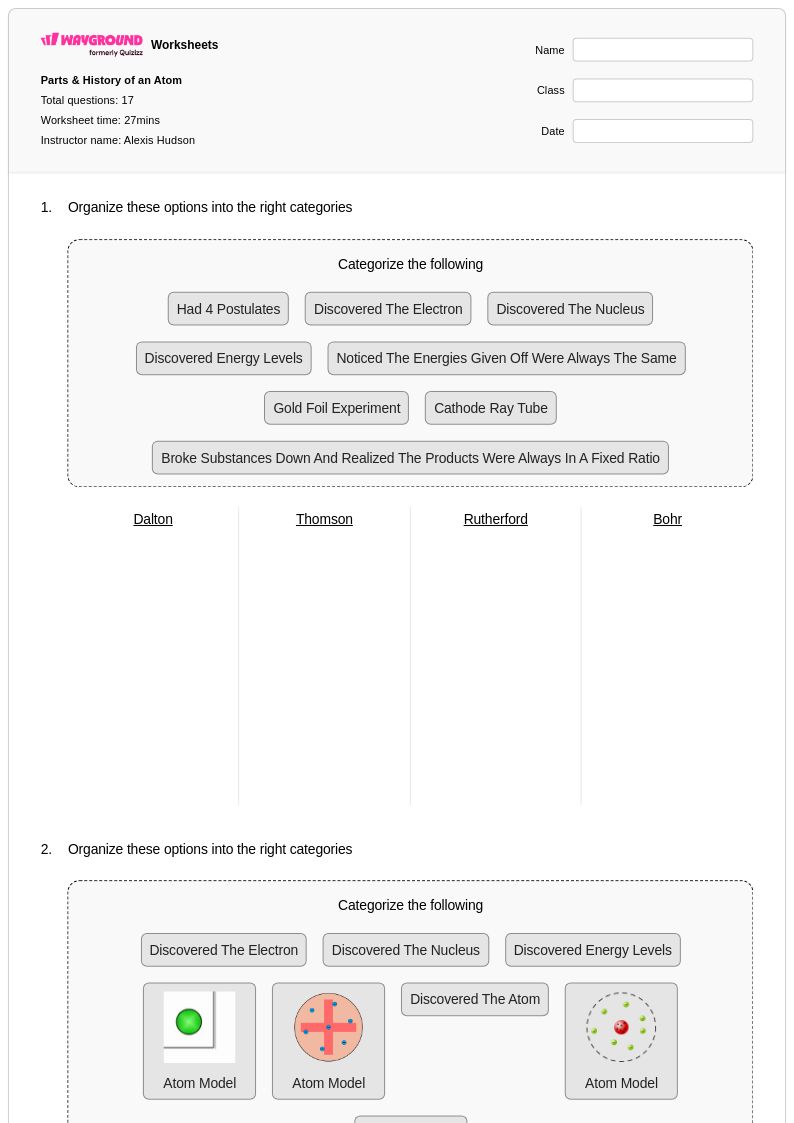
Parts & History of an Atom

Investigation 14 | Energy Flow | Biology

Cycles of Energy Review

Review - 4.3 Photosynthesis
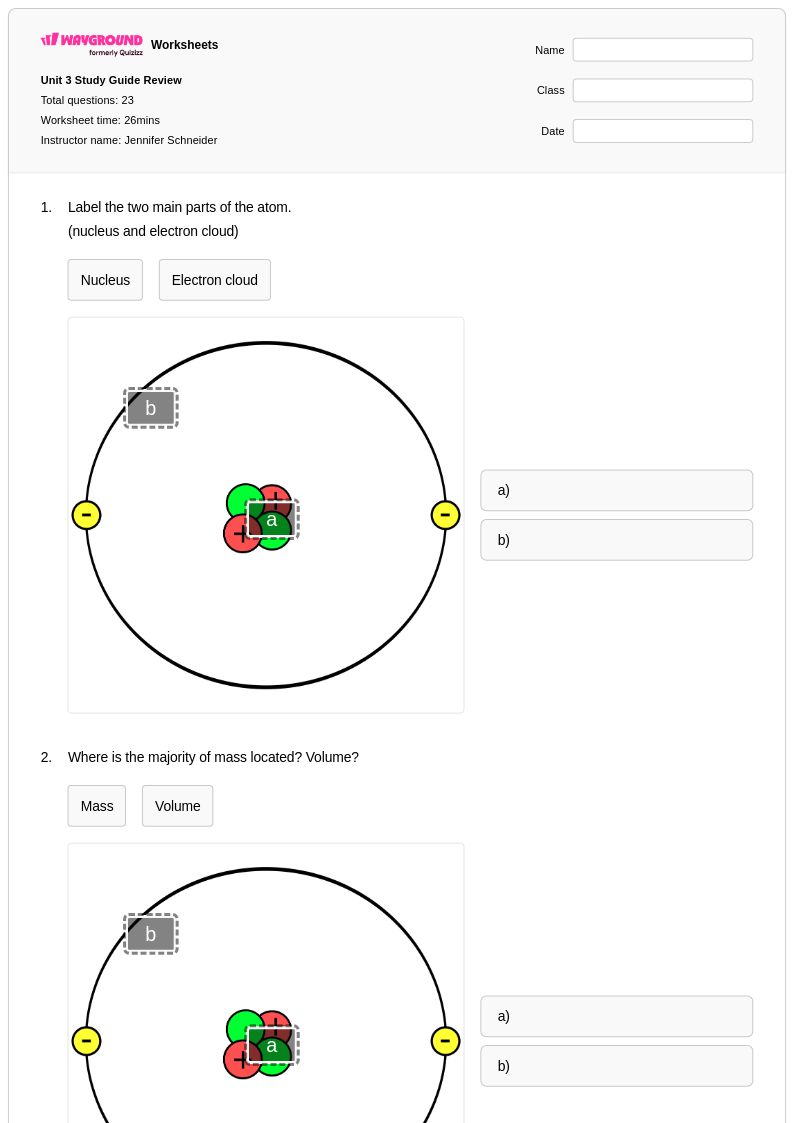
Unit 3 Study Guide Review

Atomic Structure and Models Quiz
สำรวจแผ่นงาน ระดับพลังงาน ตามเกรด
สำรวจใบงานวิชาอื่นๆ สำหรับ ระดับ 9
สำรวจแผ่นงาน ระดับพลังงาน ที่พิมพ์ได้สำหรับ ชั้นประถมศึกษาปีที่ 9
แบบฝึกหัดเรื่องระดับพลังงานสำหรับวิชาเคมี ชั้น ม.3 มีเนื้อหาฝึกฝนที่ครอบคลุม ช่วยให้นักเรียนเข้าใจแนวคิดพื้นฐานของโครงสร้างอะตอมและการจัดเรียงอิเล็กตรอนอย่างถ่องแท้ แบบฝึกหัดเหล่านี้ได้รับการออกแบบอย่างพิถีพิถัน ช่วยแนะนำนักเรียนให้เข้าใจว่าอิเล็กตรอนอยู่ในระดับพลังงานเฉพาะรอบนิวเคลียสได้อย่างไร ความสัมพันธ์ระหว่างพลังงานและระยะห่างของอิเล็กตรอนจากนิวเคลียส และแผนภาพระดับพลังงานแสดงถึงโครงสร้างอะตอมอย่างไร แบบฝึกหัดเหล่านี้ช่วยเสริมสร้างทักษะการคิดเชิงวิเคราะห์ผ่านแบบฝึกหัดที่ให้นักเรียนวาดแผนภาพระดับพลังงาน คำนวณความแตกต่างของพลังงานระหว่างระดับ และอธิบายการเปลี่ยนสถานะของอิเล็กตรอน แบบฝึกหัดแต่ละชุดมีเฉลยคำตอบโดยละเอียด ทำให้มีคุณค่าทั้งในการเรียนการสอนในห้องเรียนและการเรียนรู้ด้วยตนเอง และรูปแบบที่สามารถพิมพ์ได้ฟรีช่วยให้เข้าถึงได้ในทุกสภาพแวดล้อมการเรียนรู้
Wayground ซึ่งเดิมชื่อ Quizizz ช่วยให้ครูผู้สอนมีแบบฝึกหัดเรื่องระดับพลังงานที่สร้างโดยครูหลายล้านชุด ซึ่งสอดคล้องกับมาตรฐานและวัตถุประสงค์การเรียนรู้ของวิชาเคมี ชั้น ม.3 โดยเฉพาะ ความสามารถในการค้นหาและกรองข้อมูลที่แข็งแกร่งของแพลตฟอร์มช่วยให้ครูสามารถค้นหาสื่อที่ตรงกับความต้องการหลักสูตรเฉพาะของตนได้อย่างรวดเร็ว ไม่ว่าจะเป็นการเน้นที่แนวคิดพื้นฐานเกี่ยวกับระดับพลังงานหรือหัวข้อการจัดเรียงอิเล็กตรอนขั้นสูงก็ตาม แหล่งข้อมูลเหล่านี้สนับสนุนการสอนที่แตกต่างกันไปตามระดับความสามารถ โดยมีคุณสมบัติที่ปรับแต่งได้ ซึ่งช่วยให้ครูสามารถแก้ไขแบบฝึกหัดให้เหมาะสมกับระดับทักษะต่างๆ ได้ ในขณะที่การมีทั้งเวอร์ชัน PDF ที่พิมพ์ได้และรูปแบบดิจิทัลแบบโต้ตอบได้นั้น ช่วยเพิ่มความยืดหยุ่นให้กับสภาพแวดล้อมในห้องเรียนที่หลากหลาย ครูสามารถบูรณาการแบบฝึกหัดเหล่านี้เข้ากับการวางแผนบทเรียนได้อย่างราบรื่น ไม่ว่าจะเป็นการแนะนำทักษะเบื้องต้น การแก้ไขปัญหาเฉพาะหน้าสำหรับนักเรียนที่เรียนรู้ช้า หรือกิจกรรมเสริมสำหรับผู้เรียนที่มีความสามารถสูง เพื่อให้มั่นใจได้ว่ามีการครอบคลุมแนวคิดเรื่องระดับพลังงานอย่างครบถ้วนในทุกระดับความสามารถของนักเรียน
FAQs
ฉันจะสอนเรื่องระดับพลังงานและการจัดเรียงอิเล็กตรอนในวิชาเคมีได้อย่างไร?
เริ่มต้นด้วยการอธิบายแบบจำลองอะตอมของโบห์รให้นักเรียนเข้าใจ โดยระบุว่าอิเล็กตรอนจะอยู่ในระดับพลังงานที่แยกจากกัน โดยมีระยะห่างจากนิวเคลียสเพิ่มขึ้นเรื่อยๆ จากนั้นจึงแนะนำหลักการเอาฟ์บาว (aufbau principle) หลักการกีดกันของเปาลี (Pauli exclusion principle) และกฎของฮุนด์ (Hund's rule) ซึ่งเป็นกฎสามข้อที่ควบคุมการเติมอิเล็กตรอนในออร์บิทัล การใช้แผนภาพออร์บิทัลควบคู่ไปกับการเขียนการจัดเรียงอิเล็กตรอนจะช่วยให้นักเรียนเห็นภาพลำดับการเติมก่อนที่จะใช้สัญลักษณ์ย่อ การเชื่อมโยงระดับพลังงานกับแนวโน้มในตารางธาตุ เช่น พลังงานไอออนไนเซชันและรัศมีอะตอม จะช่วยให้นักเรียนเข้าใจแนวคิดได้อย่างเป็นรูปธรรมมากกว่าการท่องจำกฎเพียงอย่างเดียว
แบบฝึกหัดใดบ้างที่ช่วยให้นักเรียนฝึกฝนการจัดเรียงอิเล็กตรอนและระดับพลังงาน?
การฝึกฝนที่มีประสิทธิภาพจะช่วยให้นักเรียนพัฒนาจากสิ่งที่เป็นรูปธรรมไปสู่สิ่งที่เป็นนามธรรม: เริ่มต้นด้วยแผนภาพระดับพลังงานที่ให้นักเรียนวาดและเติมอิเล็กตรอนในแต่ละชั้นของธาตุอย่างง่าย จากนั้นจึงค่อยเรียนรู้เรื่องสัญลักษณ์ของวงโคจร และสุดท้ายคือการเขียนโครงสร้างอิเล็กตรอนแบบเต็มและแบบย่อของก๊าซเฉื่อย แบบฝึกหัดที่ให้นักเรียนระบุจำนวนอิเล็กตรอนในแต่ละชั้น หาค่าอิเล็กตรอนวาเลนซ์ และเขียนโครงสร้างอิเล็กตรอนสำหรับโลหะทรานซิชัน จะช่วยสร้างความคล่องแคล่วในระดับชั้นที่จำเป็นสำหรับหัวข้อนี้ การรวมโจทย์ที่เชื่อมโยงโครงสร้างอิเล็กตรอนกับการเกิดไอออนหรือแนวโน้มในตารางธาตุ จะเพิ่มบริบทเชิงประยุกต์ที่ช่วยเสริมความเข้าใจว่าทำไมทักษะนี้จึงมีความสำคัญ
นักเรียนมักทำผิดพลาดอะไรบ้างเกี่ยวกับระดับพลังงานและการจัดเรียงอิเล็กตรอน?
ข้อผิดพลาดที่พบบ่อยที่สุดคือการใช้หลักการเอาฟ์เบา (aufbau principle) ผิดวิธี โดยเฉพาะอย่างยิ่งกับซับเชลล์ 3d และ 4s — นักเรียนมักจะวางอิเล็กตรอนใน 3d ก่อน 4s เมื่อเขียนการจัดเรียงอิเล็กตรอน หรือไม่คำนึงถึงข้อยกเว้นในโครเมียมและทองแดง ความเข้าใจผิดอีกประการหนึ่งคือการถือว่าเปลือกพลังงานและซับเชลล์มีความหมายเหมือนกัน ซึ่งทำให้เกิดความสับสนเมื่อนักเรียนพบแผนภาพออร์บิทัล นอกจากนี้ นักเรียนยังนับอิเล็กตรอนสำหรับไอออนผิดพลาดบ่อยครั้ง โดยลืมเพิ่มหรือลดอิเล็กตรอนตามประจุก่อนเขียนการจัดเรียงอิเล็กตรอน
ฉันจะปรับวิธีการสอนเรื่องระดับพลังงานให้เหมาะสมกับนักเรียนที่มีระดับทักษะแตกต่างกันได้อย่างไร?
สำหรับนักเรียนระดับเริ่มต้น ให้เน้นที่ชั้นพลังงานและกฎความจุอิเล็กตรอน (2, 8, 8) โดยใช้ธาตุในคาบที่ 1-3 ง่ายๆ ก่อนที่จะแนะนำสัญลักษณ์ซับเชลล์ นักเรียนระดับสูงหรือนักเรียนเกียรตินิยมสามารถต่อยอดไปสู่เลขควอนตัม เขียนเลขควอนตัมทั้งสี่สำหรับอิเล็กตรอนเฉพาะ และสำรวจข้อยกเว้นของหลักการเอาฟ์เบาในโลหะทรานซิชัน บน Wayground ครูสามารถปรับการสอนได้ เช่น ลดตัวเลือกคำตอบ หรือช่วยอ่านออกเสียงสำหรับนักเรียนแต่ละคนที่ต้องการความช่วยเหลือเพิ่มเติม ในขณะที่นักเรียนคนอื่นๆ ในชั้นเรียนทำงานภายใต้การตั้งค่ามาตรฐาน ทั้งหมดนี้ภายในงานเดียวกัน
ฉันจะใช้แบบฝึกหัดระดับพลังงานของ Wayground ในห้องเรียนได้อย่างไร?
แบบฝึกหัดระดับพลังงานของ Wayground มีให้เลือกทั้งแบบไฟล์ PDF สำหรับพิมพ์ใช้ในห้องเรียนแบบดั้งเดิม และแบบดิจิทัลสำหรับสภาพแวดล้อมที่บูรณาการเทคโนโลยี ช่วยให้ครูมีความยืดหยุ่นไม่ว่าห้องเรียนจะมีรูปแบบใดก็ตาม ครูสามารถมอบหมายแบบฝึกหัดเวอร์ชันดิจิทัลได้โดยตรงผ่านแพลตฟอร์ม และจัดทำเป็นแบบทดสอบบน Wayground ทำให้สามารถติดตามคำตอบของนักเรียนได้แบบเรียลไทม์ แบบฝึกหัดทุกชุดมีเฉลยคำตอบ ซึ่งสนับสนุนการฝึกฝนด้วยตนเอง การบ้าน และการทบทวนด้วยตนเองโดยไม่ต้องเตรียมการเพิ่มเติมจากครู
ระดับพลังงานมีความเชื่อมโยงกับแนวคิดทางเคมีที่กว้างขึ้น เช่น แนวโน้มตามคาบและพันธะเคมีอย่างไร?
ระดับพลังงานเป็นพื้นฐานสำคัญในการทำความเข้าใจแนวโน้มตามคาบของธาตุ เพราะคุณสมบัติต่างๆ เช่น พลังงานไอออนไนเซชัน ค่าอิเล็กโทรเนกาติวิตี และรัศมีอะตอม ล้วนเป็นผลโดยตรงจากการจัดเรียงตัวของอิเล็กตรอนสัมพันธ์กับนิวเคลียสและอิเล็กตรอนอื่นๆ การจัดเรียงตัวของอิเล็กตรอนในวงโคจรชั้นนอกสุดเป็นตัวกำหนดว่าอะตอมจะสร้างพันธะได้อย่างไร ไม่ว่าจะเป็นพันธะไอออนิก พันธะโคเวเลนต์ หรือพันธะโลหะ ทำให้ความรู้เกี่ยวกับการจัดเรียงตัวของอิเล็กตรอนเป็นสิ่งจำเป็นสำหรับหน่วยพันธะ นักเรียนที่เข้าใจระดับพลังงานสามารถทำนายรูปแบบปฏิกิริยา อธิบายว่าทำไมก๊าซเฉื่อยจึงเสถียร และตีความได้ว่าทำไมโลหะทรานซิชันจึงมีสถานะออกซิเดชันหลายสถานะ
























